Clear Sky Science · he
עיכוב ATM משפר את היעילות של Knock-in על ידי דיכוי הפעלת מסלולי אפופטוזה המועָרים על ידי AAV
שיפור ביצועי עריכת הגנים
עריכת גנים באמצעות CRISPR מבטיחה טיפולים למחלות תורשתיות, גידולים עמידים יותר ותפוקות חזקות למחקר. אך אחת המטלות היקרות ביותר שלו — הכנסת רצף DNA חדש בדיוק במקום נבחר בגנום, המכונה "knock-in" — עדיין אינה יעילה דיין. המחקר הזה חוקר מדוע יש תאים שמקבלים DNA חדש בקלות רבה יותר מאחרים וחושף דרך לעודד תאים לבצע עריכות מדויקות בתדירות גבוהה יותר, במיוחד בעת שימוש בווקטור המוביל בטיפול גנטי, adeno-associated virus (AAV).
צפייה בתיקון DNA בזמן אמת
כדי להבין מה מקדם ומה מעכב הכנסת רצף מדויק, החוקרים בנו לוח בקרה מורכב בתוך תאי גזע עובריים של עכבר. מערכת הטריפל-ריפורטר הזו משתמשת בשלושה סימנים פלואורסצנטיים כדי לעקוב, באותם תאים, האם CRISPR חתך את ה-DNA, האם בוצע knock-in מדויק, והאם התא הדביק במקום זאת את ה-DNA התורם באמצעות שיטת תיקון גס יותר. על ידי קריאת שילובים של צבעים בזרימת תאים (flow cytometry) הם יכלו להפריד בין עריכות נקיות המבוססות על תבנית לבין הכנסת רצפים עם שגיאות ותאים שלא עברו עריכה. המעקב הזה זה לצד זה אפשר להם למפות כיצד מסלולי תיקון DNA שונים תורמים לכל תוצאה ברזולוציה גבוהה הרבה יותר מאשר בדיקות מבוססות PCR ישנות.
שני סוגי תורמים, שתי תגובות שונות מאד
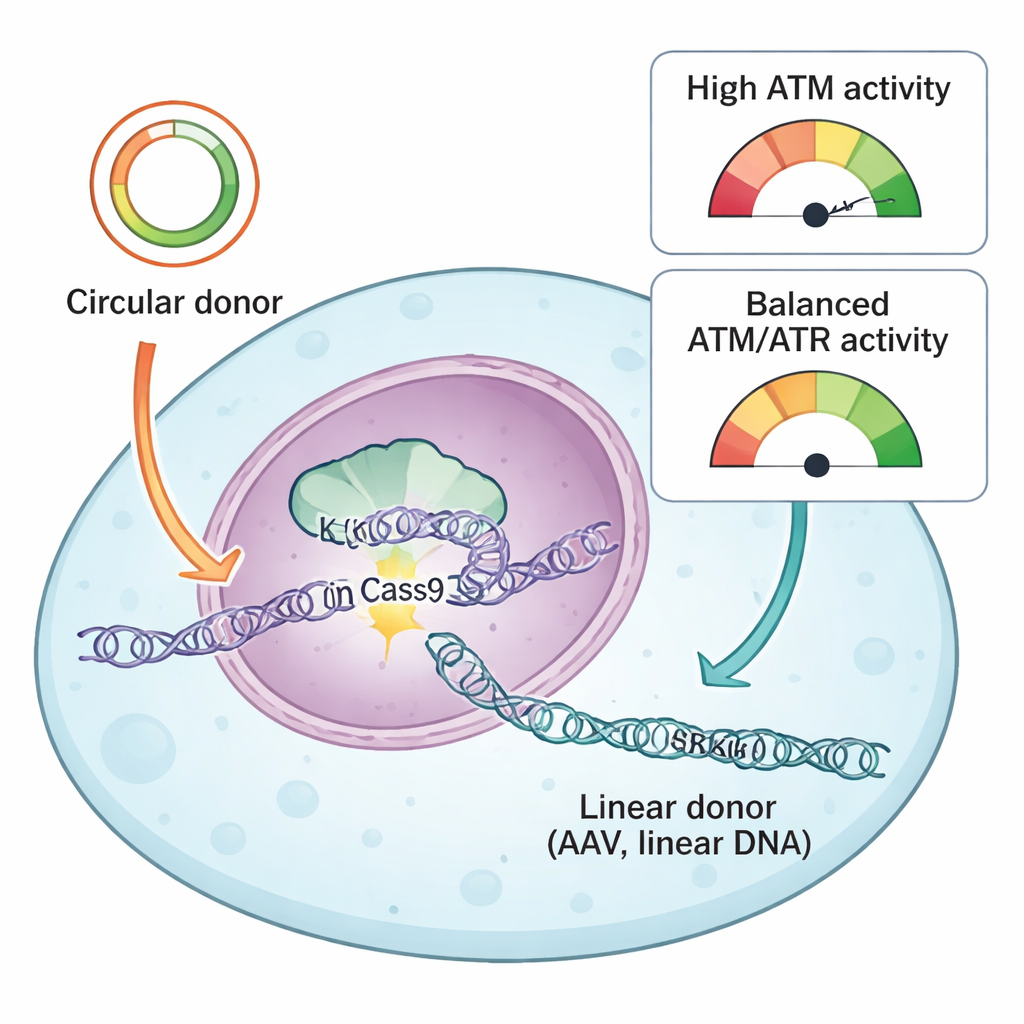
הצוות השווה שני סוגים נפוצים של DNA תורם המשמשים להכוונת תיקוני CRISPR: פלסמידים מעגליים ו-DNA ליניארי שמקורו ב-AAV. שניהם נושאים "זרועות הומולוגיה" תואמות שמורות לתא היכן להכניס את הרצף החדש, אך הם נכנסים לתא בצורות פיזיות שונות. פלסמידים מעגליים הם לולאות סגורות של DNA דו-גדילי, בעוד שתורמי AAV מגיעים בדרך כלל כמולקולות ליניאריות בודדות. באמצעות מערכת הריפורטר וספריית תרופות הפוגעות בחלבוני תגובת נזקי ה-DNA, המחברים מצאו שחלבון מפתח אחד, ATR, הוא נחוץ באופן אחיד להצלחת ה-knock-in עבור שני סוגי התורמים. עיכוב ATR הפחית באופן חד את ההכנסה המדויקת, בעוד החמרה עדינה של פעילות ATR דרך מסלול KEAP1–NRF2 עשתה את ה-knock-ins ליעילים יותר, במיוחד עם תורמי AAV.
מתי ההגנה על ה-DNA פועלת נגדם
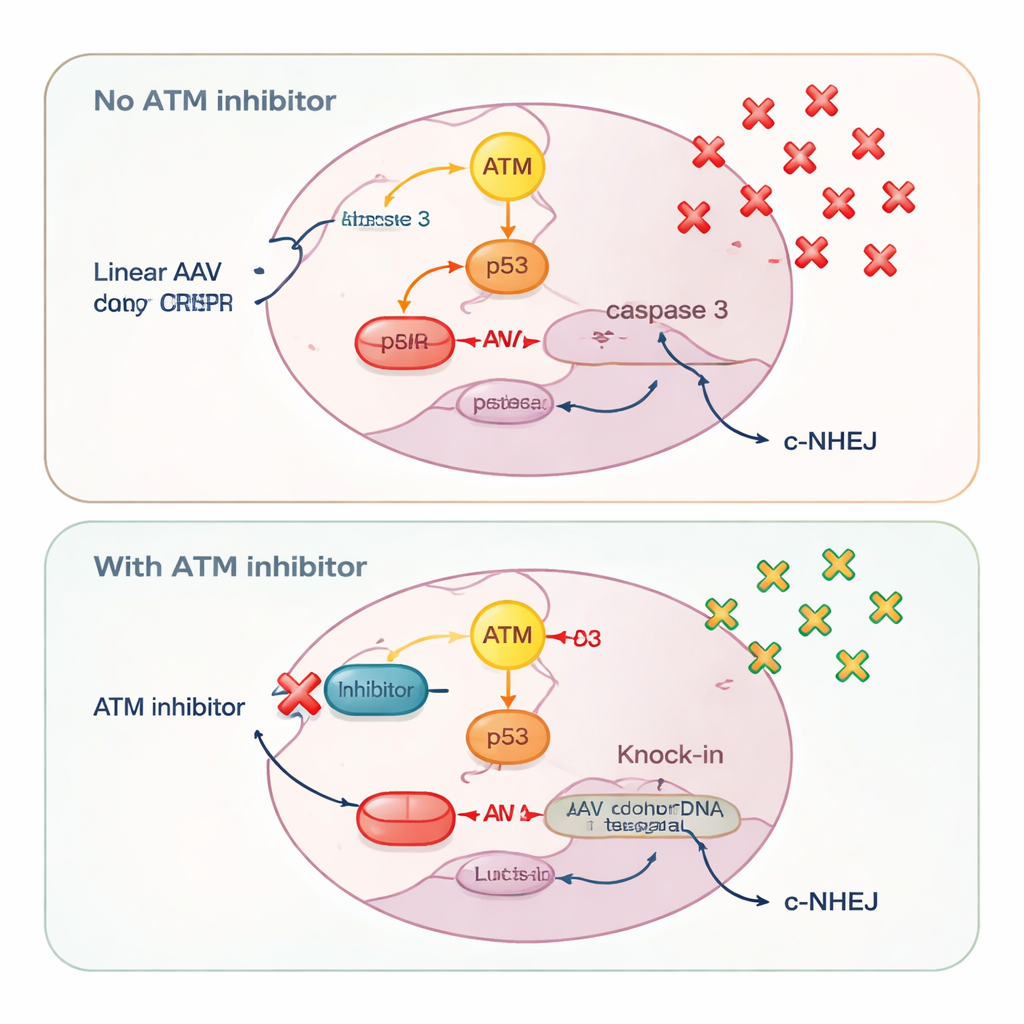
חיישן נזקי DNA אחר, ATM, התגלה כמתנהג בצורה מורכבת התלויה בסוג התורם. עם תורמי פלסמיד מעגליים, חסימת ATM הפחיתה גם את ה-knock-in המדויק וגם את ההכנסות המתווכות על ידי הצמדה קצה-לקצה (end-joining), בהתאמה לתפקידו הקלאסי בעזרה לתאים לתקן שברים דו-גדיליים. אך עם DNA ליניארי — בין אם מ-AAV, מ-AAV עצמי משלים, או מפלסמידים שחתכו לחתיכות ישרות — עיכוב ATM עשה את ההפך: הוא הגדיל את היעילות של ה-knock-in. החוקרים עקבו אחרי השפעה זו וחיברו אותה לאופן שבו תאים מפרשים פרצי DNA ליניארי. מינונים גבוהים של AAV הפעילו חזק את ATM, שבלעדיו הפעיל את p53 ואת caspase 3, שחקנים מרכזיים במוות המתוכנת. תאים שלקחו כמויות רבות של DNA תורם — ובכך היו בעלי הסיכוי הגבוה ביותר ל-knock-in מוצלח — היו גם הסבירים ביותר להיהרג על ידי מערכת האזעקה הזו.
להציל את התאים המצוידים הטובים ביותר
בהוספת מעכבי ATM, המדענים השתקו את מסלול המוות ATM–p53–caspase 3. זה חסך את התאים שנשאו כמויות גבוהות של DNA תורם, ואפשר ליותר מהם להשרוד מספיק זמן להשלים knock-in מדויק. מדידות של עותקי הגנום הויראלי אישרו שעיכוב ATM הגדיל את מספר מולקולות ה-AAV שנשמרו בתוך התאים. במקביל, חסימת ATM דיכאה במידה קלה מסלול תיקון מהיר וקהה שנקרא non-homologous end-joining קלאסי, כפי שהודגם בהפחתת ההפעלה של DNA-PK, אנזים מרכזי במסלול זה. החלשת אפשרות התיקון התחרותית הזו נדחפה יותר חתכי CRISPR לכיוון knock-in מבוסס הומולוגיה במקום תיקונים מהירים שמניחים בצד את תבנית התורם.
מה המשמעות של זה לטיפולי גנים עתידיים
עבור קהל שאינו מומחה, המסר הוא שמנגנוני ההגנה של התא שמגוננים עלינו מפני נזקי DNA עלולים באופן בלתי מכוון לסכל עריכת גנים מדויקת, במיוחד כאשר משתמשים בכמויות גדולות של DNA תורם ויראלי. עבודה זו מראה שניתן לכוונן בעדינות את מנגנוני ההגנה האלה — לשמור על ATR פעיל אך לעכב זמנית את ATM כשנוכחים תורמים ליניאריים כמו AAV — כדי להפוך knock-in של CRISPR לאמין ויעיל יותר. אסטרטגיה כזו עשויה לשפר טיפולי גנים, הנדסת תאים ודגמי מחלות על ידי עידוד יותר תאים לקבל את השינוי המיועד תוך הימנעות מאובדן תאים מיותרת.
ציטוט: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
מילות מפתח: הכנסת CRISPR, עריכת גנים ב-AAV, תגובה לנזקי DNA, עיכוב ATM, הנדסת גנום