Clear Sky Science · he
איפיונן של התכונות הניתנות לפיתוח של ננובודים לשיפור עיצוב תרופתי באמצעות ה‑Therapeutic Nanobody Profiler
מדוע בני‑דודים זעירים של נוגדנים חשובים עבור תרופות עתידיות
רבים מהתרופות המצליחות של היום הם נוגדנים — חלבונים שנקשרים למטרות מחלה בדיוק רב. מחלקה חדשה של קשרנים אף קטנים יותר, הנקראת ננובודים, מסוגלת להחליק לכיסים שקשה להגיע אליהם על פני וירוסים, גידולים מולקולות אחרות. אך היכולת להיקשר למטרה אינה מספיקה: כמועמד לתרופה עליו להיות גם קל לייצור, יציב בבקבוקון ובטוח בגוף. עבודה זו מציגה את ה‑Therapeutic Nanobody Profiler, כלי חישובי שנועד לסייע למדענים לשפוט, בשלבים מוקדמים ומבלעדית על בסיס רצף, אילו ננובודים סביר שיהפכו לתרופות מעשיות.
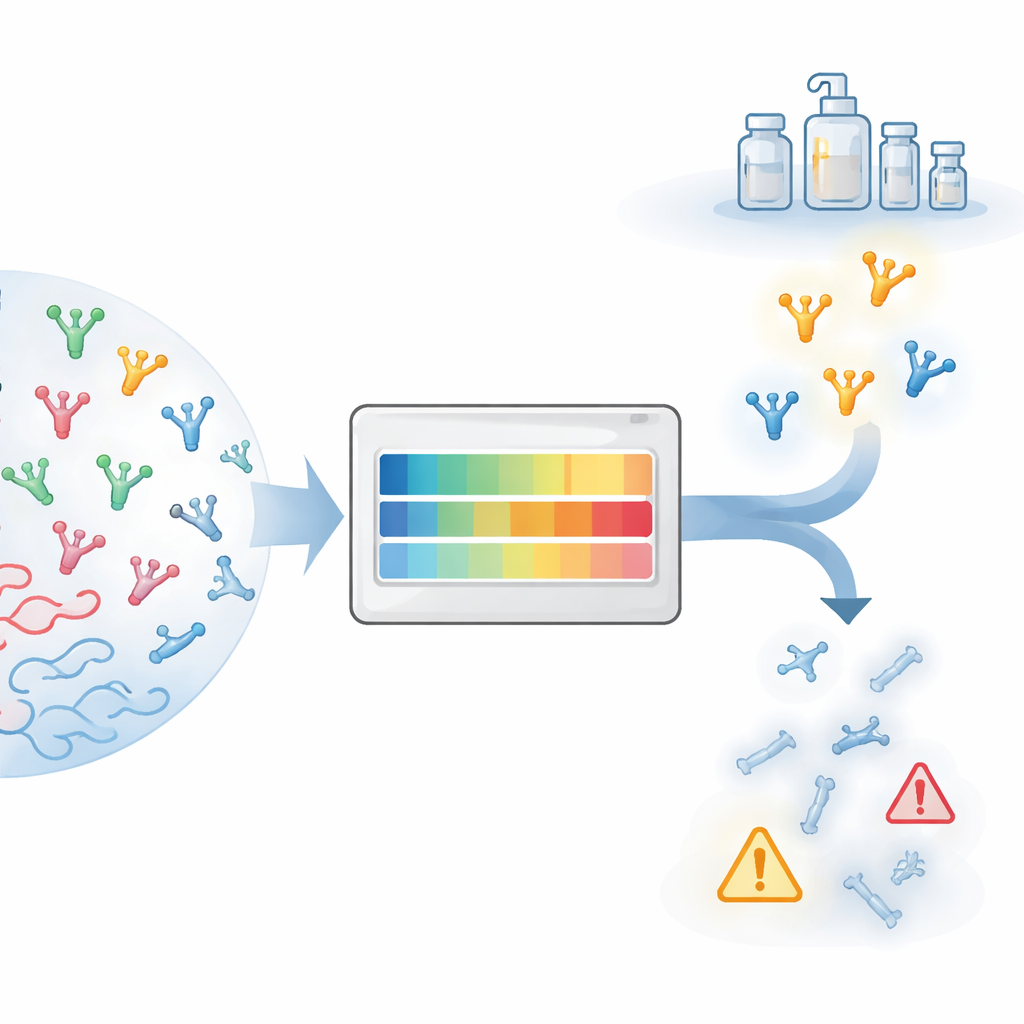
מרעיון מבטיח לתרופה מעשית
הפיכת חלבון לטיפול ממשי כרוכה במכלול מכשולים מעשיים הסוכמים תחת המונח «התכנות לפיתוח». חלבונים חייבים להיות מיוצרים בכמויות גדולות, להישאר מסיסים, להימנע מהתאגדות ולשמור על יציבות במהלך משלוח ואחסון. בעשור האחרון חוקרים למדו כיצד לחזות רבות מתכונות אלה עבור נוגדנים מונוקלונליים בגודל מלא, נתמך בנתונים קליניים רבים ובבדיקות מעבדה מיוחדות. עם זאת, ננובודים שונים מבניים: הם מורכבים מתחום יחיד במקום זוג שרשראות, לרוב בעלי לולאות הקשירה ארוכות יותר ומחשפים אזורים שטחיים שמוטמנים בנוגדנים רגילים. כתוצאה מכך, שיטות המכוונות לנוגדנים רגילים עלולות לתת תשובות מטעות כשמיישמים אותן על ננובודים.
פרופיילר שתוכנן להתאמה למאפייני ננובודים
כדי להתמודד עם חוסר ההתאמה הזה, החוקרים פיתחו את ה‑Therapeutic Nanobody Profiler (TNP), בהשראת כלי קודם לנוגדנים סטנדרטיים אך מהונדס מחדש סביב הביולוגיה של ננובודים. הם אספו רצפי ננובודים ממקורות רבים: ניסויים קליניים, מאגרי חיסון טבעיים, פטנטים, מאמרים מדעיים ומבני גביש ידועים. באמצעות מנבאים מבניים המבוססים על למידה עמוקה המותאמים לאנטי‑גופים בעלי תחום יחיד, הם ייצרו מודלים תלת‑ממדיים לרצפים אלה. מכל מודל מדדו כמה ארוכות לולאות הקשירה, כמה רחוק אחת הלולאות המפתח בולטת מגוף החלבון, ואיך מאורגנות אשכולות שיירים הידרופוביים וטעונים על המשטח — תכונות המשפיעות בחוזקה על מסיסות, התמ aggregates ודבקות לא ספציפית.
שתי סגנונות מבניים, שניהם ישימים
אחת הממצאים הבולטים נוגעת ללולאת הקשירה הראשית, הידועה כ‑CDR3. כאשר הצוות כמדד עד כמה הלולאה "קומפקטית" — בהשוואת אורכה למידת ההארכה שלה מהגוף — הם מצאו חלוקה ברורה לשני סגנונות מבניים. בתת‑סוג אחד הלולאה ארוכה יותר וקופלת חזרה מעל צידו של החלבון, יוצרת הרבה מגעים מייצבים עם קבוצת שיירים מאפיינת. באחרת, הלולאה בולטת החוצה יותר כפי שנראה ברסיס נוגדן קונבנציונלי. ננובודים בשלב קליני מופיעים בשני תתי‑הסוגים, וכאשר החוקרים השוו כמה עשרות מדידות מעבדה מעשיות — כגון התמ aggregates, אסוציאציה עצמית ויציבות תרמית — הם לא מצאו עונש שיטתי לאף אחד מהסגנונות. משמעות הדבר היא שמעצבי תרופות אינם חייבים להעדיף צורת לולאה אחת על פני השנייה, כל עוד שאר התכונות נראות מקובלות.
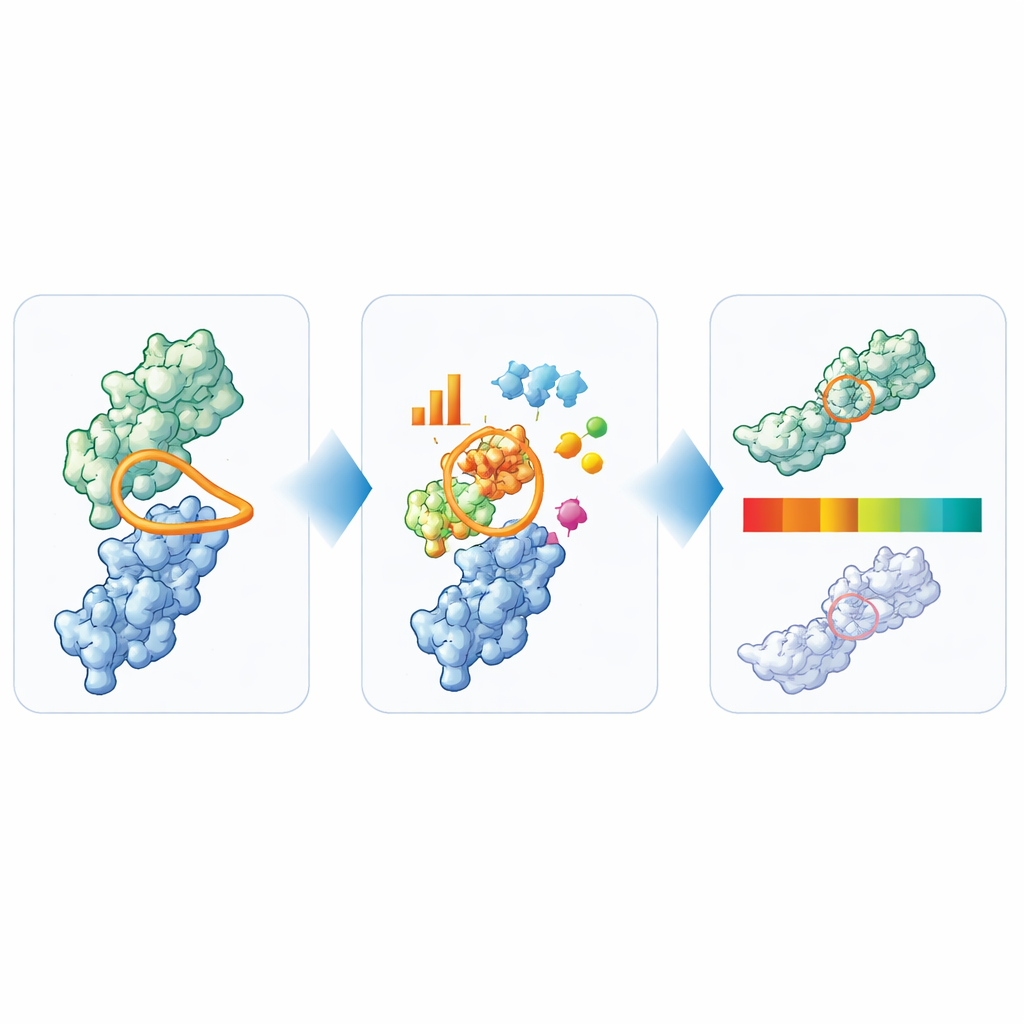
הפיכת מבנה לאורות תנועה פשוטים
מהניתוח הרחב שלהם זיקקו המחברים שש תכונות מרכזיות שתופסות יחד את הדאגות העיקריות להתכנות הפיתוח של ננובודים: אורך כולל של הלולאות, האורך הספציפי והקומפקטיות של CDR3, וגודלם של כתמי משטח הידרופוביים, חיוביים ושליליים סביב אתר הקשירה. לאחר מכן השתמשו ב‑36 הננובודים שהגיעו לניסויים קליניים כדי להגדיר גבולות מעשיים לכל מדד. ערכים באזור המרכזי, הנפוץ, מסומנים כ"ירוק", ערכי קצה כ"חום" והחריגים הברורים כ"אדום". כדי לבדוק עד כמה האיתותים הללו אינפורמטיביים, הם החילו את ה‑TNP על 72 ננובודים קנייניים נוספים והשוו את הדגלים לפאנל נרחב של בדיקות מעבדה. ננובודים שסומנו על‑ידי TNP כחריגים ברורים הראו בדרך כלל גם מספר סימני אזהרה ניסוייתיים, בעוד שאלה שנראו נקיים חישובית התנהגו לעתים קרובות טוב יותר במעבדה.
מה המשמעות עבור טיפולים של העתיד
ללא‑מומחים, המסר המרכזי הוא כי צורתו ותבנית המשטח של ננובוד ניתנות עתה להמרה לפרופיל התכנות לפיתוח פשוט לפני שמתחילים עבודות מעבדה יקרות. ה‑Therapeutic Nanobody Profiler אינו מחליף ניסויים, ועדיין מתרחשות אי‑התאמות בין תחזיות לבדיקה, במיוחד מאחר שבדיקות מעבדה בוצעו על ננובודים המשולבים עם רסיסים גדולים יותר של נוגדנים. אך על‑ידי איתור מהיר של מועמדים בעלי לולאות יוצאות דופן — ארוכות או מקופלות בנוקשות — או כתמי משטח בעייתיים, TNP מסייע לכוון תשומת לב לננובודים שסביר שיהפכו לתרופות אמינות יותר. ככל שיותר ננובודים ייכנסו לניסויים קליניים וירחיבו את קבוצת הייחוס, הכלי צפוי להשתפר ולהאיץ עוד יותר את תכנוןן של תרופות קטנות ודמויות‑נוגדן יציבות למגוון רחב של מחלות.
ציטוט: Gordon, G.L., Gervasio, J., Souders, C. et al. Characterising nanobody developability to improve therapeutic design using the Therapeutic Nanobody Profiler. Commun Biol 9, 344 (2026). https://doi.org/10.1038/s42003-026-09594-y
מילות מפתח: ננובודים, התכנות לפיתוח של תרופות ביולוגיות, פרופיילינג חישובי, הנדסת נוגדנים, יציבות חלבונים