Clear Sky Science · he
פיתוח ליגנדים נגזרים מקפסאיצין לפרוהיביטין לצורך ויסות האינטראקציה בין קינאזת אורורה A/PHB2 ומיטופאגיה בתאי סרטן
למה מולקולה מהצ’ילי חשובה עבור סרטן
החריפות של צ׳ילי נובעת מקפסאיצין, מולקולה קטנה שמוצמדת לחלבונים בתאים שלנו. המחקר הזה חוקר טוויסט מפתיע לעירוי המוכר הזה: החוקרים שיפרו את הקפסאיצין כדי ליצור מולקולות בעלות מאפיינים דמויי-תרופה שפונות אל "תחנות הכוח" של תאי סרטן — המיטוכונדריות — וממתנות תהליך שהן משתמשות בו כדי לשמור על בתי האנרגיה שלהן במצב מיטבי. מכיוון שתאי סרטן מסתמכים במידה רבה על מיטוכונדריות יעילות לצורך גדילה בלתי מבוקרת, היכולת להפריע סלקטיבית למערכת תמיכה זו עשויה לפתוח נתיב חדש לטיפולים אנטי‑סרטניים.
תחנות הכוח של התא וצוות הניקוי הפנימי שלהן
המיטוכונדריות מאזנות באופן מתמיד בין בנייה של יחידות חדשות לבין מיחזור של יחידות פגומות. צד המיחזור, המכונה מיטופאגיה, מתפקד כמו מערכת בקרת איכות: מיטוכונדריות בלויות מסומנות ומתפרקות, בעוד שהבריאות יותר נשמרות. תאים סרטניים רבים חוטפים את האיזון הזה, ומשתמשים במיטופאגיה כדי לסלק מיטוכונדריות חלשות ולהעשיר ב"ביצועיות-על" שמפיקות כמויות גדולות של ATP, מטבע האנרגיה של התא. חלבון בשם קינאזת אורורה A (AURKA), שמופק לעתים יתר ברקמות סרטניות, נמצא לאחרונה בתוך מיטוכונדריות שם הוא משתף פעולה עם חלבון נוסף, פרוהיביטין‑2 (PHB2), והמתאם האוטופגי LC3. יחד הם יוצרים קומפלקס שמעודד מיטופאגיה ותומך בפלט אנרגיה גבוה בתאי סרטן.
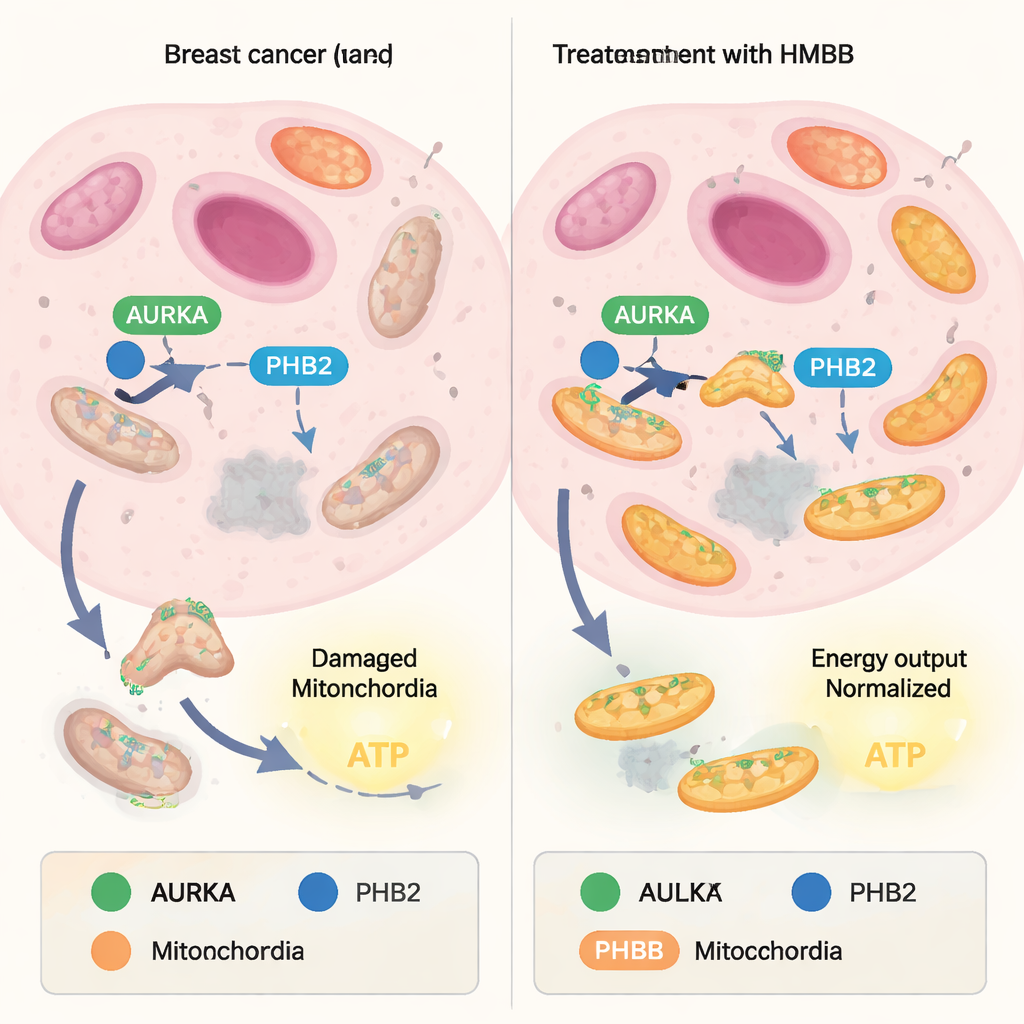
מקפסאיצין חריף לכלים מולקולריים ממוספרים
עבודות קודמות הראו כי תרכובת טבעית בשם זנת'ומונול (xanthohumol) יכולה להיצמד ל‑PHB2 ולהפריע לקומפלקס AURKA–PHB2–LC3, לחסום מיטופאגיה ולהפחית את ייצור ה‑ATP המיטוכונדריאלי. עם זאת, המבנה הכימי של זנת'ומונול אינו אידיאלי לפיתוח תרופתי. במחקר הנוכחי פנו המחברים אל הקפסאיצין, ליגנד טבעי נוסף של PHB, ובדקו האם ניתן לעצב אותו מחדש לכלים פרקטיים יותר. הם אישרו תחילה כי קפסאיצין מחליש במידה מסוימת את האינטראקציה בין AURKA ל‑PHB2 בתאי סרטן של השד בחיות חיים, באמצעות טכניקת הדמיה (FRET/FLIM) שמודדת כמה קרובים שני חלבונים מתויגים זה לזה. לאחר מכן הם סינתזו 16 מולקולות בהשראת קפסאיצין על ידי שינוי ה"זנב" וה"ראש" הארומטי של המבנה המקורי ובדקו שיטתית כיצד כל וריאנט משפיע על השותפות בין AURKA ל‑PHB2 בתוך המיטוכונדריה.
גילוי "דבק" מולקולרי שמנע נעילת חלבונים זה לזה
המולקולות שעוצבו השפיעו בצורה בולטת ושונה. חלקן, כמו הקפסאיצין עצמו או נגזרת בשם תרכובת 5, גרמו לכך ש‑AURKA ו‑PHB2 נפרדו ביתר קלות. אחרות כמעט שלא השפיעו. תת‑קבוצה, במיוחד מולקולה בשם תרכובת 13, שבאה לימים להיקרא HMBB, הפכה את המצב והדוקת משמעותית את הקשר בין AURKA ל‑PHB2. סימולציות דוקינג ממוחשבות סייעו להסביר התנהגות זו. קפסאיצין ותרכובת 5 נטו להסתדר באתר הפעיל של AURKA באופן שיצר התנגשות פיזית עם PHB2, ולדחוף את שני החלבונים זה מזה. לעומת זאת, תרכובות 12 ו‑13 התמקמו באתר הפעיל של AURKA ונגעו במקביל בכיס מעכב מוכר על PHB2 מבלי ליצור התנגשות. במקום זאת, צורותיהן איפשרו להן לפעול כ"דבק מולקולרי", לגשר בין AURKA ל‑PHB2 ולייצב את הקומפלקס.
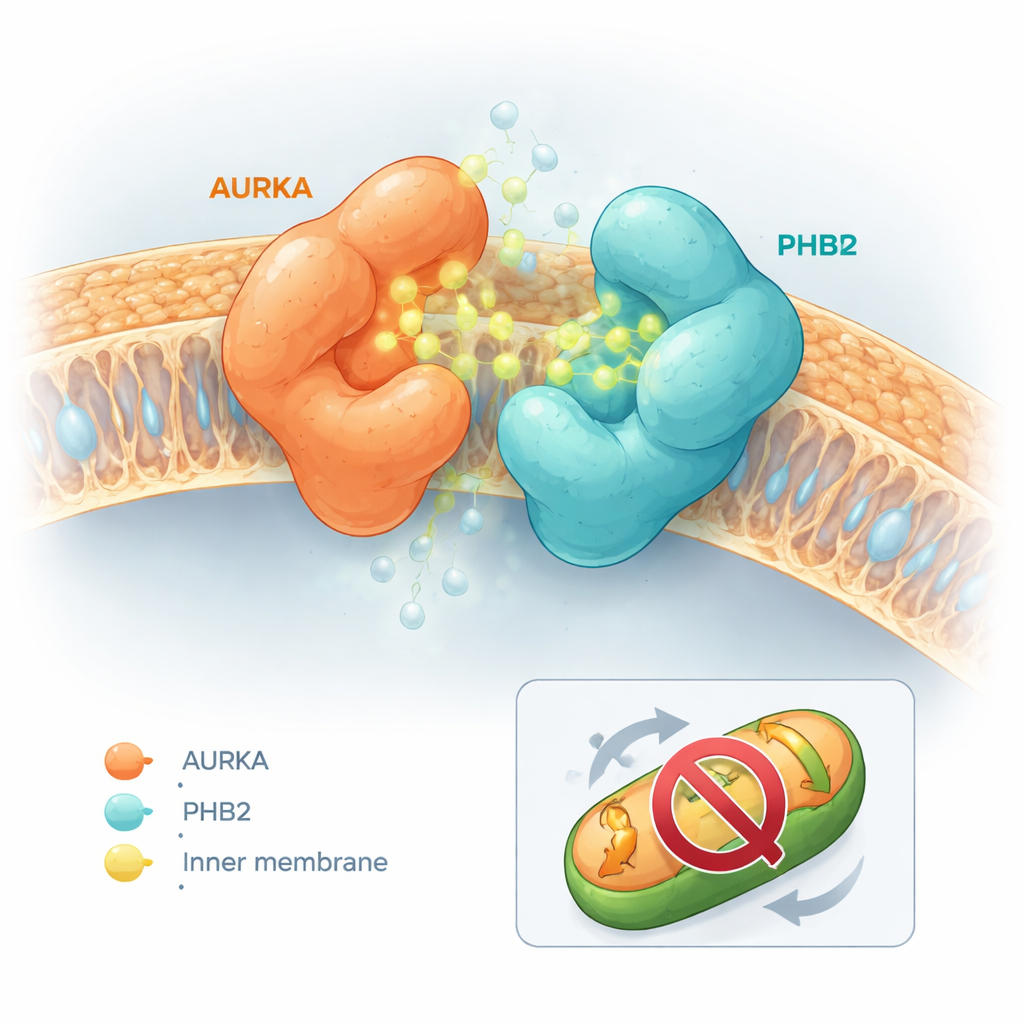
חסימת הניקוי המיטוכונדריאלי בלי לכבות את מרכז הבקרה של התא
שאלה מכרעת הייתה האם התנהגות ה"דבק המולקולרי" הזאת משתקת פשוט את AURKA בכל תא באופן שעלול לגרום לתופעות לוואי נרחבות, או שמא פועלת בצורה סלקטיבית יותר. באמצעות ביו‑סנסור פלואורסצנטי נפרד שמדווח על הפעלת AURKA במרכזי הסנטרוזום — המבנים שמארגנים את מכונת החלוקה של התא — הצוות צפה ש‑HMBB לא דיכא את פעילות AURKA באתרים האלה. ואולם בבדיקות מיטוכונדריאליות, HMBB הביא להיפוך של אובדן מסת המיטוכונדריה שנגרמת בדרך כלל מהבעת יתר של AURKA בתאי סרטן של השד. בתאים שמייצרים באופן טבעי רמות גבוהות של AURKA, HMBB הגדיל את תכולת המיטוכונדריה, מה שמצביע על כך שמיטופאגיה מונעת הנגרמת על‑ידי AURKA נחסמה. בתאים עם רמות נמוכות של AURKA ל‑HMBB היה השפעה מועטה, דבר המדגיש את התלות שלו במסלול AURKA–PHB2.
מה משמעות הדבר עבור טיפולים סרטניים עתידיים
סיכום הממצאים מראה כי נגזרות קפסאיצין שעוצבו בקפידה יכולות לכוונן את האינטראקציה בין AURKA ל‑PHB2 בתוך המיטוכונדריה. על ידי פעולה כ"דבק מולקולרי", HMBB ותרכובות קשורות מנעילות את AURKA ו‑PHB2 בקונפיגורציה שמונעת את התכנית הרגילה של מיטופאגיה, מבלי לכבות את התפקידים החיוניים של AURKA באזורים אחרים בתא. עבור הקורא הכללי, הרעיון המרכזי הוא שהמחברים יצרו מולקולות פרוטוטיפיות שמתערבות באופן סלקטיבי בדרך שבה תאי סרטן שומרים על תחנות הכוח שלהם, וייתכן שהן מחלישות את אספקת האנרגיה שלהם תוך שמירה על תפקודים נורמליים בתאים. אמנם התרכובות הללו נמצאות עדיין בשלב מעבדה ראשוני, אך הן מדגימות אסטרטגיה מבטיחה: שימוש במולקולות קטנות ודמויי‑תרופה כדי למקד שותפויות חלבוניות ספציפיות בתוך מיטוכונדריה ובכך לערער את היתרונות המטבוליים שעליהם רבים מהגידולים נשענים.
ציטוט: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
מילות מפתח: מיטוכונדריה, מיטופאגיה, קינאזת אורורה A, נגזרות קפסאיצין, מטבוליזם של סרטן