Clear Sky Science · he
הערכת מחדש של הספציפיות בין חלבוני Gα לקטעי תגובה בסיגנaling של GPCR
מדוע מתגי התא הקטנים חשובים לרפואה
רבות מהתרופות של היום פועלות על ידי הפעלת "מתגים" מולקולריים על פני התא שלנו הנקראים קולטן‑חלבון‑G‑נגזר (GPCR). מתגים אלה מעבירים הודעות לתוך התא באמצעות חלבוני עזר הנקראים חלבוני G ולבסוף מפעילים או מכבים גנים. במשך עשורים חוקרים הסתמכו על מבחנים פשוטים שמפיקים אור כדי לזהות אילו חלבוני G משתמשים בהם תרופה או קולטן נתון. המחקר הזה שואל שאלה בסיסית אך קריטית: האם המבחנים האלה באמת מודיעים לנו את מה שאנחנו חושבים—והאם ניתן עדיין לסמוך עליהם בעת תכנון הדור הבא של תרופות מדויקות?
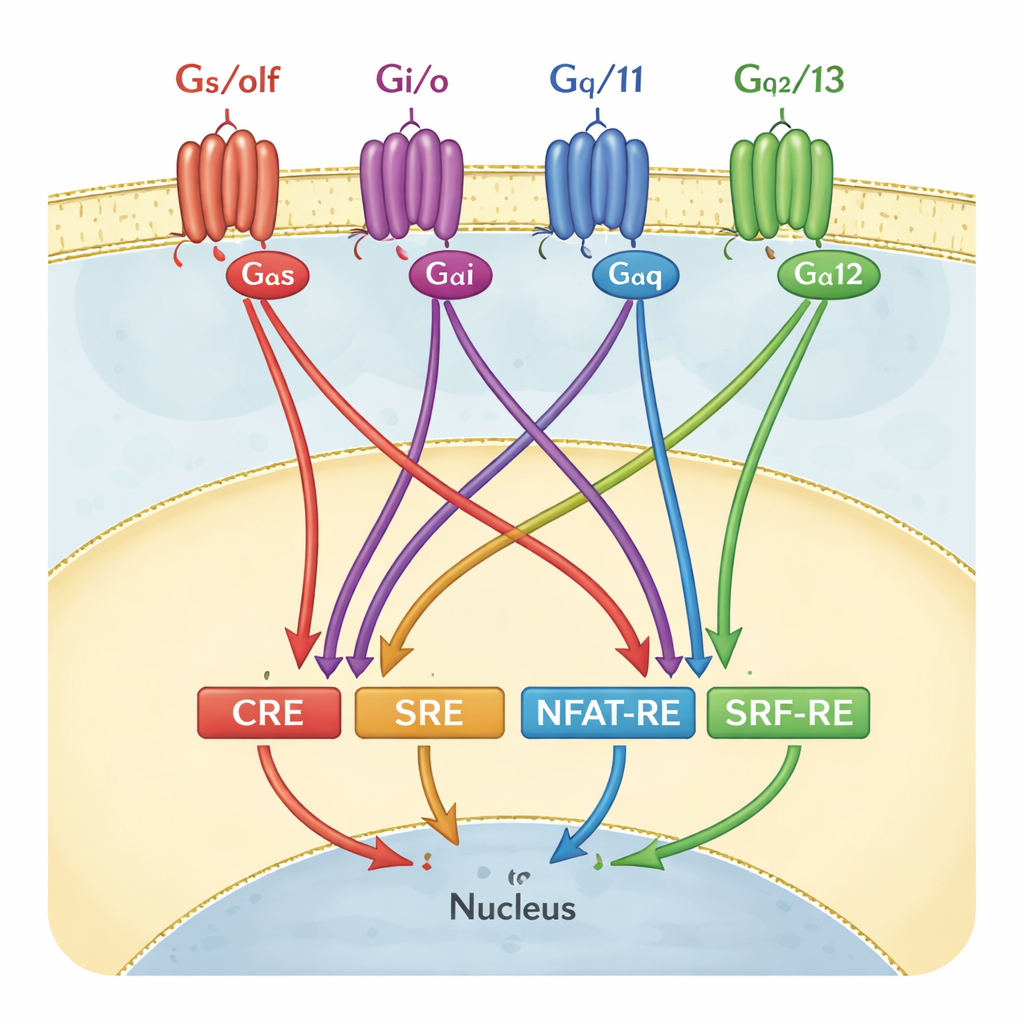
כיצד מדענים קוראים בדרך‑כלל את אותות ה‑GPCR
כדי לעקוב אחרי פעילות GPCR, מעבדות רבות משתמשות בבדיקות גן‑דיווח. במבחנים אלה מהנדסים תאים כך שכאשר מתג גן מסוים, או "קטע תגובה", מופעל, התאים זוהרים. ארבעה קטעי תגובה כאלה פופולריים במיוחד: CRE, SRE, NFAT‑RE ו‑SRF‑RE. כל אחד מהם נתפס מזה זמן רב כתחליף לענף מסוים של איתות חלבוני G—למשל CRE עבור משפחת Gαs/olf, או SRF‑RE עבור Gα12/13. בספרי לימוד ובתהליכי סינון, הזיווגים האלה לעתים מוצגים כמעט כמו דיאגרמות חיווט חד‑לחיצתיות: מפעילים חלבון G ספציפי ורק מדווח אחד נדלק.
לבחון את דיאגרמת החיווט הישנה
המחברים אתגרו שיטה זו באופן שיטתי תוך שימוש בתאי HEK293 אנושיים שבהם הוסרו משפחות חלבוני G ספציפיות—או אפילו כל חלבוני G—באמצעות עריכה גנומית. לאחר מכן הם החזירו סוגי חלבוני G בודדים אחד‑אחד. לתאים אלה הם הביעו תשעה GPCRs שונים, שנבחרו כדי לייצג קולטנים שמסמנים בררנות גבוהה או דרך שותפים רבים של חלבוני G. על‑ידי מדידת עוצמת הזוהר של כל אחד מארבעת המדווחים על פני ריכוזי תרופות רבים, הם יכלו לראות אילו חלבוני G נדרשים באמת לכל קטע תגובה, ואילו עלולים לסייע בעקיפין.
מסלולים חופפים במקום תעלות נפרדות
התוצאות מפילות את מודל "קולטן‑אחד‑מדווח‑אחד" המסודר. בעוד ש‑CRE עדיין התבסס בעיקר על חלבוני Gαs/olf—הדרך הקלאסית שמעלה cAMP—משפחות חלבוני G אחרות יכלו להשפיע במידה ניכרת על פעילות CRE, אך רק כאשר Gαs/olf היה נוכח. עבור שלושת המדווחים האחרים, SRE, NFAT‑RE ו‑SRF‑RE, משפחת Gαq/11 התגלתה כנושאת העומס העיקרית, אף על פי ש‑SRE ו‑SRF‑RE היו מסורתית מקושרות לענפים אחרים של חלבוני G. SRE ו‑SRF‑RE התנהגו בדמיון מיוחד, מה שמרמז שהן נזקקות למכונות משותפות במורד הזרם במקום לדרכים מבודדות נפרדות. במקרים רבים חלבוני G נוספים כגון Gα12/13 ו‑Gαi/o סיפקו דחיפה נוספת או פעילות רקע, מה שהבליט רשת של חפיפה (crosstalk) ולא תעלות נפרדות.
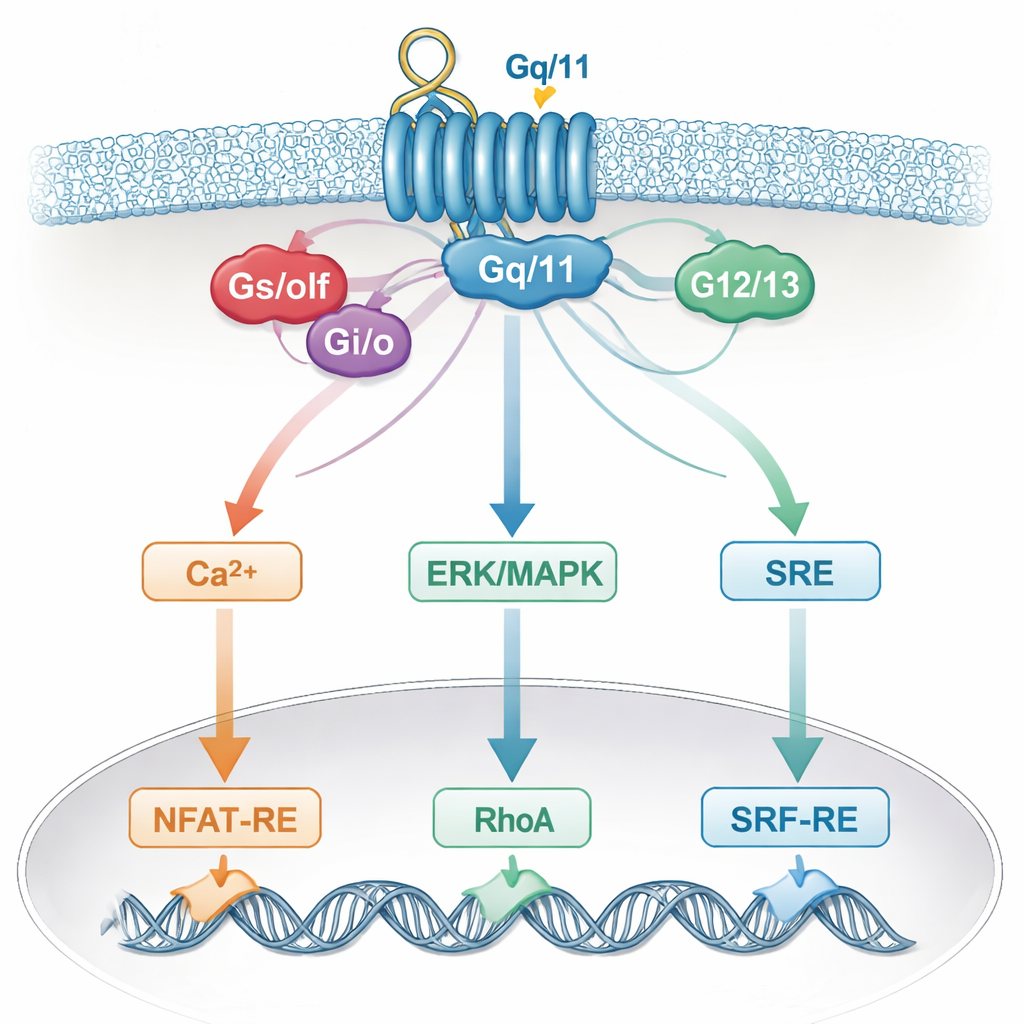
מדוע רשת התא מטשטשת את קריאותינו
חוסר הספציפיות המטושטש הזה משקף ככל הנראה כיצד תאים אמיתיים מאחדים אותות. קולטן יחיד יכול להפעיל מספר חלבוני G, אשר מתנקזים לאחר מכן על מוליכים משותפים כגון סידן, ERK/MAPK, RhoA או cAMP, ועל עוזרים משותפים כמו תתי‑יחידות Gβγ. המסלולים המשותפים הללו, בתורם, זורמים אל אותם מתגים גנטיים בגרעין. כתוצאה מכך מדווח שנחשב כמשתמש במשפחת חלבוני G אחת למעשה "שומע" כמה משפחות. גורמים תלויי‑סוג‑תא והסט המדוייק של קולטןים נוכחים מוסיפים עוד מורכבות, מה שאומר כי מסקנות העולות ממערכת תאים אחת עשויות שלא לחול במערכת אחרת.
מה המשמעות לזה בעריכת תרופות
עבור מי שאינו מומחה, המסקנה המרכזית היא שרבות מהבדיקות מבוססות‑זוהר של GPCR שהן בשימוש נרחב פחות ספציפיות ממה שמצוין על התווית שלהן. הן עדיין יכולות ליידע אותנו שקולטן פעיל ובאופן גס אילו מסלולים רחבים מעורבים, אך אינן הוכחה אמינה לכך שמשפחת חלבוני G מסוימת—ורק היא—מעורבת. המחברים טוענים שחוקרים ומפתחי תרופות צריכים להתייחס למדווחים אלה כאינדיקטורים גסים ולצד זאת לשלב שיטות ישירות יותר הצופות באינטראקציות חלבוניות בזמן אמת. כך יתקבל תמונה מדויקת יותר של האופן שבו תרופות פוטנציאליות מנווטות את האיתות התאי, ויסייע להימנע מקיצורי דרך מטעות בחיפוש אחר טיפולים בטוחים וממוקדים יותר.
ציטוט: Saito, A., Kise, R., Yamaguchi, S. et al. Re-evaluating Gα protein–response element specificity in GPCR signaling. Commun Biol 9, 288 (2026). https://doi.org/10.1038/s42003-026-09569-z
מילות מפתח: סיגנaling של GPCR, חלבוני G, בדיקות דיווח, רשתות איתות תאיות, גילוי תרופות