Clear Sky Science · he
בדיקות מבוססות תאים ובחירת איזופור ספציפית של קינאזות G לחלבון־מקושרות (GRK) להערכת מעכבים מקיפה
מדוע חשוב לכבות את "כפתורי העוצמה" התאית
תרופות רבות שלנו פועלות על ידי העלאה או הורדה של פעילות קולטני־משטח תאים החשים הורמונים, מוליכים עצביים ותרופות. קולטנים אלה צריכים להיות כבויים מחדש באופן מבוקר כדי שהתאים לא יישארו מופרזים בפעילותם; תהליך זה נשלט חלקית על ידי אנזימים הנקראים GRK. כאשר פעילות ה‑GRK מוגברת מדי, כפי שנצפה בכשל לבבי ובחלק מהסרטן, האיתות מתפרש לא נכון. במחקר זה פותחו בדיקות מעשיות המבוססות על תאים שמודדות כמה טוב מולקולות ניסיוניות חוסמות איזופורים ספציפיים של GRK, ועוזרות לחוקרים לעצב תרופות חכמות יותר שמכווננות את אותם כפתורי עוצמה תאיים קריטיים.
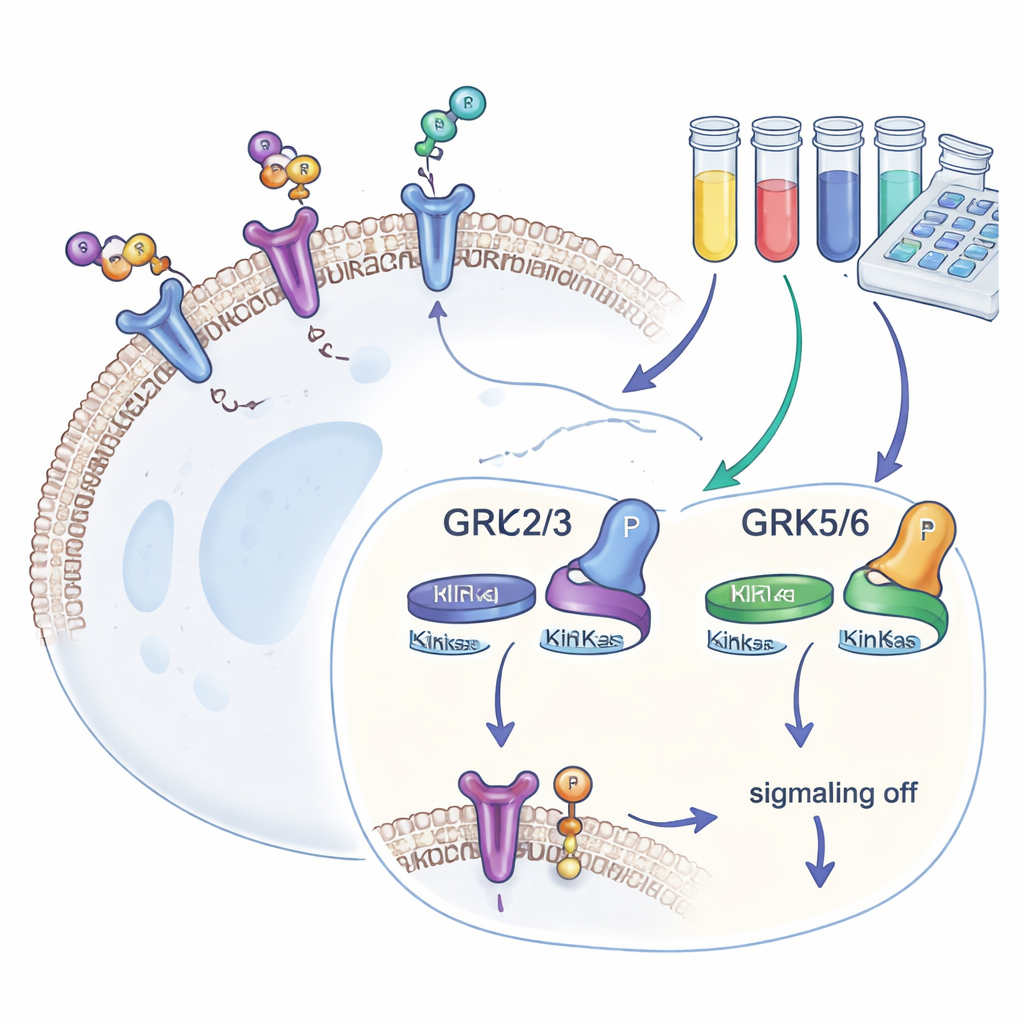
שומרי־שער על פני משטח התא
בתאים שלנו קיימים מאות סוגים של קולטן‑חלבון G (GPCR), אשר מזהים אותות חיצוניים ומתרגמים אותם לתגובות פנימיות. לאחר שה‑GPCR הופעל, אנזימי GRK מצמידים דגלוני־זרחן זעירים לזנבו. דגלונים אלה מושכים חלבון נוסף, בטא‑ארסטין, שמפסיק המשך איתות ולעתים מושך את הקולטן פנימה לתוך התא. ארבעת האיזופורים — GRK2, GRK3, GRK5 ו‑GRK6 — מצויים ברקמות רבות. מאחר שהם מעצבים עד כמה הקולטנים מגיבים, ומכיוון שרמותיהם משתנות במחלות כמו כשל לבבי, סרטן והתמכרות, מפתחים תרופות מעוניינים למצוא מעכבים של GRK שיהיו גם רבי‑עוצמה וגם סלקטיביים.
בניית קרקע בדיקה נקייה בתוך תאים
מרבית המחקרים הקודמים על GRK הסתמכו על דוגמנות ממוחשבת או כימיה במבחנה, שמחשיפה כמה חזק מעכב יכול להתחבר אך לא כיצד הוא מתפקד בסביבה הצפופה של תא חי. כדי לגשר על הפער הזה, החוקרים הנדסו תאי HEK293 אנושיים שמחוסרים מכל ארבעת ה‑GRK הנפוצים ולאחר מכן החזירו כל פעם איזופור GRK יחיד. לכל שורת תאים צורף גם קולטן ידוע היטב — הקולטן הבטא‑2 אדרנרגי — שסומן כך שניתן יהיה לקרוא את זירוח הפוספט במיקום זנב ספציפי (המכונה T360/S364) באמצעות בדיקת אנטי‑גוף רגישה. מאחר שמיקום זה מותאם רק על ידי GRK, כמות הזרחן שם משמשת מדד ישיר וכמותי לפעילות כל איזופור GRK בתאים חיים.
מיון הטובים, החלשים והלא‑ספציפיים
באמצעות ערכת הכלים הזו הקבוצה בחנה פאנל של מעכבים מסחריים ל‑GRK. תחילה קיבצו תרכובות המכוונות בעיקר ל‑GRK2 ו‑GRK3, וקבוצה אחרת המכוונת ל‑GRK5 ו‑GRK6. על‑ידי השוואת מידת הירידה בזירחון הקולטן בתאים שמביעים איזופור GRK יחיד, הם יכלו למפות סלקטיביות בעולמם הממשי. תרכובת אחת, שכונתה 8h, התגלתה כמעכבת החזקה ביותר של GRK2/3, בעוד שתרכובת 18 בלטה כבעלת סלקטיביות ל‑GRK5/6. כמה מולקולות נפוצות הראו אפקט מועט במינונים שנבדקו, ככל הנראה כי לא חדרו היטב לתאים, ומעכב קוולנטי חזק במיוחד פגע בבריאות התאים, מה שהפך אותו ללא מתאים לניסויי הדמיה.
מטביעים כימיים להתנהגות הקולטנים
כדי להראות שהמעכבים משפיעים לא רק על קולטן ניסוי יחיד אלא על ביולוגיית GPCR באופן רחב יותר, החוקרים בחנו מספר קולטנים חשובים רפואית, כולל קולטן המי‑אופיאט וקולטן הווזופרסין V2. הם מדדו גם זירחון וגם אינטרנליזציה של קולטנים בעזרת מיקרוסקופיה. תרכובת 8h או 18 לבדן צמצמו חלקית את הזירחון והתנועה הפנימית של קולטנים עבור יעדים רבים, אך השילוב של 8h ו‑18 מנע כמעט לחלוטין שינויי אלה והשאיר את הקולטנים על פני משטח התא. ניסויים נוספים שעקבו אחרי גיוס בטא‑ארסטין אישרו שאותן תרכובות יכולות לכוונן איתות גם בקולטנים אחרים הנשלטים על‑ידי מערכי GRK חופפים.
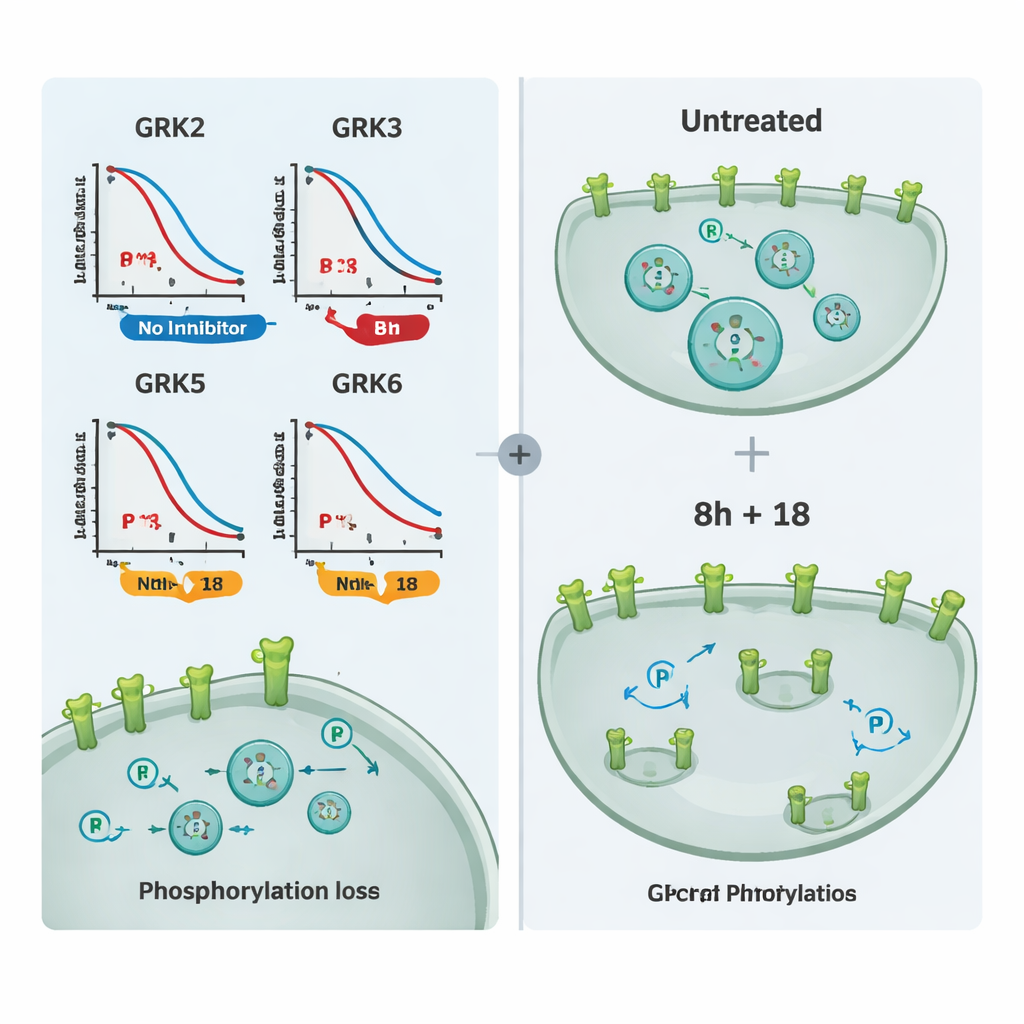
מה משמעות הדבר עבור תרופות עתידיות
ללא־מומחים, המסר המרכזי הוא שהמחקר מספק ערכת בדיקות אמינה מבוססת תאים — ושתי תרכובות‑כלי שימושיות במיוחד, 8h ו‑18 — שמאפשרות לחוקרים לראות, בתאים חיים, בדיוק כיצד מכוונים איזופורים שונים של GRK. במקום להסתמך על ניחושים מתוך נתוני מבחנה מפושטת, מדענים יכולים כעת להשוות מעכבים מועמדים זה לצד זה ולקבוע האם הם משפיעים בעיקר על GRK2/3, על GRK5/6, או על ארבעתם יחד. בהירות זו עשויה להאיץ פיתוח תרופות שמווסתות באופן מדויק יותר את איתות ה‑GPCR, עם פוטנציאל לתועלת בטיפול במחלת לב, סרטן, מצבי כאב ומצבים נוספים שבהם מאזן האיתות הופר.
ציטוט: Blum, N.K., Kiefer, M.C., Decker, A. et al. Cell-based and isoform-selective G protein-coupled receptor kinase assays for comprehensive inhibitor evaluation. Commun Biol 9, 287 (2026). https://doi.org/10.1038/s42003-026-09568-0
מילות מפתח: איתות GPCR, מעכבי GRK, קולטן בטא־אדרנרגי, בדיקת מבוססת תאים, גילוי תרופות