Clear Sky Science · he
טיפול דינאמי מוּנָע רדיונוקלידים מעורר מסלולי מוות תאיים משלים: נקרופטוזיס אימונוגני ואפופטוזיס בסרטן
להפנות את טריקי הסרטן נגדו
הסרטן ידוע ביכולתו להתחמק מהטיפולים הטובים ביותר שלנו, במיוחד בגידולים תוקפניים של השד שמתפשטים ברחבי הגוף. המחקר הזה בוחן גישה חדשנית הנקראת טיפול דינאמי מוּנָע רדיונוקלידים (RaST), שמשתמש במולכי איתור רפואיים ובננומרס עם תגובת-אור כדי להרוג תאים סרטניים באופן שמעיר גם את המערכת החיסונית. לקוראים זה חשוב כי העבודה מציעה כיצד כלים קיימים לדימות וחומרים חכמים עשויים להיות ממוחזרים ליצירת שליטה ממושכת יותר בסרטן מונעת-חיסון, ולא רק התכווצות זמנית של הגידול.
דרך חדשה להאיר את הגידול מבפנים
טיפולים מבוססי אור מסורתיים פועלים רק במקום שבו קרן חיצונית יכולה להגיע, כמו בעור או בגידולים שטחיים. RaST מתגבר על מגבלה זו בעזרת סוכר רדיואקטיבי, דומה למוליך שמשמש כבר בסריקות PET, שצובר באופן טבעי בתאים סרטניים שנמצאים בצמיחה מהירה. כאשר המוליך הזה נע דרך הגידול, הוא פולט זוהר כחול קל המוכר כרדיואורנס של צרנkov. החוקרים עיצבו ננומולקולות זעירות של תחמוצת טיטניום מצופות חלבון שמטרתו לכוון אל הגידול, כך שגם הן מתמקמות באתר הסרטני. כשהמוליך והרכיבים הננומטריים נפגשים, האור הפנימי מדליק את החלקיקים, שמייצרים בעקבות כך פרצי מולקולות חמצן פעיל—מולקולות תגובתיות שפוגעות בתאים הסרטניים מבפנים.
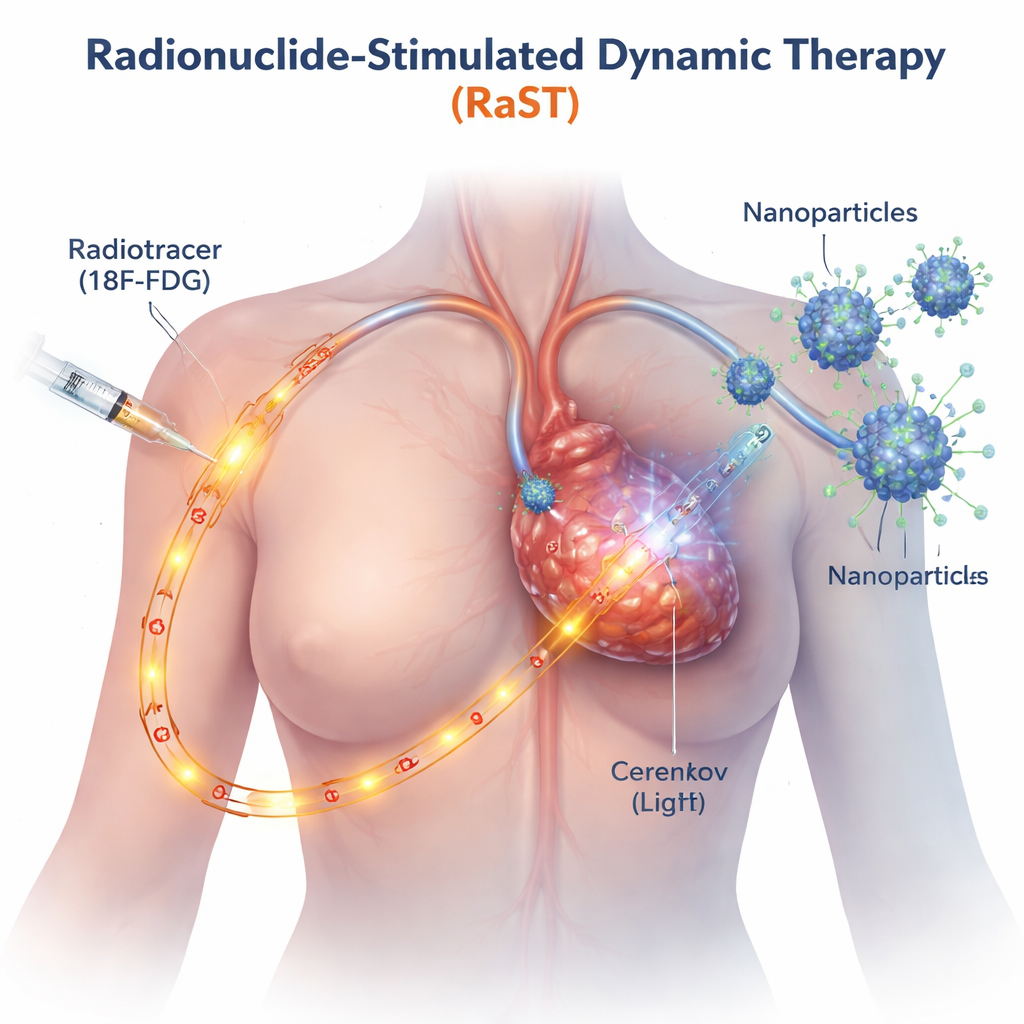
הפעלת שני מסלולי מוות תאיים מובחנים
הצוות רצה לדעת לא רק האם RaST הורג תאים סרטניים, אלא איך. בעבודה עם מספר שורות תאים תוקפניות של סרטן השד במעבדה הם גילו כי מנות מכווננות בקפידה של המוליך הרדיואקטיבי והננומולקולות פועלות יחד כדי לפגוע בתאי הגידול ביעילות רבה יותר מכל אחד מהרכיבים בנפרד, אפילו בסוגים שנוטים להתנגד לכימותרפיה סטנדרטית. הדמיה מדוקדקת ומדידות חלבון חשפו כי RaST הפעיל בו־זמנית שני תוכניות מוות תאיות מוסדרות. אחת מהן הייתה אפופטוזיס, המתוארת לעתים כ'התאבדות' תאית, שבה התאים פורקים את עצמם בסדר מבוקר. השנייה הייתה נקרופטוזיס, צורת מוות תאית יותר פיצוצית שבה התאים מתנפחים, נסדקים ומפזרים אותות מצוקה מולקולריים לסביבה. אותות אלה, הידועים כמולקולות קשורות לנזק וציטוקינים דלקתיים, יכולים לשמש כמוקשים שמושכים ומפעילים תאים חיסוניים.
גיוס המערכת החיסונית לשליטה מתמשכת
כדי לבדוק האם סגנון ההרג הדלקתי הזה חשוב באורגניזמים חיים, החוקרים ניסו את RaST במודלים עכבריים של סרטן השד. בעכברים שחסרו הגנה חיסונית מרכזית, RaST לא עשה הרבה לעצור את גדילת הגידול או את התפשטותו לריאות, למרות שהוא יצר הרבה מוות תאי מקומי. אבל בעכברים עם מערכת חיסונית שלמה, הטיפול הזה הניב תגובות חלקיות ומלאות של הגידול ומנע גרורות לריאות. הגידולים שנחשפו ל-RaST התמלאו בתאים חיסוניים—במיוחד תאים מיואידיים כמו מאקרופאגים ותאי דנדריט—שמיומנים בספיגת חומר מת ומשחקים תפקיד בהצגת פיסות גידול לתאי T. בדיקות דם הראו גליים של אותות מעוררי-חיסון ומווסתי-חיסון במשך הזמן, מה שמרמז כי RaST קודם כל מדליק התקפה על הסרטן ולאחר מכן עובר למצב מאוזן יותר ככל שהגידולים מתכווצים או מתייצבים.
ציד שרידים נסתרים והגנה מפני החמרה חוזרת
אפילו בעכברים שבהם הגידולים נראו מרפאים לחלוטין על-ידי RaST, צבע דימות רגיש מאוד גילָה מאוחר יותר כיסים זעירים של תאים סרטניים ששרדו ושהתחבאו בתוך קשרי לימפה. באופן מרשים, בעלי החיים הללו עדיין לא פיתחו גידולים חדשים או גרורות מרוחקות במשך חודשים רבים. אנליזות כימיות הראו כי ננומולקולות תחמוצת הטיטניום, שהיו בשפע בתחילה בעצמות ובכבד, הוסתו בהדרגה אל הטחול ואל קשרי הלימפה—בדיוק הצמתים שבהם מסתובבים תאי החיסון. הגירה איטית זו כנראה שומרת מקור מקומי ליצירת חמצן תגובתי שמגיע לידם של תאים חיסוניים, ועוזרת להם לזהות ולשלוט בשרידי סרטן נסתרים לפני שהם מסוגלים לשגשג או להתפשט.
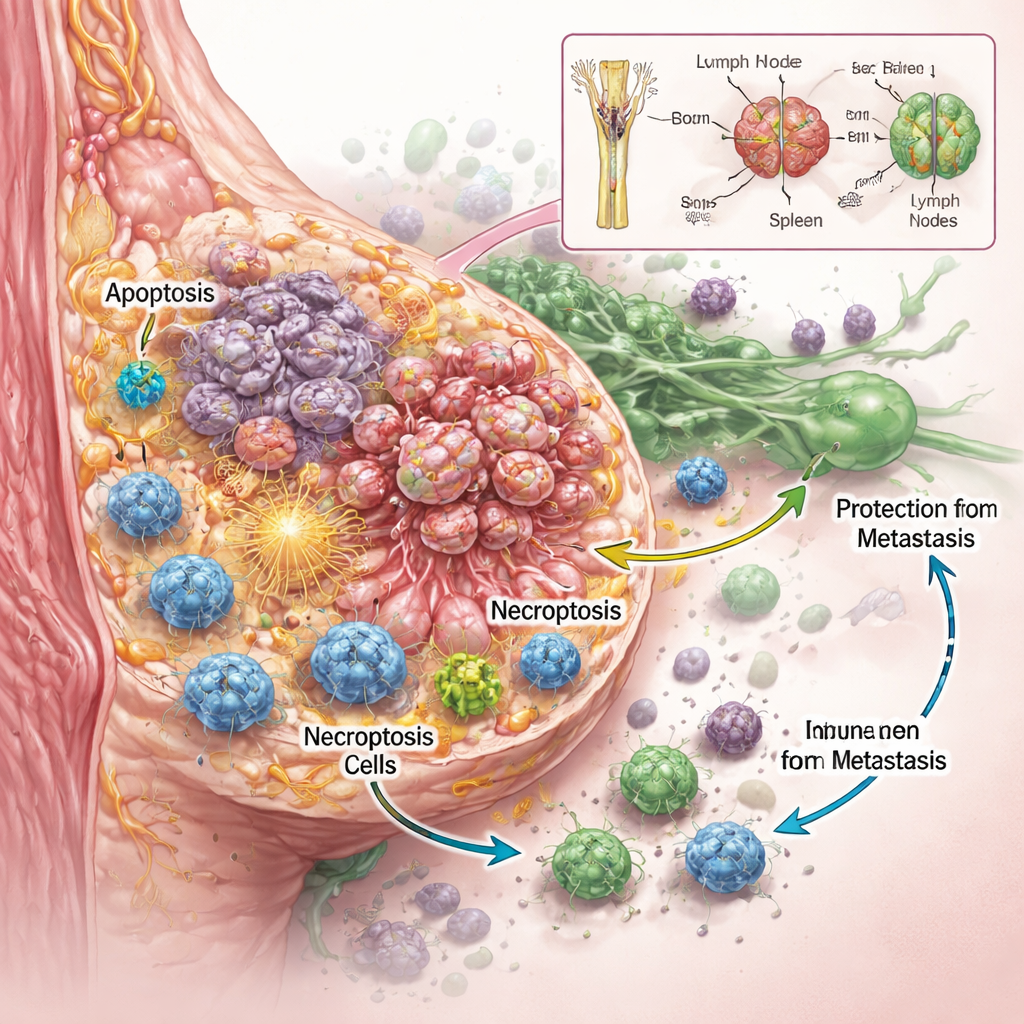
מה זה יכול להשפיע על טיפול בעתיד
במלים פשוטות, עבודה זו מראה ש-RaST הוא יותר מאשר דרך נוספת להרוג תאי גידול. בשילוב מוליכים רדיואקטיביים, ננומולקולות רגישות לאור והגנות הגוף עצמם, הוא דוחף תאים סרטניים לשתי צורות של מוות מתוכנן שמושכות בחוזקה את המערכת החיסונית. בחיות עם מערכת חיסונית שלמה זה מוביל לשליטה ממושכת על גידולים תוקפניים של השד וחוסם גרורות, אפילו כשהכמה תאים סרטניים נשארים בקשרי הלימפה. למרות שעדיין יש הרבה עבודה לפני שניתן לבדוק גישה זו באופן נרחב בבני אדם, המחקר מצביע על טיפולים עתידיים שלא יסתמכו רק על כיווץ גידולים, אלא ישנו את הקשר בין סרטן, מוות תאי וחיסון—כך שהגוף עצמו יוכל לעזור לשמור על המחלה תחת שליטה לאורך זמן רב יותר.
ציטוט: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
מילות מפתח: סרטן השד, ננומולקולות, חיסון-טיפולי, טיפול רדיונוקלידי, נקרופטוזיס