Clear Sky Science · he
גליקופאגיה היא מסלול בילטריאני עתיק התומך בהתאמה מטבולית דרך האבולוציה המבנית של STBD1
איך האויסטרים חושפים טריקים חבויים של אנרגיה
בעלי החיים שורדים זמנים קשים על ידי ניצול דלק מאוחסן, אבל הם לא כולם נשענים על אותו סוג "סוללה". המחקר הזה בוחן את האויסטר הפסיפי ומראה שבמקום להסתמך על שומן כפי שעושים רבים מבעלי החיים האחרים, האויסטרים נשענים במידה רבה על סוכר מאוחסן בצורת גליקוגן. העבודה חושפת נתיב מיחזור תאי פחות מוכר — שנקרא גליקופאגיה — שמאפשר לאויסטרים לרוקן ולמלא במהירות את מאגרי הסוכר שלהם, ומציירת את התפתחות המערכת הזו ברחבי ממלכת החי.
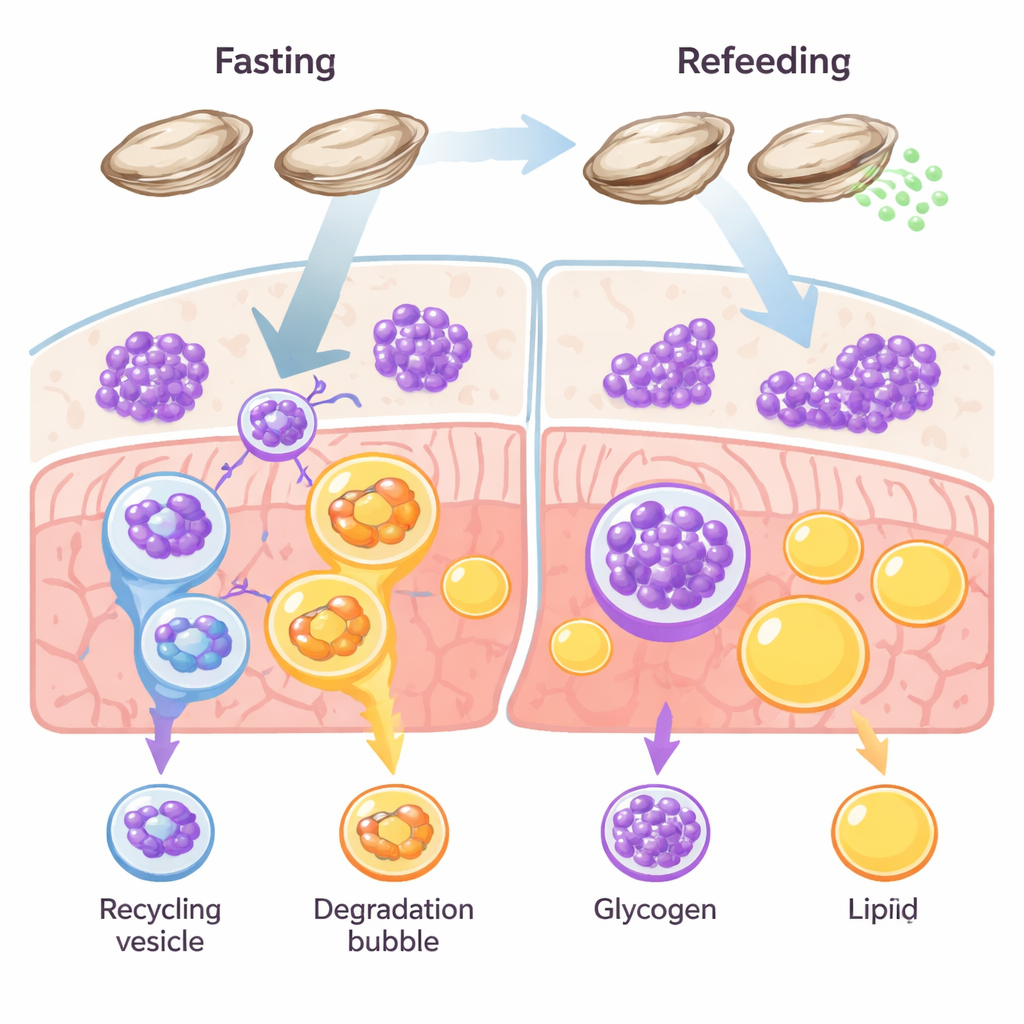
אסטרטגיית הישרדות שמעמד הסוכר ראשונה
רוב בעלי החיים מנהלים מספר מאגרים של אנרגיה, בעיקר שומן וגליקוגן. ביו-חוליות כגון דגים ואוכלי יונקים, השומן בדרך כלל שולט כמאגר ארוך־טווח. האויסטרים שוברים את הכלל הזה. רקמותיהם מלאות בגליקוגן, ומחקרים קודמים הצביעו על כך שהרכיכות האלה שורפות סוכר במקום שומן כאשר המזון נדיר או בעת יצירת ביצים וזרע. החוקרים ביקשו לבחון האם גליקופאגיה — פירוק ממוקד של גליקוגן בתוך התאים — פועלת כנתיב הישרדות ראשי באויסטרים במהלך צום והתאוששות.
צפייה בתאים שמחליפים מצב מאגירה להוצאה
הקבוצה הרעיבה אותן לאויסטרים הפסיפיים במשך שבועיים ואז האכילה אותם שוב, ומדדה כיצד רקמותיהם הגיבו לאורך זמן. במהלך הצום, צביעות מיקרוסקופיות הראו עלייה בסמנים של אוטופאגיה — אותות "ניקיון" תאי — בדיוק במקומות שבהם מאוחסן הגליקוגן, בעוד שהגליקוגן עצמו הצטמצם. המאגרים של השומן, לעומת זאת, כמעט ולא השתנו. כאשר האויסטרים אוכלו שוב, הגליקוגן חזר במהירות וסימני האוטופאגיה ירדו. במקביל, רמות חלבון רצפטור מרכזי בשם STBD1, שמקשר ספציפית בין גליקוגן למכונת האוטופאגיה, עלו וירדו בקורלציה לשימוש בגליקוגן. רצפטור אחר המקושר למחזור שומן, p62, נשאר יציב במידה רבה. יחד, התבניות האלה מצביעות על נתיב מיחזור ייעודי שממוקד בסוכר: גליקופאגיה, לא ליפופאגיה של שומן, מבצעת את רוב העבודה באיזון האנרגיה של האויסטר.
הווּך המולקולרי שאוחז בגליקוגן
גליקופאגיה תלויה ב‑STBD1 שפועל כוו מולקולרי: הוא נקשר לגליקוגן ומעביר אותו לחלבוני מתאם קטנים שבונים ואזיקי מיחזור. באויסטרים התגלה כי ה‑STBD1 תכנת שונה מהמקבילה שלו בחולייתנים. חלבון האויסטר נושא את אזור אחיזת הגליקוגן שלו, המוכר כדומיין CBM20, בקצה הקדמי שלו (N‑terminus), בעוד ש‑STBD1 בחולייתנים ממקם את אותה יחידה בקצה האחורי (C‑terminus) וכולל זנב שומני נוסף העוגן לממברנות תאיות. מודלים חישוביים וסימולציות הציעו שסידור N‑טרמינלי אצל האויסטר מעניק ל‑CBM20 אחיזה חזקה וגמישה יותר על שרשראות סוכר מסועפות. ניסויים במעבדה חיזקו זאת: STBD1 טהור מאויסטר ניקה קשירת גליקוגן חזקה יותר מאשר STBD1 מדג או מעכבר, וכאשר כל הגרסאות הוביעו בתאים אנושיים, חלבון האויסטר הניע ירידה חדה יותר בגליקוגן במהלך אוטופאגיה מגורה.
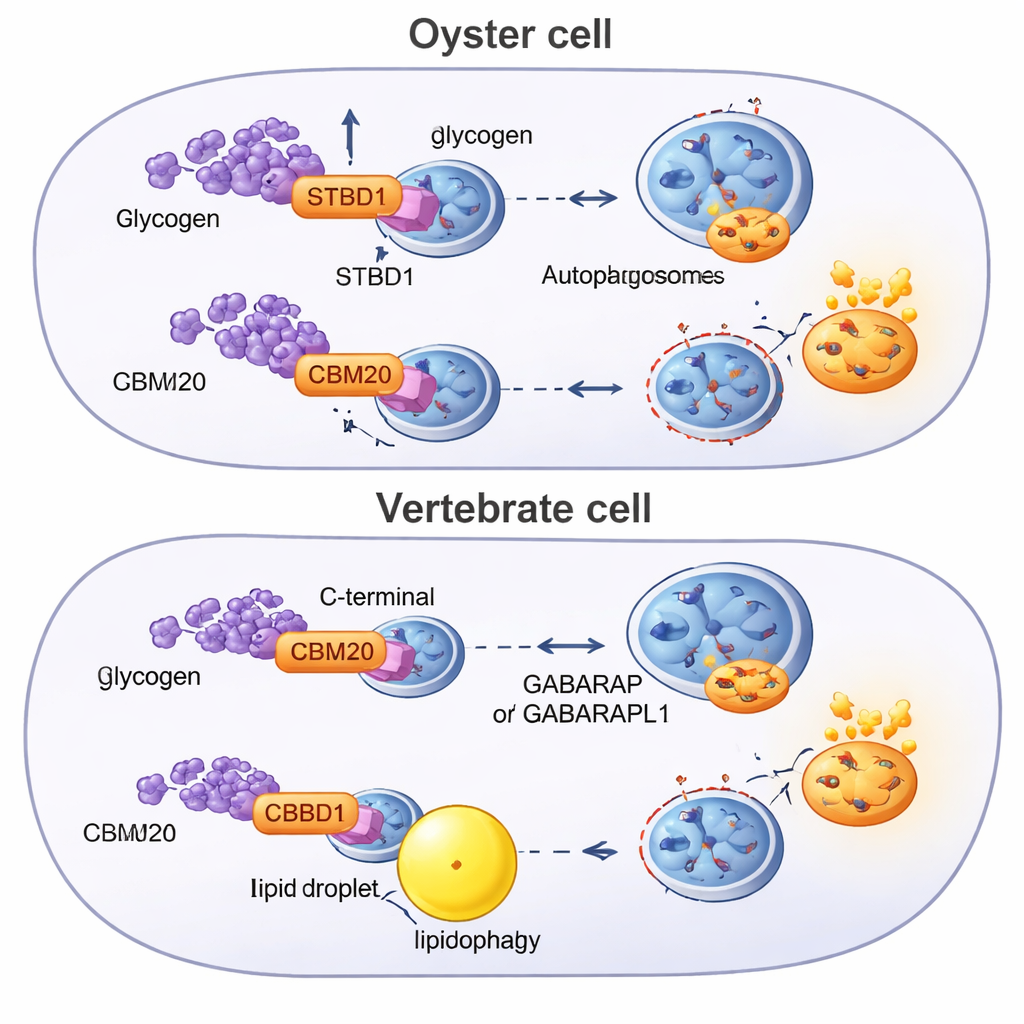
התאמת מסלול עתיק מחדש בקרב בעלי חיים
כדי להבין מאין הגיע המנגנון הזה, החוקרים סרקו גנומים מעשרות בעלי חיים עבור חלבונים הנושאים CBM20 ובנו עצי אבולוציה. הם מצאו ש‑STBD1 הוא המצאה בילטריאנית — הופיע באניצי האבות המשותף של בעלי החיים בעלי תכנון גוף דו‑צדדי — אך המבנה שלו עבר סידורים מחדש בקווי יוחסין שונים. האויסטרים ואחרים מבין הלופוטרוכוזואנים נוטים לשמור על העיצוב האבהי של CBM20 בקצה ה‑N, ולעתים אפילו לשכפל את היחידה הקשורת לסוכר. הקורדטים, הקבוצה הכוללת את החולייתנים, מציגים גרסה מובחנת שבה ה‑CBM20 הועבר לזנב החלבון. סידור זה מתקשר לקשירת גליקוגן חלשה יותר ולאסטרטגיית מטבוליזם שנוטה יותר להסתמך על פירוק שומן דרך ליפופאגיה, בתמיכה של רצפטורים וחלבוני מתאם נוספים שאויסטרים אינם מחזיקים.
מה המשמעות של זה עבור בחירות האנרגיה של החיים
ללא מומחיות מיוחדת, המסר המרכזי הוא שבעלי החיים פיתחו יותר מאסטרטגיה אחת לעבור תקופות של חוסר אנרגיה. האויסטרים ממחישים אסטרטגיה עתיקה וממוקדת בסוכר: גרסה בעלת זיקה גבוהה של STBD1 תופסת גליקוגן במהירות ומזינה אותו ליחידות המחזור התאי, מה שהופך את הגליקופאגיה למקור כוח עיקרי בזמן לחץ. חולייתנים, לעומת זאת, נראים כמי שהחליפו חלק מהאחיזה החזקה הזו בסוכר בגישה מאוזנת יותר או נוטה לשומן, בתמיכה של שותפי חלבון וארגונים דומיניים שונים. על ידי קישור בין מבנה חלבוני מפורט לבחירות דלק ברמה של האורגניזם, המחקר מדגים כיצד "השעיתיים" מולקולריים קטנים יכולים לעזור לענפים שונים בעץ החיים להתאים לסביבות ולסגנונות חיים משלהם.
ציטוט: Ren, L., Bai, Y., Shi, C. et al. Glycophagy is an ancient bilaterian pathway supporting metabolic adaptation through STBD1 structural evolution. Commun Biol 9, 268 (2026). https://doi.org/10.1038/s42003-026-09546-6
מילות מפתח: גליקופאגיה, מטבוליזם של גליקוגן, ביולוגיית חסילון/אויסטר, אוטופאגיה, אבולוציית המטבוליזם