Clear Sky Science · he
מעכבי PAK4 מעודדים פירוציטוזה מוּנעת-גמציטאבין בסרטן הלבלב דרך ציר NLRP1/caspase-3/GSDME
מדוע רצח תאי סרטן "בצורה לוהטת" יכול להיות חשוב
סרטן הלבלב הוא אחד הסרטנים הקטלניים ביותר, ואף ששיטות הכימותרפיה הטובות ביותר שלנו לעתים קרובות מפסיקות לעבוד כשהגידולים מפתחים עמידות. המחקר הזה בוחן טוויסט מפתיע: אותו תרופה, גמציטאבין, יכולה להרוג תאי סרטן בצורה מתפרצת ודלקתית יותר הנקראת פירוציטוזה — אם יצור מולקולרי מרכזי שפועל כ"בלם" בשם PAK4 מכוּבת. הבנה ועמידה ממוקדת על הבלם הזה עשויות לשפר את היעילות של טיפולים קיימים עבור מטופלים רבים.
סרטן עקשן שמזלזל בטיפול
אדנוקרצינומה צינורית של הלבלב מאובחנת בדרך כלל בשלב מאוחר ונענית גרוע לטיפול, ולכן גמציטאבין נותר תרופה מרכזית למרות מגבלותיה. גמציטאבין לרוב הורג תאים דרך אפופטוזה, צורת מוות מתוכננת, מסודרת ושקטה. אך יותר ממחצית הגידולים הלימודים במחקר זה ייצרו רמות גבוהות של חלבון בשם GSDME, שיכול להפוך מוות שקט לפירוציטוזה — צורת מוות מהירה "מתפוצצת" הפוגעת בממברנת התא ומשחררת אותות דלקתיים. זה העלה שאלה מרכזית: אם גידולים מסוגלים לעבור פירוציטוזה, מדוע רבים מהם עדיין עמידים לגמציטאבין?
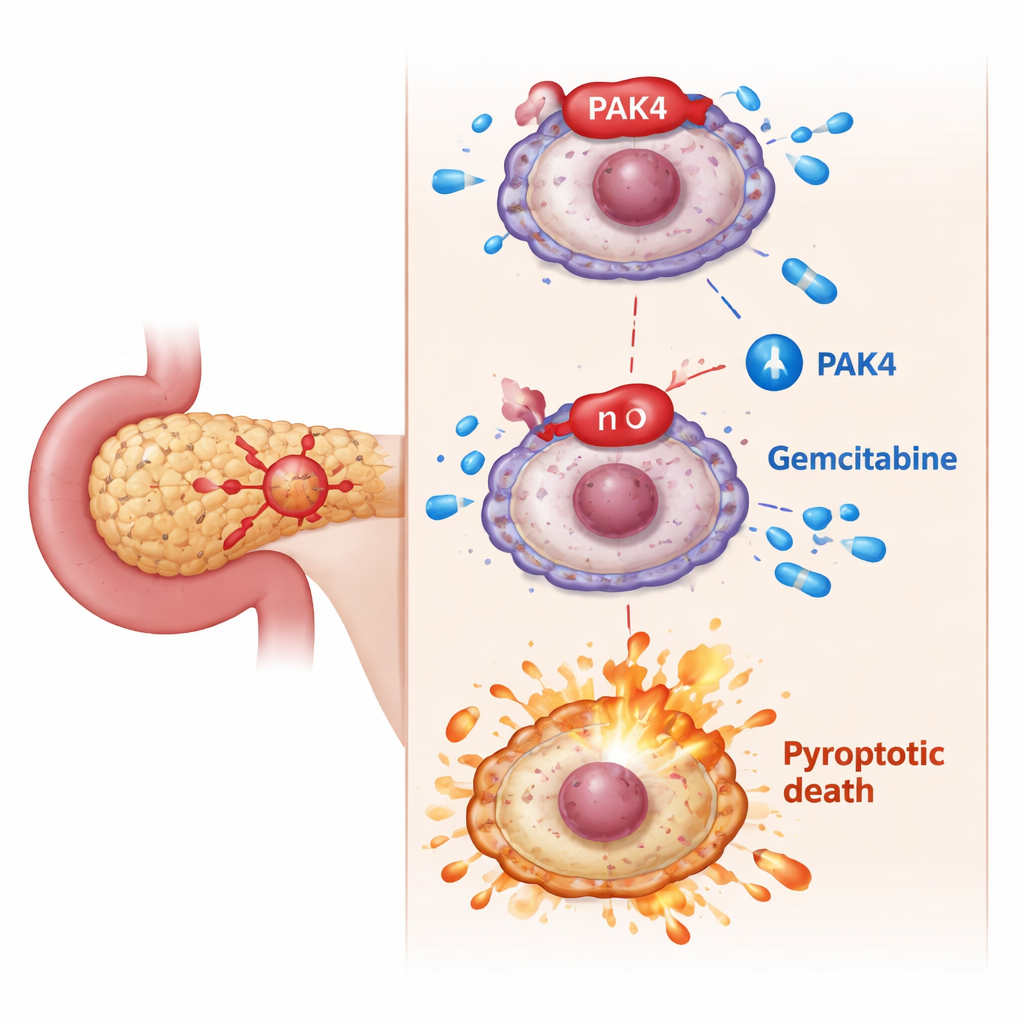
הבלם החבוי: PAK4 חוסם מוות לוהט
החוקרים ממקדו את תשומת לבם ב-PAK4, חלבון המקדם גדילה הידוע כפעיל יתר בסרטן הלבלב וקשור לתגובה חלשה לגמציטאבין. בניסויים תאי, תאי סרטן עם רמות גבוהות של PAK4 היו קשים יותר להשמדה עם גמציטאבין. כאשר הקבוצה הורידה את רמות PAK4, גמציטאבין הפך בפתאומיות לרעיל הרבה יותר: התאים הראו תכונות טיפוסיות של פירוציטוזה — התנפחות, בועות דמויות בלון, קריעת ממברנות ושחרור מוגבר של תכולת התא. ברמה מולקולרית, המעבר הזה תלוי בחיתוך של GSDME לקטע פעיל על ידי חלבון אחר, caspase-3. חסימת caspase-3 עצרה את היכולת של GSDME לעורר פירוציטוזה, ואישרה ש-PAK4 בדרך כלל פועל כדי לעכב את מסלול המוות הזה.
כיצד PAK4 מפרק את אזעקת המוות של התא
בהעמקה נוספת, המדענים מצאו ש-PAK4 אינו תוקף את GSDME ישירות. במקום זאת הוא לפוגג חיישן "אזעקה" על-זרם בשם NLRP1. אצל מטופלים, רמות גבוהות יותר של NLRP1 נקשרו להישרדות טובה יותר, מה שמעיד שהוא מסייע לגוף לשלוט על הגידולים. בתאים סרטניים, כאשר הסירו את NLRP1, הכמות של המוות המוּנעת-גמציטאבין והפעלת GSDME ירדה משמעותית, מה שמראה ש-NLRP1 מזין את המנגנון של הפירוציטוזה. רמות PAK4 ו-NLRP1 היו הפוכות במדגםי גידולים: במקום שבו PAK4 היה גבוה, NLRP1 היה נמוך. המחקר הראה ש-PAK4 הפעיל פועל דרך חלבון אחר, ה-E3 ligase Mdm2, כדי לסמן את NLRP1 להריסה על-ידי מערכת הסילוק התאית. על-ידי סימון NLRP1 כך, PAK4 מונע הפעלת תגובת שרשרת — דרך caspase-9 ו-caspase-3 — שברגיל הייתה מסתיימת בפירוציטוזה מונעת על-ידי GSDME.
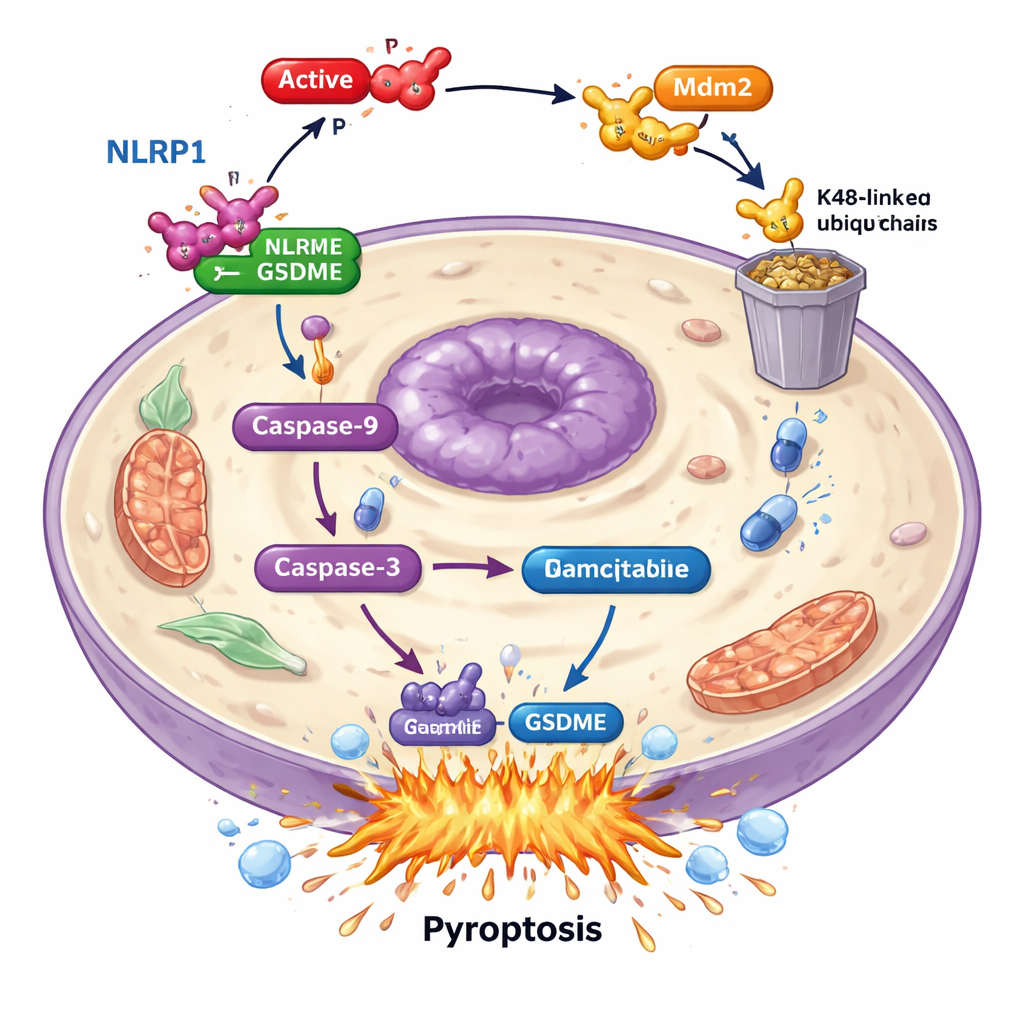
כיבוי PAK4 כדי להגביר את הכימותרפיה
מכיוון ש-PAK4 פועל כבלם על הפירוציטוזה, הצוות בדק האם חסימת פעילותו יכולה להעיר מחדש את כוחה ההורג של גמציטאבין. הם השתמשו בחסם קטלני-מולקולה ל-PAK4 בשם PF-3758309. כשהוא לבד, החסם הזה כבר דחף תאי סרטן הלבלב לעבר פירוציטוזה, הגביר את הפעלת caspase-3, חיתוך GSDME וקריעת ממברנת התא. בשילוב עם גמציטאבין, האפקט היה חזק אף יותר: יותר תאים מתו דרך פירוציטוזה, וסימנים מולקולריים של מסלול המוות הוגברו. במודלים עכבריים הנושאים גידולים אנושיים של הלבלב, או הפחתת PAK4 או טיפול בחסם PAK4 הפכו את גמציטאבין ליעיל יותר בכיווץ הגידולים והגבירו סמנים של פירוציטוזה בתוך הסרטנים.
מה זה אומר עבור מטופלים וטיפולים עתידיים
באופן פשוט, עבודה זו מגלה מנעול מולקולרי — PAK4 — שמונע מתאי סרטן הלבלב למות בצורה הרסנית באופן מיוחד תחת כימותרפיה. על-ידי נטרול PAK4, רופאים עשויים לדחוף גידולים המטופלים בגמציטאבין לעבר פירוציטוזה, להפוך את התרופה ליעילה יותר ואולי לעורר את המערכת החיסונית נגד הסרטן. אף שדרוש עוד מחקר במודלים נגזרי-מטופל ובניסויים קליניים, המחקר מציע מפת דרכים ברורה: לכוון לציר PAK4–Mdm2–NLRP1–GSDME כדי להפוך גידולים עמידים לגידולים רגישים, באמצעות שילובים חכמים של תרופות שכבר נמצאות ברשותנו.
ציטוט: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
מילות מפתח: סרטן הלבלב, התנגדות לגמציטאבין, פירוציטוזה, PAK4, טיפול ממוקד