Clear Sky Science · he
פלובסטטין מדכא את תחילת וסרטן השד והתקדמותו באמצעות מטרה על CYP4Z1
מדוע תרופה לכולסטרול חשובה לסרטן השד
נשים רבות המקבלות טיפול בסרטן השד מפתחות רמות שומנים בלתי תקינות בדם ומתמודדות עם סיכון מתמשך לחזרת המחלה או להתפשטותה. המחקר בוחן רעיון מרתק: האם כדור שכיח להורדת כולסטרול, פלובסטטין, יכול להיות ממוען מחדש כדי להאט או למנוע סרטן השד על ידי נטרול חלבון שמזין תאי גידול מסוכנים הדומים לתאי גזע?
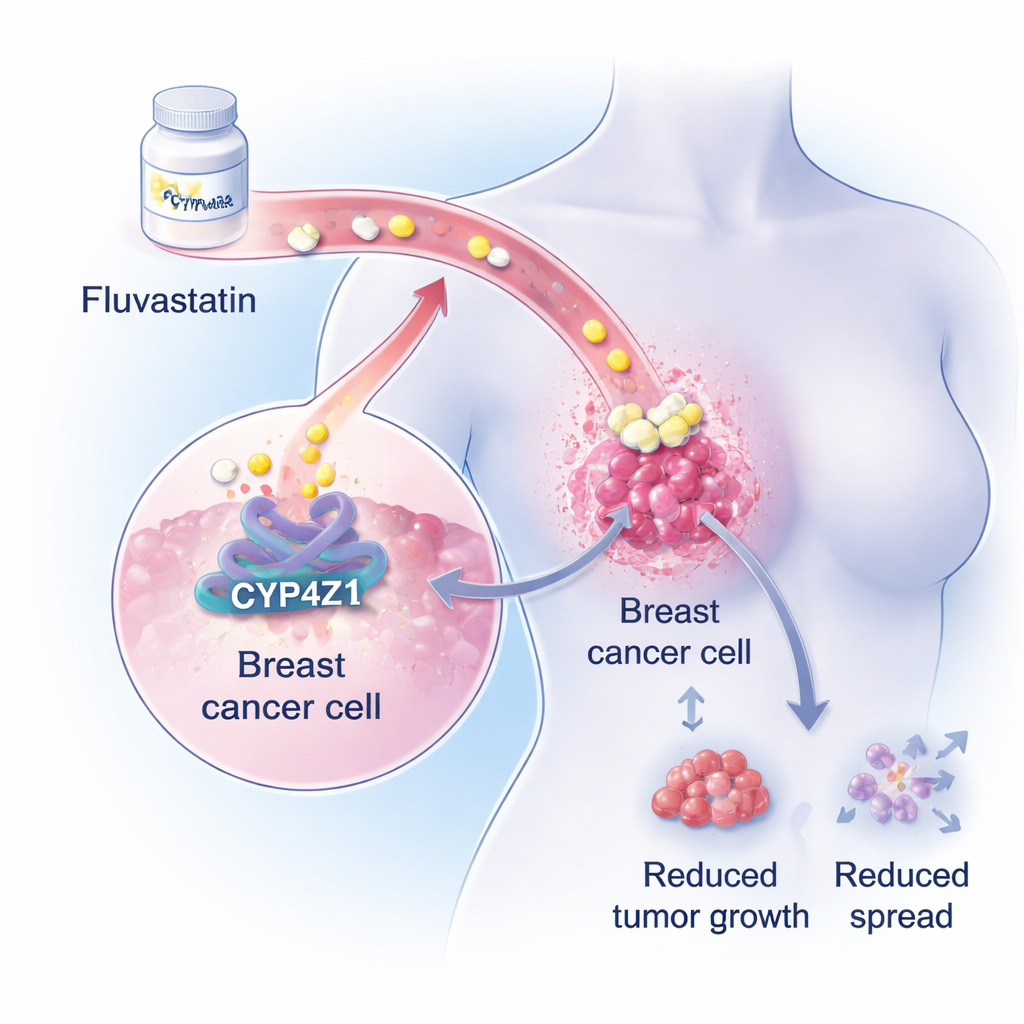
מניע מוסתר בתוך גידולי השד
החוקרים מתמקדים בחלבון פחות מוכר בשם CYP4Z1, שנמצא ברמות גבוהות בתאי סרטן השד אך לא ברקמה שדית בריאה. עבודות קודמות הראו ש-CYP4Z1 מסייע לתאי הסרטן להתנהג בדומה לתאי גזע — תאים שיכולים להתחדש ללא גבול, לעמוד בפני כימותרפיה ולהשיב את הגידול לאחר טיפול. בניתוחים גנטיים וביוכימיים גדולים מציג הצוות כעת כי פעילות מופרזת של CYP4Z1 מחזקת במידה רבה נתיבי בניית השומנים בתוך תאי סרטן השד, ובפרט את ייצור הטריגליצרידים, שהוא שומן מאגרי מרכזי. מכיוון שרבים ממטופלות סרטן השד מפתחות כבר הפרעות בשומני הדם במהלך כימותרפיה, תפקיד זה המעודד שומן של CYP4Z1 הציע נקודת פתיחה לתרופות קיימות להורדת שומנים.
מיון פלובסטטין משמירה על הלב לטיפול בסרטן
כדי לבחון רעיון זה, המדענים מסננים ספריה קטנה של 23 תרופות מאושרות על ידי ה-FDA המשמשות להורדת שומנים בדם. פלובסטטין, סטטין נלקח נפוץ להורדת כולסטרול, בלט כמבטיח: הוא חסם ישירות את פעילות האנזים של CYP4Z1 במידה התלויה במינון. במינונים שהיו מזיקים הרבה פחות לתאים שחלביים רגילים מאשר לתאי סרטן, פלובסטטין הפחית באופן חד סמנים מרכזיים של 'סטמנס' (מאפייני תאי גזע), את היכולת של תאי סרטן השד ליצור "כדורי גידול" צפים, ואת יכולתם לנוע וחודר דרך מחסומים דמויי רקמה בניסויים במעבדה. הוא גם הגביר את רגישות תאי הגידול לתרופת הכימותרפיה אדריאמיצין, מה שמרמז שהוא יכול להעצים טיפולים קיימים.
מבחן התרופה בחיות חיות
בהמשך הצוות העריך את השפעת הפלובסטטין במודלים של עכברים. בעכברים שקיבלו השתלה של תאי סרטן שד אנושיים, טיפול תקופתי בפלובסטטין האט את גדילת הגידולים, הוריד את רמות סמני הסטמנס (ALDH1A1) ואת סמן חלוקת התאים Ki67 בגידולים, והפחית את מספר הנגעים המטרסתיים שהופיעו בריאות. חשוב לציין שעכברים שקיבלו פלובסטטין שמרו על משקל גופם ולא הראו חריגות משמעותיות בדם או במח העצם, תומך בפרופיל בטיחות נאות במינון הנבדק. במודל גנטי ריאלי יותר — עכברים מהונדסים המפתחים גידולי שד מונעים על־ידי גן מסרטן — החוקרים הוסיפו גם את CYP4Z1 האנושי לרקמת השד. עכברים אלו פיתחו יותר נגעים פרה-סרטניים וסרטניים, ויותר גרורות בכבד ובריאות, מאשר בעלי החיים בקבוצת הביקורת. טיפול בפלובסטטין הפחית במידה ניכרת הן את מספר נגעי השד והן את הגרורות מרוחקות, במיוחד בעכברים שנשאו את גן ה-CYP4Z1 הנוסף.
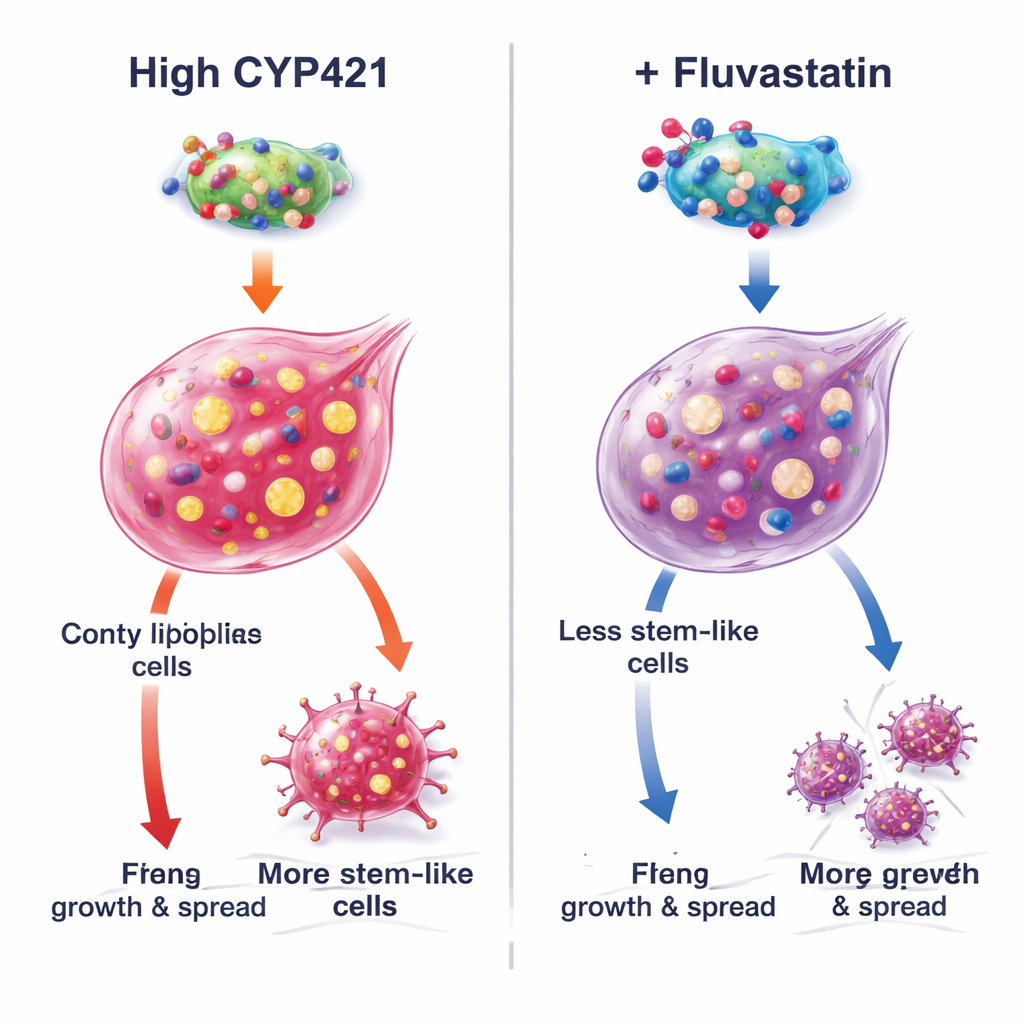
כיצד פלובסטטין מנטרל חלבון המעודד סרטן
כדי להבין את המנגנון, המחברים שילבו דוגמנות מחשבית עם הנדסת חלבונים מדויקת. הם חזו שפלובסטטין נכנס לאתר הפעיל של CYP4Z1 ומשתלשל לשלושה חומצות אמינו קריטיות (Lys109, Pro444 ו-Arg450). כשאתרים אלה הוטמעו במוטציות, פעילות ה-CYP4Z1 ירדה ופלובסטטין כבר לא הצליח לעכבו יותר, מה שאישר את הנקודות הללו כמרכזי עיגון. בתאים החסרים באופן טבעי CYP4Z1, הוספת החלבון הרגיל הגדילה את ה'סטמנס' והפעילה איתות מעודד גדילה PI3K/AKT, בעוד שפלובסטטין הפך אפקטים אלה. גרסאות מוטנטיות של CYP4Z1 היו פחות עוצמתיות ופחות תגובתיות לתרופה. ניסויים נוספים הראו שהשפעת פלובסטטין נחלשה כאשר ייצור הטריגליצרידים הוגבר באופן מלאכותי, או כאשר CYP4Z1 הושתק, מה שמדגיש שההשפעות החזקות של התרופה נובעות מחסימת החלבון הספציפי הזה ותוצאותיו של בניית השומן ולא מהפעלת מוות תאי דרך "פרורופתוזה" מונעת ברזל.
מה משמעות הדבר עבור מטופלות
בסך הכול, המחקר מציע שפלובסטטין, מעבר להורדת כולסטרול, יכול לדכא את השלבים המוקדמים וגם את התפשטות סרטן השד במודלים ניסיוניים על ידי מטרה על CYP4Z1, חלבון שמניע מטבוליזם שומני והתנהגות הדומה לתאי גזע בגידולים. כיוון שפלובסטטין כבר מאושר ובטיחותו מאופיינת היטב, ממצאים אלה מציעים נתיב מבטיח מבחינת בדיקות קליניות מהירות יותר כתרופה משלימה, במיוחד בחולות שהגידולים שלהן מבטאים בחוזקה את CYP4Z1. בעוד שעדיין נדרשת עבודה נוספת כדי לבדוק גישה זו בבני אדם ולזהות מטרות נוספות אפשריות של התרופה, המחקר פותח דלת לשימוש בתרופה מוכרת ללב כאסטרטגיה חדשה נגד סוגים אגרסיביים של סרטן השד הנוטים לחזור.
ציטוט: Li, H., Chen, Y., Shi, W. et al. Fluvastatin suppresses breast cancer initiation and progression via targeting CYP4Z1. Commun Biol 9, 254 (2026). https://doi.org/10.1038/s42003-026-09532-y
מילות מפתח: סרטן השד, פלובסטטין, תאי גזע סרטניים, חילוף חומרים של שומנים, שימוש חוזר בתרופות