Clear Sky Science · he
חסימה ממוקדת של עיבוד גנים עלולה להפר את ויסות ה‑microRNA הטבוע בלוקלוסי אינטרון
הודעות נסתרות בתוך הגנים שלנו
הרבה טיפולים גנטיים חדשים פועלים על ידי שינוי המסרים של ה‑RNA בתאים שלנו, אך ל‑RNA אלה לעתים קרובות יש "הערות בשוליים" נוספות שמדענים רק מתחילים להבין. המאמר הזה מראה שתרופות שנועדו לתקן חיתוך לקוי של גנים עלולות באופן בלתי צפוי להגביר RNAים רגולטוריים זעירים הקבורים בתוך אינטרונים — מקטעים בלתי מקודדים בין קטעי הגן — עם השפעות מפתיעות על חישוביות העצב והתפתחות המוח.
טיפולים גנטיים שמשנים RNA
אוליגונוקלאוטידים אנטיסנס, או ASOים, הם קטעים סינתטיים קצרים של חומר גנטי שנצמדים ל‑RNA ומשנים את אופן קריאתו או עיבודו. כמה ASOים כבר נמצאים בניסויים או בשימוש עבור מחלות גנטיות נדירות, במיוחד אלו הנגרמות מפגמים בחיתוך ה‑RNA — השלב שמחבר את מקטעי הקוד של הגן. רוב בדיקות הבטיחות מתמקדות בשאלה האם ה‑ASO משיב את החלבון הנכון ומונע תופעות לוואי ברורות. אבל הרבה גנים נושאים גם RNAים שאינם מקודדים, כולל microRNAים, בתוך האינטרונים שלהם. מולקולות זעירות אלה יכולות לכייל פעילות גנטית בעוצמה, ועד למחצית מה‑microRNAים הידועים בוורטברטים מקורם באינטרונים. המחקר החדש שואל: מה קורה ל‑microRNAים הטבועים האלה כשאנחנו מאלצים שינויים בחיתוך בעזרת ASOים?
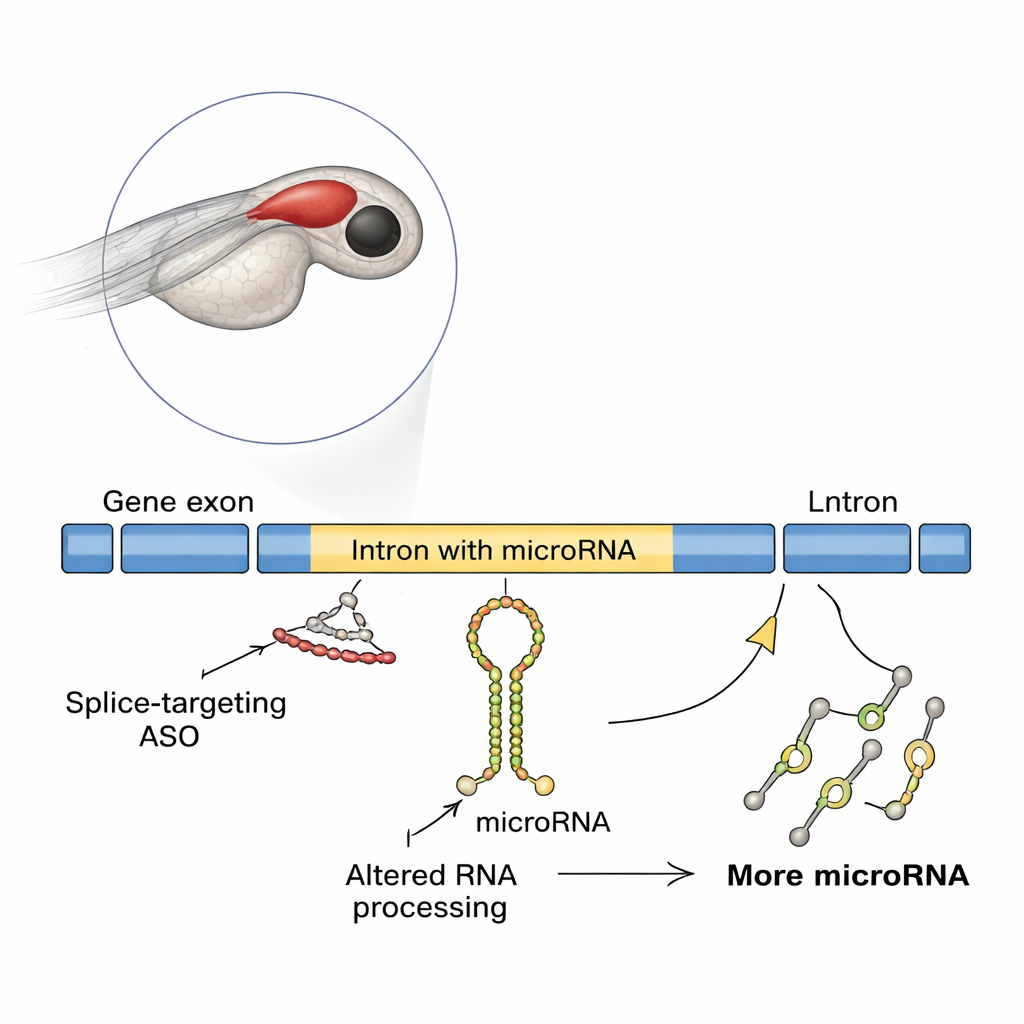
השפעה מפתיעה במוחות דגים מתפתחים
החוקרים השתמשו בזברה־פיש, דגם ורטברט פופולרי שעובריו השקופים מקלים על מעקב התפתחות המוח. הם התרכזו בגן בשם slit3, שעוזר לכוון סיבי עצב ומכיל microRNA בשם mir-218a-1 בתוך אחד האינטרונים שלו. כאשר הקבוצה חסמה את תחילת התרגום של slit3, התפתחות האקסונים שמפרישים הורמונים מההיפופיזה נראתה תקינה. אבל כששימשו ASO שחוסם חיתוך בנקודת חיתוך ספציפית של slit3, האקסונים שצריכים לפרוש להיפופיזה האחורית פחתו באופן דרסטי, אף על פי שמספר הנוירונים שמייצרים אוקסיטוצין נותר ללא שינוי. מבחנים מולקולריים הראו כי ה‑ASO שחוסם חיתוך גרם להשארת אינטרון ב‑RNA של הגן, והגביר באופן בלתי צפוי את רמות הטרנסקריפט של slit3, את האינטרון הארוך שלו ואת הטרנסקריפט הראשוני של ה‑microRNA הטבוע mir-218a-1.
microRNA — לא חוסר חלבון — הוא המניע של האנומליה
כדי לפענח מה גרם לבעיה האקסונית, המחברים השוו מספר תרחישים. חסימה של ה‑mir-218a-1 הבשל לבדו לא שינתה את רמות slit3, ו‑ASO נפרד שמיועד לאתר חיתוך אחר סמוך ל‑microRNA לא יצר ליקויי אקסונים ולא הגביר את mir-218a-1. קריטי לכך, כאשר ה‑ASO שחוסם חיתוך של slit3 שומש יחד עם ASO שמנטרל את mir-218a-1, החיבוריות האקסונית התאוששה במידה ניכרת. באופן דומה, בזברות חסרות גנטית של mir-218a-1, אותו ASO שחוסם חיתוך של slit3 כבר לא גרם לליקויי אקסונים, בעוד שהזרקה של דימוי סינטטי של mir-218a יכלה לשחזר את הפנוטיפ בדגים רגילים. ניסויים אלה מצביעים על כך שהעלייה ב‑microRNA האינטרוני — ולא חלבון Slit3 מקוצר — היא המניע העיקרי של ההפרעה ההתפתחותית.
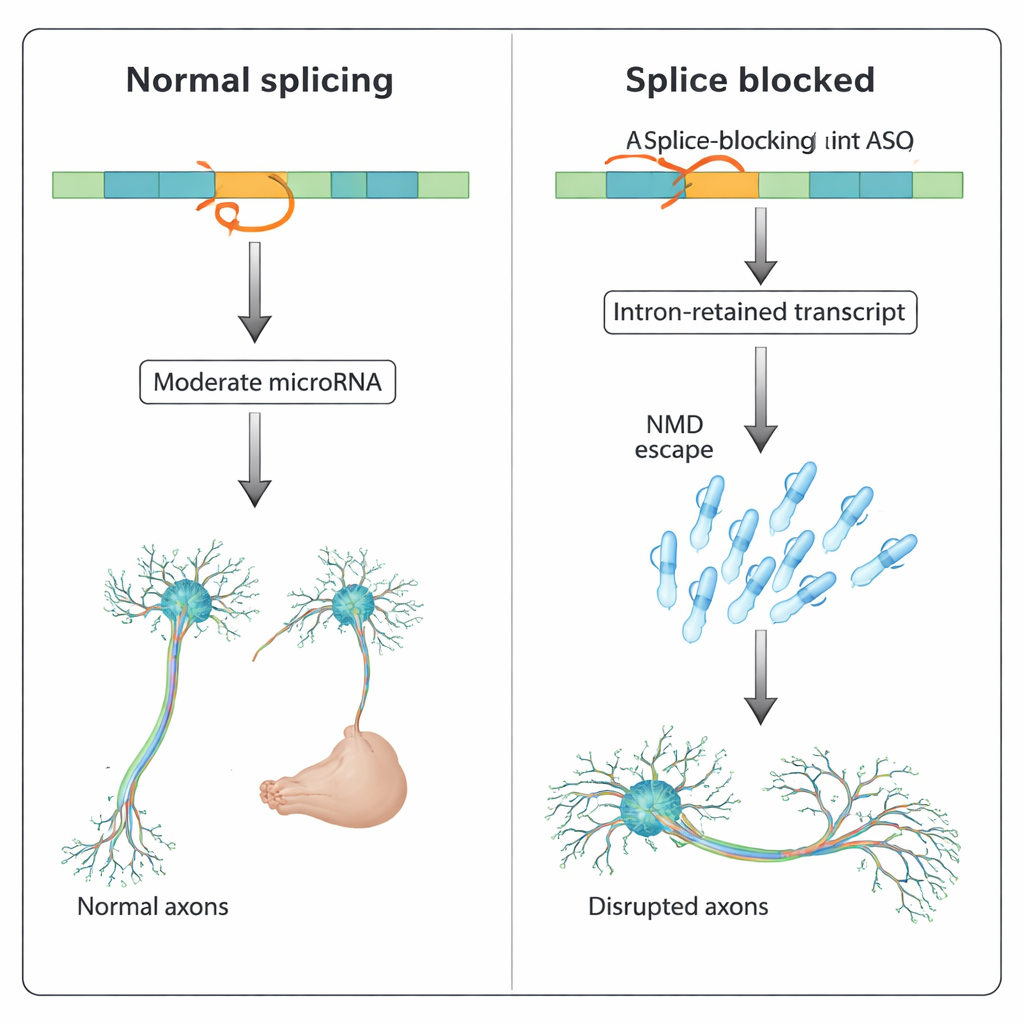
תבנית רחבה יותר במספר גנים
הקבוצה שאלה לאחר מכן האם האפקט הזה ייחודי ל‑slit3. הם חיפשו בגנום של זברה־פיש ומצאו עשרות גנים מקודדי חלבון שמכילים microRNAים אינטרוניים, רבים מהם מעורבים בהתפתחות וניתוב אותות. שני גנים כאלה, pank2 ו‑dnm2a, הראו בעבר בעיות התפתחותיות חמורות כאשר החיתוך שלהם נחסם על ידי ASOים, כולל הצטברות נוזלים מוחיים, נפיחות לב ועיוותי גוף — בעיות שכריתות גנטיות של אותם גנים לא השכפילו. במחקר זה, הזרקה משולבת של ASOים שחסמו ספציפית את ה‑microRNAים האינטרוניים mir-103 (ב‑pank2) או mir-199-5p (ב‑dnm2a) הצילה באופן חלקי את הפנוטיפים שמעוררים ה‑ASOים. במקרים מסוימים חסימת ה‑microRNA גם שחזרה את הביטוי של גן המאכסן, בעוד שבמקרים אחרים היא לא עשתה זאת, מה שמרמז כי פעילות microRNA מוגברת בפני עצמה יכולה להזיק גם כאשר השינויים ברמות הכוללות הם מתונים.
מה משמעות הדבר לטיפולים עתידיים
הממצאים מגלים כי ASOים שמטרתם חיתוך יכולים לגרום ליותר מאשר דילוג על אקסונים או השארת אינטרונים: הם יכולים לייצב טרנסקריפטים שבהם נותר אינטרון ולעקוף את מערכת בקרת האיכות של התא ולהגביר את ה‑microRNAים הראשוניים האינטרוניים, שמיד לאחר מכן מפריעים לרשתות של גנים-מטרה. בניורונים מתפתחים, פעילות microRNA פורצת שכזו יכולה לעוות את גדילת האקסונים והקישוריות. עבור מפתחי תרופות, המשמעות היא שפנוטיפים בלתי שגרתיים או "אוף‑טארגט" בניסויים על בעלי חיים לא תמיד נובעים ממסלולי רעילות כלליים כמו הפעלת p53, אלא מתוצאות לא מכוונות על RNAים אינטרוניים חבויים. השוואה זהירה בין ASOים שחוסמים תרגום לאלו שחוסמים חיתוך, ומעקב אחרי ביטוי microRNAים אינטרוניים, יכולה לסייע לזהות סיכונים אלה מוקדם ולחדד עיצובים של ASO לפני שהם מגיעים למטופלים.
ציטוט: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
מילות מפתח: אוליגונוקלאוטידים אנטיסנס, microRNA, חיתוך RNA, התפתחות זברה, בטיחות טיפול גנטי