Clear Sky Science · he
ניתוח חוסר-הומוגניות של אפיטופים חישובית בצביעות חיסוניות מסדרות דילול נוגדנים
מדוע איכות צביעת נוגדנים חשובה
מעקב אחר תאי סרטן ואבחון זיהומים — הביולוגיה המודרנית נשענת רבות על נוגדנים שמ"מאירים" מולקולות ספציפיות בתוך תאים. עם זאת, מעבדות רבות מתמודדות בשקט עם בעיה מטרידה: צביעות חלשות מדי, רעשיות או מטעות. המאמר מציג שיטה מעשית מבוססת מחשב להוציא יותר מידע מסדרת דילול נוגדנים שגרתית, ועוזר לחוקרים לכוונן את הצביעה לתמונות נקיות יותר, מדידות אמינות יותר ואף דרכים חדשות לצבוע מספר מטרות בערוץ צבע יחיד. 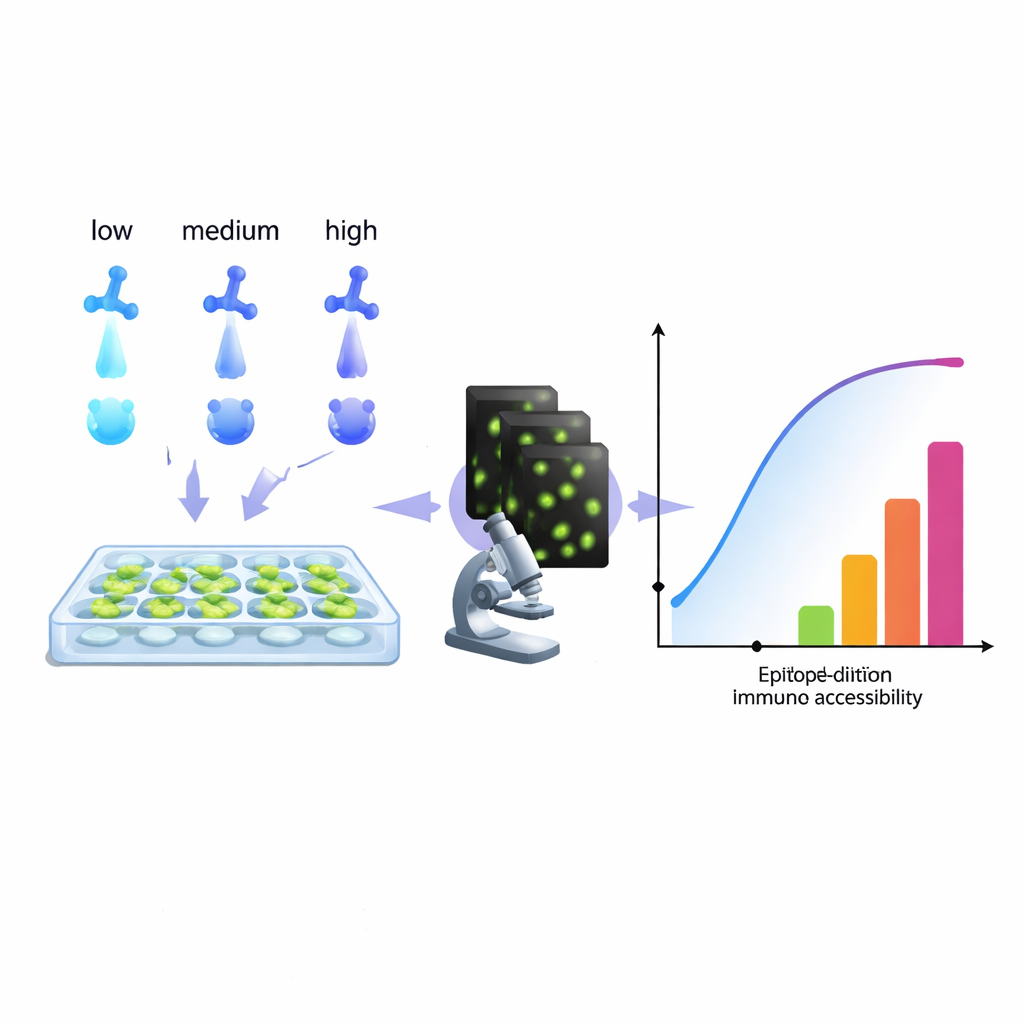
איך מדענים בדרך כלל מכוונים צביעות נוגדנים
כשחוקרים מכניסים ניסוי אימונוסטיינינג, הם בדרך כלל מניחים ריכוז נוגדן מדרישת היצרן, מנסים כמה דילולים ובוחרים את זה ש"נראה טוב". מאחורי הקלעים פועלים אינספור גורמים זעירים — צורת חלבון, צפיפות בתוך התאים, pH, והיכולת של הנוגדן להיכנס למקומו — שקובעים אם הנוגדן נדבק או נשבר בהשטפה. כלים מסורתיים למדידת קשירת נוגדנים, כמו רזוננס פלזמוני פני שטח, מתאימים יותר לחלבונים מטוהרים על משטחים מלאכותיים ולא לתאים או רקמות דחוסות. משמעות הדבר היא שהמספרים שהם מספקים עשויים שלא לשקף את המערכת הביולוגית שבה הנוגדן באמת משמש. כתוצאה מכך, מעבדות עלולות לבחור בריכוזים שמגבירים רקע מטושטש או מסתירים מטרות חשובות אך פחות נגישות.
להפוך סדרת דילול פשוטה ל"מפות נגישות"
המחברים מציעים גישה שונה: להתייחס לסדרת דילול נוגדנים סטנדרטית כסט נתונים עשיר ולהתאים אותה למודל שמשקף את מה שהדמיה באמת רואה — נוגדנים שנשארים קשורים גם אחרי שטיפות חוזרות. בניתוח האופן שבו האות גדל על פני הריכוזים, האלגוריתם שלהם משחזר "היסטוגרמת נגישות". במקום לנסות לבודד קבועי קשירה כימיים טהורים, ההיסטוגרמה מקבצת אתרי מטרה ל"כיתות אפיטופ" טכניות לפי קלות הצביעה שלהם בתנאים אמיתיים. אפיטופ ביולוגי יחיד עלול להופיע בכמה כיתות אם, למשל, הוא קל להגיע אליו בחלק אחד של התא וקשה באזור צפוף. חשוב: השיטה עובדת ישירות עם קריאת המיקרוסקופ, ללא צורך בחלבונים מטוהרים או בחומרה נוספת, כך שכל מעבדה שיכולה להריץ סדרת דילול ולכמת פלואורוסצנציה יכולה, מבחינה עקרונית, לבנות היסטוגרמות כאלה. 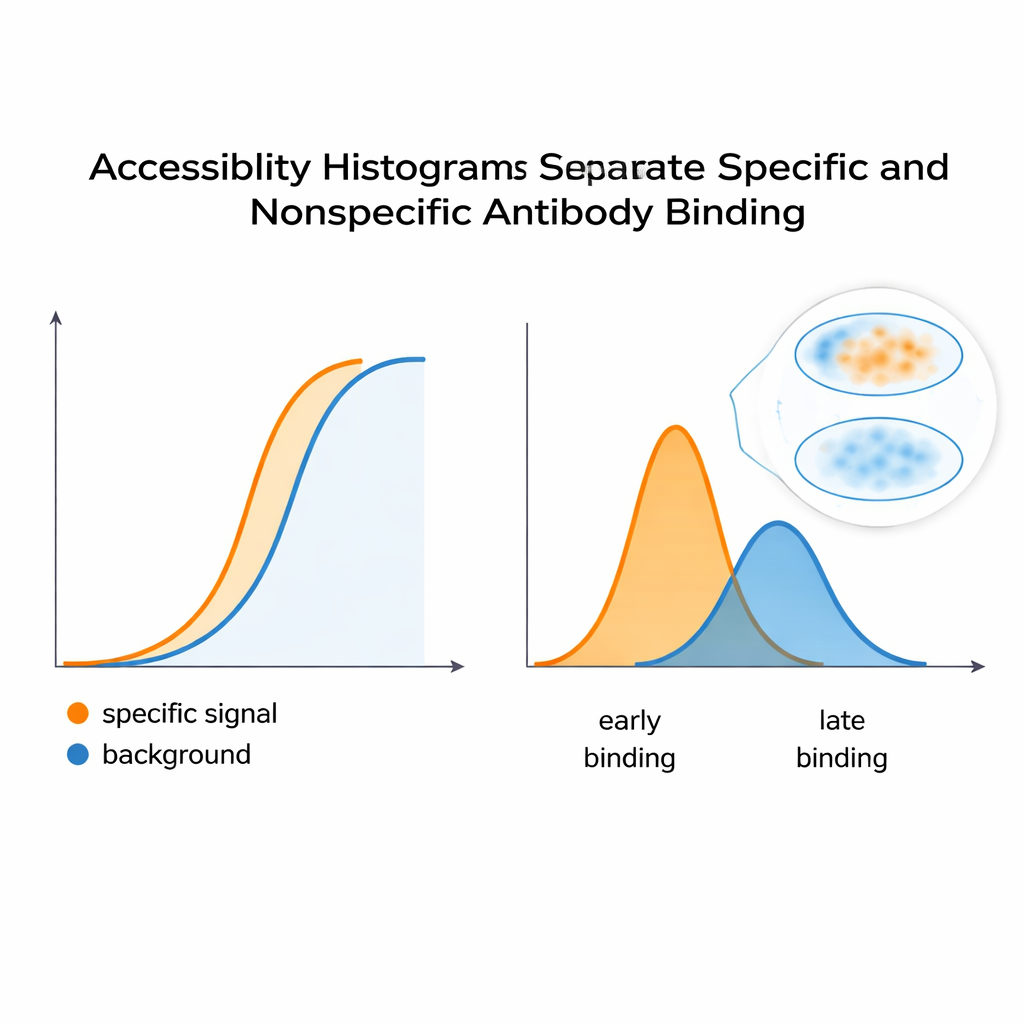
להפריד אות אמיתי מרקע
כדי לבחון האם ההיסטוגרמות אכן לוכדות את התנהגות הצביעה, הצוות בנה מערכת מבוקרת באמצעות תאי הלה ושני נוגדנים מונוקלונליים: אחד המדמה אות רצוי וספציפי ואחד שמתנהג כרקע בלתי רצוי. כשערבבו אותם, עקומת הפלואורוסצנציה המשולבת נראתה כמו תגובה חלקה אחת — דבר לא רמז על שני תורמים נבדלים. אולם הניתוח החישובי פרק את העקומה לשיאים נפרדים בהיסטוגרמת הנגישות, וחשף לפחות שתי כיתות אפיטופ בסיסיות. אסטרטגיה דומה שנועדה לנוגדן שמזהה אתר רגיש למבנה בתת־יחידת רגולציה של PKA הראתה כי שינויים בקונפורמציה של החלבון — שנגרמו על ידי מולקולה בשם cAMP — הזיזו את התפלגות האפיטופים הנגישים. זה מרמז שהשיטה יכולה לאותת על פתיחה או סגירה של מבני חלבון, שמשנה את קלות הקשירה של נוגדנים בתוך תאים.
בחירת דילולים טובים יותר וצביעה מרובה בצבע אחד
מכיוון שכל שיא בהיסטוגרמת הנגישות תורם בעיקר בטווח ריכוזים מסוים, המחברים משתמשים בשיאים הללו כמדריך לבחירת דילולי "הנקודה המתוקה". שיאים בעלי נגישות נמוכה שמופיעים רק ברמות נוגדן גבוהות מאד סבירים לכלול קשירה לא ספציפית, בעוד שיאים מוקדמים לרוב משקפים את המטרה המיועדת. על ידי מיזוג מודל כיצד שיאים בודדים בונים את עקומת התגובה למינון הכוללת, הצוות יכול להציע דילולים שממקסמים את האות הספציפי לפני ששיאים בעייתיים מופיעים — לעתים בדילולים דלילים בהרבה מההמלצות של היצרן. הם מרחיבים רעיון זה גם לצורת "מולטיפלקסינג חישובי" חכמה: על ידי צביעת אותו מדגם קבוע שוב ושוב בריכוזים שנבחרו בקפידה, ביצוע הדמיה אחרי כל סבב והחסרת תמונות מוקדמות מתמונות מאוחרות, הם מבדילים אותות המקושרים לכיתות נגישות שונות — ובכך מפרידים כמה מטרות בתוך ערוץ פלואורסצנציה יחיד.
מה המשמעות לעבודה מעבדתית יומיומית
במילים פשוטות, עבודה זו הופכת שלב פתרון בעיות שגרתי — הרצת סדרת דילול נוגדנים — לכלי כמותי. היסטוגרמות הנגישות מסייעות למדענים לזהות מורכבות נסתרת בצביעות שלהם, לבחור דילולים שמקטינים רקע מטעה, ובמקרים מסוימים להפריד אותות חופפים בלי צורך בתוויות פלואורסצנטיות נוספות. אף על פי שהמודל הבסיסי מכוון להיות פשוט ואינו לוכד כל פרט מולקולרי, הוא תכנן להיות קל לשימוש וחזק דיו לעיבוד נתונים מעשיים. אם יאומץ באופן רחב, גישה זו עשויה להפוך טכניקות מבוססות נוגדנים — מהדמיה בסיסית ועד בדיקות אבחוניות — לאמינות יותר, אינפורמטיביות יותר ופחות תלויות בניסוי ותהייה.
ציטוט: Tschimmel, D., Saeed, M., Milani, M. et al. Computational epitope heterogeneity analysis in immunostainings from antibody-dilution series. Commun Biol 9, 238 (2026). https://doi.org/10.1038/s42003-026-09517-x
מילות מפתח: צביעת נוגדנים, אימונופלואורנס, נגישות אפיטופ, תגובה למינון, מולטיפלקסינג חישובי