Clear Sky Science · he
התקדמות אסטרטגית ללימודים מבניים ב-cryo-EM של GPCRים קטנים (<100 kDa)
למה מתגי התא הקטנים חשובים לרפואה
חלק גדול מהרפואה המודרנית פועל על ידי דחיפה עדינה של מתגים זעירים המושיבים בממברנות התאים שלנו, המכונים קולטנים מקושרי חלבון G (GPCRs). מתגים אלה חשים הורמונים, ריחות ותרופות, וכמוהם כשליש מכל התרופות המאושרות פועלות עליהם. כדי לעצב תרופות בטוחות וחכמות יותר, החוקרים זקוקים לתמונות תלת־ממד מפורטות של הקולטנים האלה, במיוחד במצבים ה“כבויים” או הבלתי־פעילים שלהם, שאליהם תרופות רבות מכוונות במפורש. מאמר זה מסביר כיצד חוקרים לומדים לראות חלק מה‑GPCRים הקטנים ביותר באמצעות מיקרוסקופיה קריואלקטרונית (cryo‑EM), שיטה חזקה להדמיה שיכולה לצפות במולקולות קפואות במצב הקרוב לטבעי.
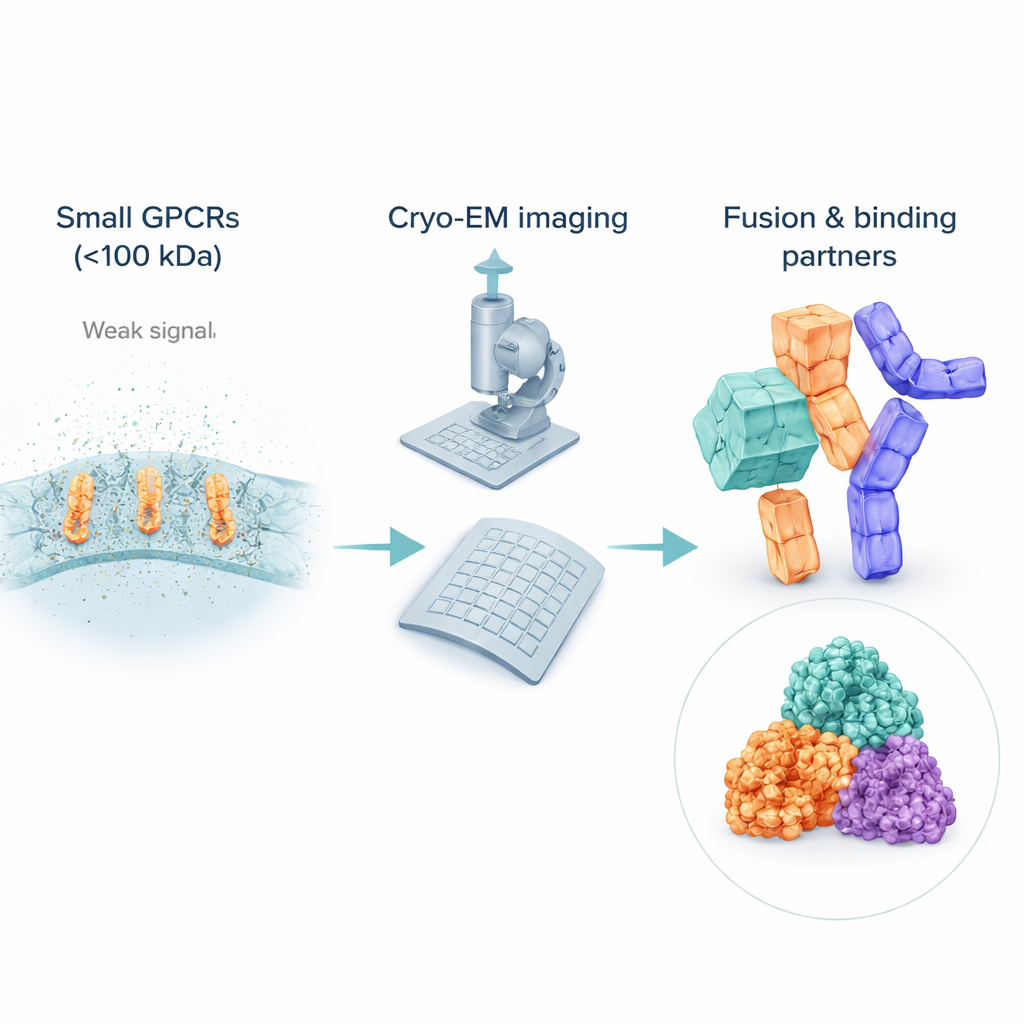
האתגר בלראות קולטנים קטנטנים מאוד
אף ש‑cryo‑EM חוללה מהפכה בביולוגיה מבנית, היא עדיין מתקשה מול מולקולות קטנות וגמישות. רבים מה‑GPCRs הבלתי־פעילים שוקלים הרבה פחות מ‑100 קילודלטון, מה שהופך אותם לקשים לזיהוי וליישור בתמונות רעשיות. כדי לשמור על המסיסות שלהם, החוקרים עוטפים את הקולטנים בבועות חומר ניקוי או בחיקויי ליפידים, אשר למעשה עלולים להיראות “גדולים יותר” לקרן האלקטרונים מאשר הקולטן עצמו, ולטשטש את האות של החלבון המבוקש. בשונה מקולטנים פעילים הקשורים לשותפים מגושמים כמו חלבוני G, ל‑GPCRs הבלתי־פעילים לעיתים חסרים תכונות חיצוניות בולטות, ולכן למחשבים קשה לממוצע מספר רב של תמונות לתצוגה תלת־ממדית חדה. כתוצאה מכך, רוב המבנים של GPCRs הבלתי־פעילים עדיין מגיעים משיטות קריסטלוגרפיית קרני־X ישנות יותר, מה שיוצר פער בכיסוי ה‑cryo‑EM בדיוק שם שרבים מהתרופות פועלות.
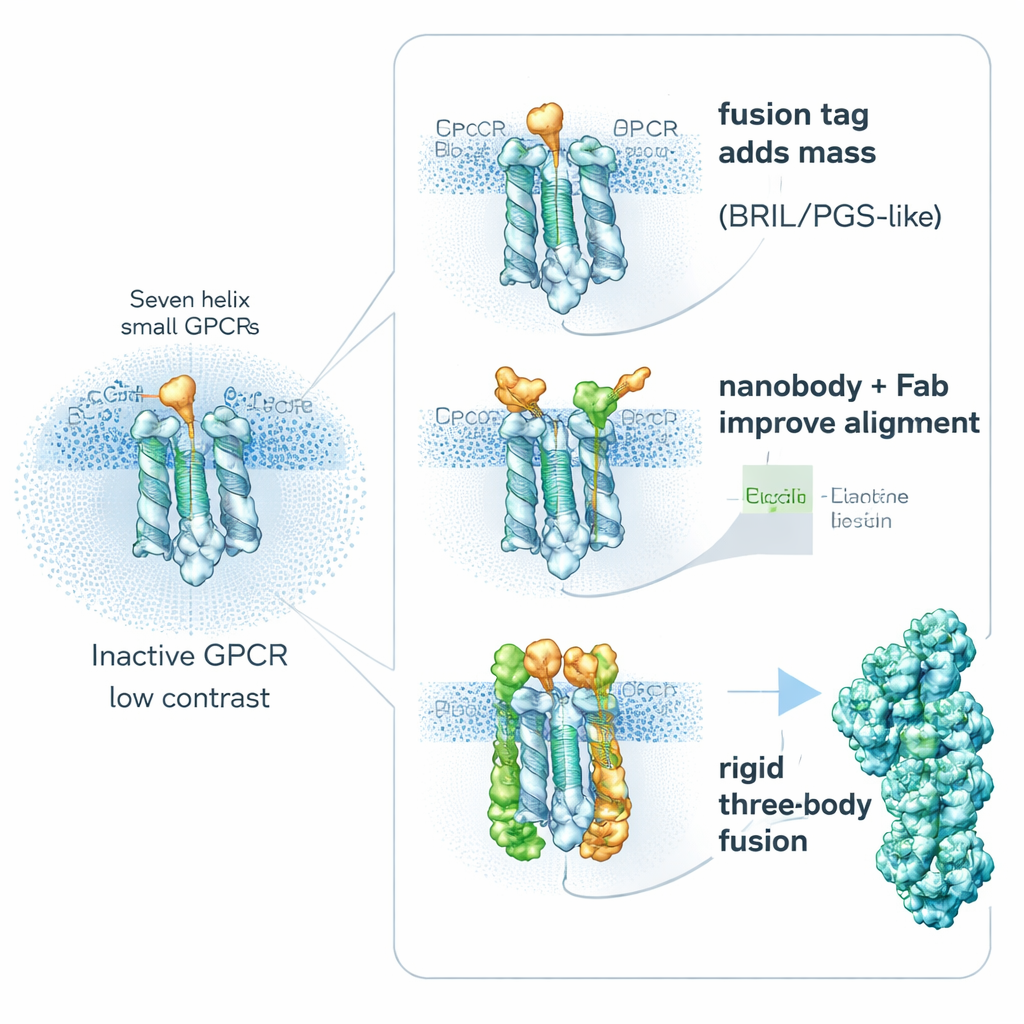
הגדלת משקל הקולטנים בעזרת מסייעים מובנים
אסטרטגיה מרכזית היא מפתיעה בפשטותה: להפוך את הקולטן “כבד” יותר בכוונה. חוקרים מאחדים גנטית חלבוני מסייע קטנים ויציבים לחלקים הגמישים של ה‑GPCRs כדי להגדיל את גודלם ונוקשותם, מבלי לחסום את אזורי קישור התרופות החשובים. מסייעים פופולריים כוללים את BRIL (חבילה של ארבע אלפאות), PGS (קטע של אנזים יציב תרמית) וחלבון גדול יותר בצורת מהדק המכונה קלצינורין. שותפי ההיתוך האלה מוזרקים לעתים קרובות ללולאה פנימית ניידת המחברת שתי האלפאות. על ידי ההקשחה של אזור זה הם מצמצמים את הטשטוש הנגרם מתנועת מולקולות ומספקים צורות זיהוי שעוזרות למחשבים ליישר את החלקיקים. מחקרים מראים שמיקום וזווית היתוך המדויקים יכולים להכריע הצלחה או כישלון של פרויקט: בקולטן אחד, תג PGS שהוצמד במיקום שונה שיפר את הרזולוציה מ‑6 אנגסטרום מטושטש ל‑3.7 אנגסטרום ברור בהרבה.
השאלת נוגדנים וקושרי מעצבים כידיות
נתיב שני נמנע מבניית היתוכים גדולים לתוך הקולטן ובמקום זאת מצמיד “ידיות” בעלות זיקה גבוהה מחוץ. קטעי נוגדן זעירים המכונים ננובודים וקושרים קרובים יכולים להיות מיוצרים להכיר GPCRs בלתי־פעילים ולהיצמד ללולאות פנימיות גמישות. דוגמה בולטת היא Nanobody‑6, שנוצרה בתחילה כחיישן לקולטן אופיאואידי אחד ואז שוחזרה, עם התאמות מצומצמות, לייצב כמה GPCRs נוספים במצבים הבלתי־פעילים שלהם. כיוון שהיא נקשרת מחוץ למרכז, היא נותנת לכל חלקיק רמז כיוון ברור, מה שהופך את ממוצע התמונות לאמין יותר. חוקרים לעיתים מרחיבים רעיון זה על‑ידי הוספת שכבה שנייה — קטע נוגדן רגיל שמזהה את הננובודי עצמו — וכך יוצרים קומפלקס מגושם ונוקשה יותר שמופיע חד ב‑cryo‑EM. קושרים מתוכנתים אחרים, כגון DARPins, יכולים לשמש כמפרידים מודולריים או כמחברים לכלוב חלבוני גדול יותר, ובכך מגדילים עוד יותר את האות ממטרות קטנות מאוד.
עיצוב דגימות חכם ועיבוד תמונה משופר בבינה מלאכותית
חיבור מסייעים או הוספת קושרים היא רק חלק מהסיפור. הסקירה מדגישה שמבנים טובים מתחילים בבניית קונסטרוקטים מוקפדת של הקולטן: קיצוץ אזורים זנביים רפויים, הכנסת מוטציות מייצבות ושימוש בכלי חיזוי מבנה מודרניים לזיהוי חלקים שעתידים לגרום לבעיות. בצד ההדמיה, תכסיסים ישנים כמו צלחות פאזה, המגבירות ניגודיות לחלקיקים חלשים, מוחלפים או מושלבים בכלי בינה מלאכותית. תוכנות למידה עמוקה יכולות לבחור חלקיקים זעירים הנסתרים במיקרוגרפים רעשיים, ואלגוריתמים חדשים מסוגלים למיין תמונות לצורות שונות כאשר הקולטנים מדגימים כמה קונפורמציות. יחד עם מסייעי רפרנס, ההתקדמות הזו דוחפת את ה‑cryo‑EM לפתור באופן מהימן חלבוני ממברנה שנחשבו בעבר לקטנים או דינמיים מדי למחקר.
מה המשמעות של זה לתרופות בעתיד
המאמר מסכם שאין “מסייע קסם” יחיד שמתאים לכל הקולטנים, אבל ערכת כלים גדלה של שותפי היתוך, קושרי‑דמויי נוגדן ושיטות מונעות‑AI פותחת בהדרגה את נוף ה‑GPCRs הבלתי־פעילים ל‑cryo‑EM. עבור לא‑מומחים, המסקנה המרכזית היא שעל ידי הפיכת הקולטנים הקטנים לגדולים ומסודרים יותר בעיני המיקרוסקופ, מדענים סוף‑סוף יכולים לקבל תמונות מפורטות של הצורות המדויקות שאליהן תרופות רבות מעדיפות להיקשר. המפות המבניות האלה צפויות להאיץ את עיצוב התרופות שמכבות את המתגים התאיים האלה ביתר דיוק — או מכוונות את פעילותם באופן עדין יותר — עם פחות תופעות לוואי.
ציטוט: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
מילות מפתח: קולטנים מקושרי חלבון G, מיקרוסקופיה קריואלקטרונית, גילוי תרופות, ביולוגיה מבנית, תבניות ננובודי