Clear Sky Science · he
חיבור בין מתיחות מולקולרית ולחצי משיכה תאיים: גישה מולטי-סקייל למכניקת הדבקות מוקדית
איך תאים מרגישים וגוררים את סביבתם
בכל פעם שתא נע, מתחלק או מעצב מחדש רקמה, הוא מושך בעדינות את סביבתו. המשיכות המכאניות הקטנות הללו חשובות בריפוי פצעים, בהתפשטות סרטן ובאופן שבו איברים מתפתחים, אך קשה לראותן וקשה עוד יותר למדודן. מחקר זה מציג דרך חדשה להסתכל על הכוחות האלה משתי זוויות בו־זמנית: עד כמה תא שלם מושך חומר רך וכמה כוח נושא כל "קפיץ מולקולרי" בודד בתוך אתרי העיגון של התא. על ידי קישור בין שתי התצפיות האלה, העבודה מסייעת להסביר כיצד תאים חשים קשיחות ומווסתים את אחיזתם בעולמם.
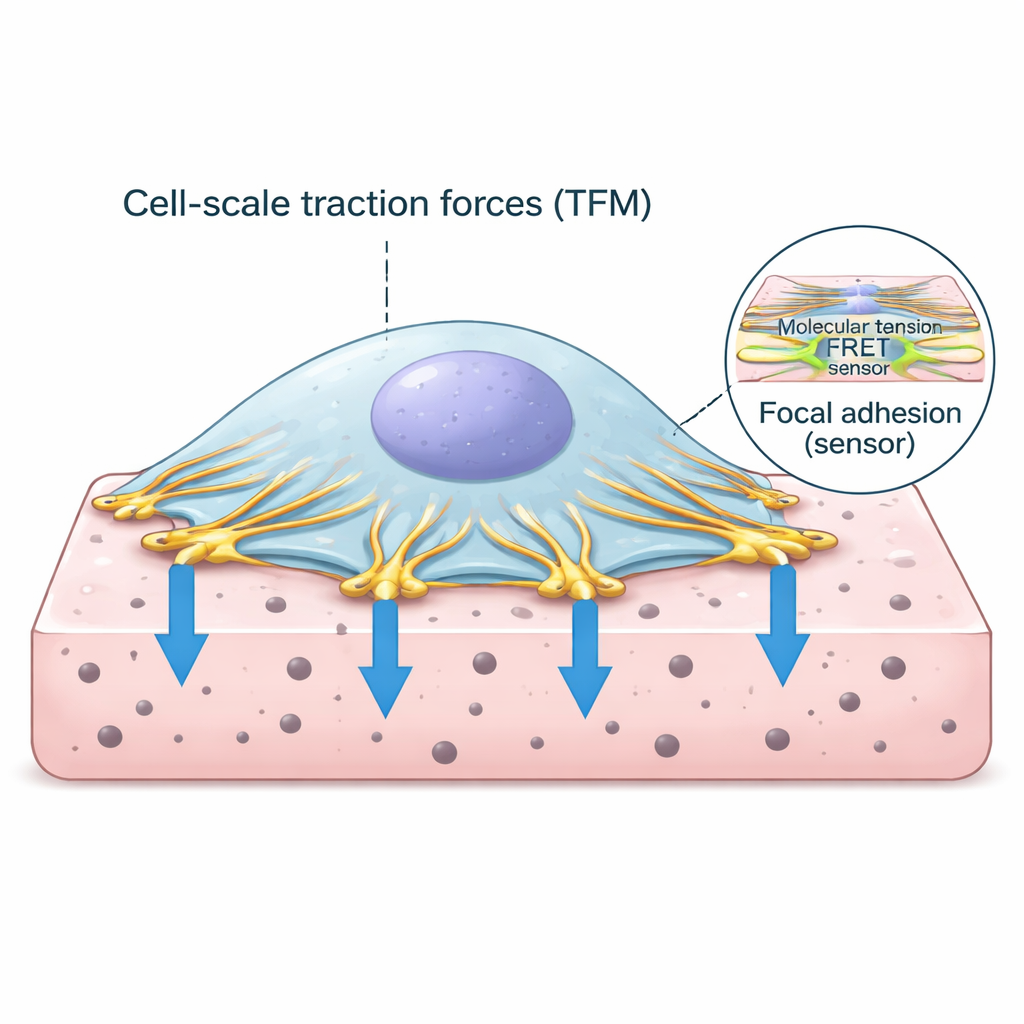
נקודות האחיזה של התא בעולם החיצוני
תאים אינם פשוטים צפים ברקמות; הם מעגנים את עצמם דרך נקודות מגע מיוחדות הנקראות הדבקות מוקדיות. בנקודות אלה, שלד האקטין הפנימי של התא מתחבר לחלבונים החוצים את ממברנת התא ונצמדים למטריקס הסביבתי. אחד החלבונים המרכזיים במורכב העיגון הזה הוא ונקולין, שמתנהג כקשר הרגיש לכוח. כאשר מכונת הכיווץ של התא מושכת את האקטין, ונקולין מרגיש את העומס ועוזר לחזק את החיבור. הבנת כמות הכוח שעוברת דרך הקשרים האלה וכיצד היא קשורה למשיכה הכוללת של התא היא מרכזית לפענוח כיצד רקמות נשארות בריאות או נעשות חולות.
שתי חלונות אל כוח תאי
החוקרים שילבו שתי טכניקות עוצמתיות בעבודה אחת. ראשית, מיקרוסקופיית כוח משיכה מודדת עד כמה תא מעוות מצע רך בדמוי ג'ל על ידי מעקב אחרי תזוזת חלקיקי פלואורסנציה זעירים בג'ל. מתנועות החלקיקים הללו ניתן לחשב את התפלגות כוחות הדחיפה והמשיכה מתחת לתא. שנית, חלבון ונקולין מהונדס במדויק נושא חיישן מתיחה פלואורסצנטי שמשנה את אות האור שלו כשהוא נמתח. באמצעות הדמיית זמן־קיום מתקדמת, הקבוצה המירה את אות האור הזה לקריאה של מתיחות מולקולרית על הונקולין. הם תכננו הידרוג'לים דקים ושטוחים שניתן לדמותם ברזולוציה גבוהה וכתבו תוכנה מותאמת לצורך יישור, סגמנטציה וניתוח של שני מערכי הנתונים עד לרמת אתרי העיגון הבודדים.
כיצד קשיחות משנה את מאמץ התא
כאשר תאים גדלו על ג'לים רכים לעומת קשים יותר, ההתנהגות הכוללת שלהם השתנתה בצורה ברורה. על מצעים קשים יותר, התאים התרחבו יותר והפעילו כוחות משיכה חזקים יותר על פני משטח הג'ל. באותו זמן, הקריאה הפלואורסצנטית מחיישן הונקולין הראתה מתיחה מולקולרית גבוהה יותר בתוך ההדבקות המוקדיות. מעניין שהמאפיינים המבניים הבסיסיים של ההדבקות — כמו מספרן או גודלן הממוצע — לא השתנו הרבה בין ג'לים רכים וקשים. במקום זאת, האופן שבו הכוחות היו מאורגנים השתנה. הדבקות גדולות, מכוונות רדיאלית עם יותר ונקולין נטו לשאת מתיחות משיכה גבוהה יותר, מה שמרמז ששני הגיאומטריה והמיקום המולקולרי של אתרים אלה מסייעים לקבוע עד כמה התא מושך.
קשר מורכב בין כוחות מקומיים ומולקולריים
מבט מעמיק יותר על הדבקות בודדות חשף שהקשר בין משיכה מקומית למתיחת ונקולין אינו אחיד. בחלק מהתאים, הדבקות שיצרו משיכות גבוהות הראו גם מתיחת ונקולין גבוהה יותר, דבר המשליך שהמגעים המעורבים שנושאים עומס מחלקים כוח ישירות יותר דרך הקשרים המולקולריים שלהם. בתאים אחרים הופיעה הדפוס ההפוך: אזורים של משיכה חזקה קושרו למתיחת ונקולין נמוכה יותר, בעוד שהדבקות אחרות נשאו עומס מולקולרי רב יותר ללא ייצור משיכות חיצוניות גדולות. תאים רבים לא הראו כלל דפוס ברור. התנהגויות מובחנות אלה משקפות כנראה מצבים תאיים שונים — כמו התפשטות פעילה, הדבקה יציבה או נסיגה — ומרמזות שהתאים יכולים להפיץ כוחות ברשת ההדבקות שלהם בדרכים שונות.
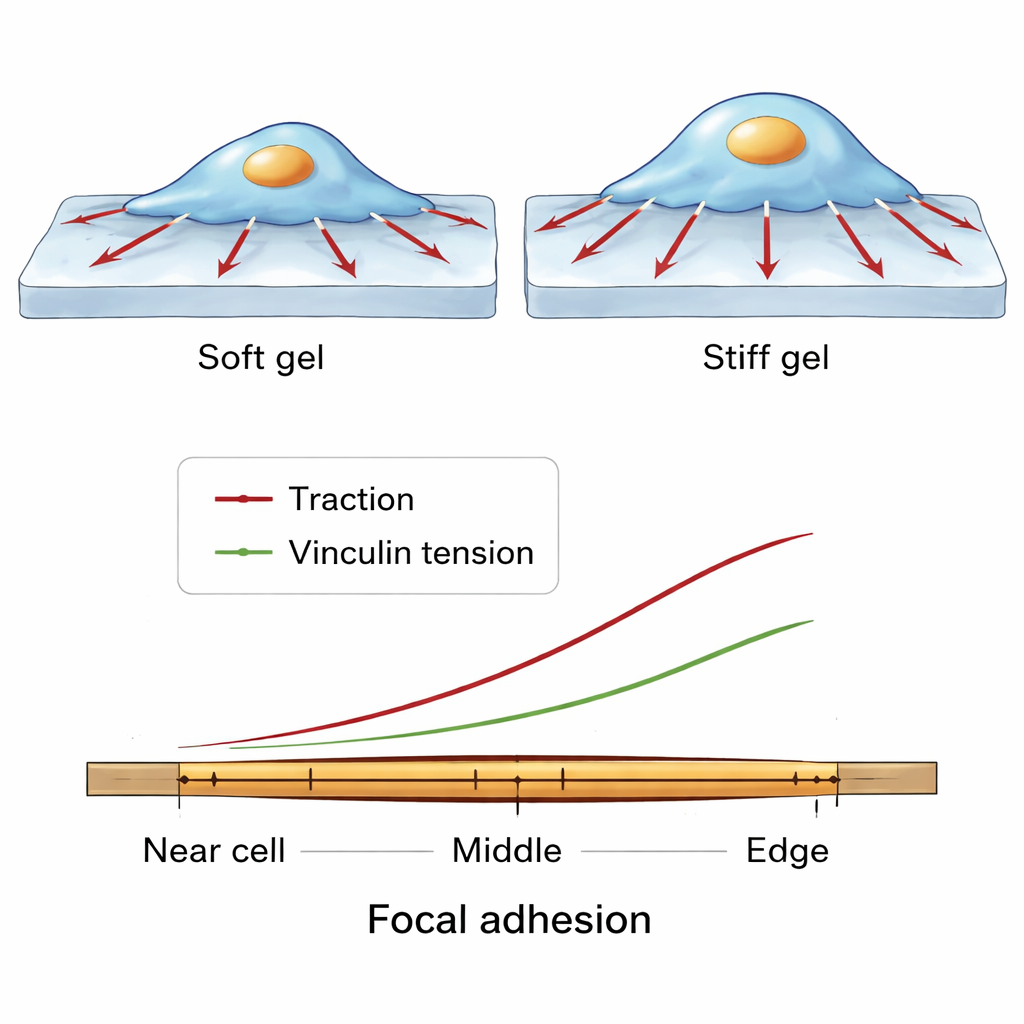
תבניות כוח עדינות לאורך נקודת אחיזה יחידה
הצוות אז הגדיל את המיקרו-סקופ עוד יותר, ובחן כיצד הכוחות משתנים לאורך אורך של הדבקה מוקדית יחידה, מן הצד הקרוב יותר למרכז התא ועד לקצה הקרוב להיקף התא. בחלק גדול מהתאים והתנאים נתגלה דפוס עקבי. מולקולות ונקולין היו מרוכזות ביותר בכיוון האמצע של ההדבקה. עם זאת, הן המשיכה המופעלת על המצע והן המתיחה המולקולרית על הונקולין עלו לקראת הקצה החיצוני, הפריפריאלי יותר. הדבר מציע איזון: באזורים מרכזיים, מולקולות ונקולין רבות יכולות לחלוק את העומס, ולכן כל מולקולה חשה פחות מתיחה, בעוד שבקצה החיצוני פחות מולקולות נושאות יחסית יותר כוח, תומכות במשיכה מקומית חזקה תוך שמירה על שלמות ההדבקה.
מה משמעות הדבר לבריאות ומחלה
על ידי איחוד מפת משיכות של תא שלם עם מדידות מתיחה ברמת החלבון, מחקר זה מציע תמונה מולטי-סקייל של האופן שבו תאים מנהלים את אחיזתם המכאנית. העבודה מראה שכשהסביבה מתקשה, תאים גם מושכים בחוזקה יותר וגם מעמיסים יותר על הקשרים של הונקולין, אך שהקשר המפורט בין הכוחות החיצוניים למתיחה המולקולרית משתנה מאתר הדבקה לאתר ומתא לתא. לצד זאת, דפוס מרחבי יציב של חלוקת הכוח בתוך ההדבקות הבודדות נראה נשמר. עבור הקורא הלא‑מומחה, המסר המרכזי הוא שתאים מווסתים בקפידה הן היכן והן איך הם מושכים, מפזרים כוח על פני רבים מ"קפיצים" מולקולריים קטנים כדי להסתגל לסביבות מכאניות שונות — עקרון שעשוי להיות בסיסי לתהליכים מגוונים כמו התפתחות רקמות, פיברוזיס וחדירת סרטן.
ציטוט: Aytekin, S., Kimps, L., Coucke, Q. et al. Linking molecular tension and cellular tractions: a multiscale approach to focal adhesion mechanics. Commun Biol 9, 236 (2026). https://doi.org/10.1038/s42003-026-09514-0
מילות מפתח: מכניקת תאים, הדבקות מוקדיות, ונקולין, מיקרוסקופיית כוח משיכה, מכנוטרנסדוקציה