Clear Sky Science · he
ויסות מקבוצת GPCR מסוג B1 בבני אדם על־ידי שומני ממברנה פלזמטית
שומנים שמדייקים את קולטי ההודעה בתא שלנו
התאים שלנו מסתמכים על אנטנות חלבוניות זעירות, הקרויות קולטנים, כדי לחוש הורמונים וחומרים כימיים מוחיים. תרופות רבות מצליחות פועלות על ידי מיקוד בקולטנים אלה. המחקר הזה מגלה כי שומנים שכיחים בשכבה החיצונית של התאים עושים הרבה יותר מאשר ליצור רקע פסיבי: הם אוחזים במישרין ומעצבים משפחה של קולטנים מרכזיים, וכך משפיעים ברמז על אופן ההפעלה והכיבוי של האותות. הבנת שכבת הבקרה הנסתרת הזו עשויה לסייע בתכנון תרופות חכמות יותר עם תופעות לוואי פחותות.
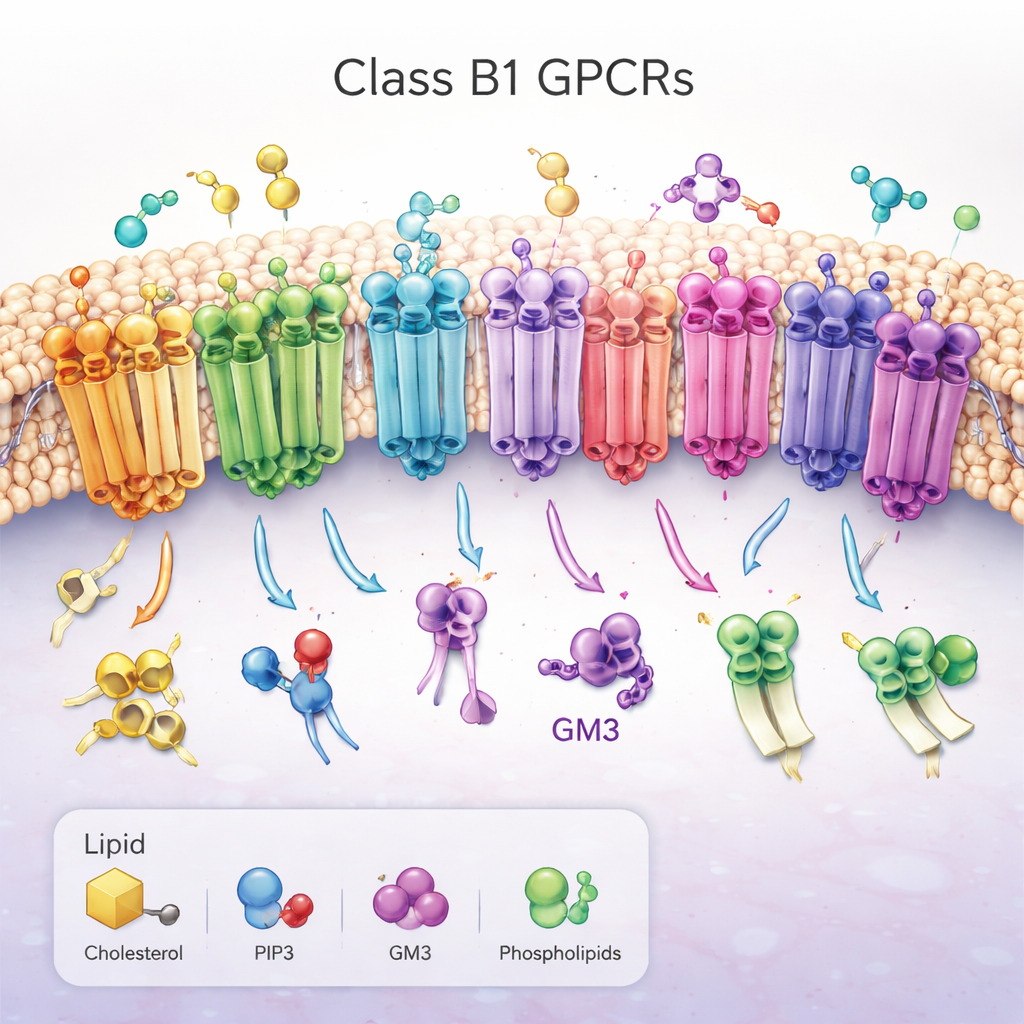
משפחה של אנטנות מולקולריות חשובות
העבודה מתמקדת בקולטן מקבוצה B1 של קולטני G החלבוניים (GPCR), קבוצה של 15 קולטנים קרובים שאחראים על בקרה של רמת הסוכר בדם, חילוף חומרים, גדילה ומערכת התגובה ללחץ. הם נמצאים חוצי ממברנת התא החיצונית, עם "ראש" גדול מחוץ לתא שחקוק מולקולות דמויות הורמון וחבילה של שבעת ההליקסים שעוברים דרך הממברנה השומנית. בהפעלה, הקולטנים משנים צורה בחלק הפנימי של התא, פותחים חריץ שמגייס חלבוני שותפים ומפעיל מסלולי איתות. בגלל תפקידם המרכזי במחלות כמו סוכרת והשמנה, קולטני B1 הם מטרות חשובות לתרופות, אך האופן שבו שומני הממברנה שמסביב מסדירים אותם נותר בגדר תעלומה עד כה.
סימולציה של הקולטנים בשכונתם הטבעית
במקום לחקור קולטנים בבועות דטרגנט מלאכותיות, החוקרים הציבו את כל 15 קולטני ה-B1 האנושיים בתוך ממברנות שנבנו במחשב המדמות את התערובת המורכבת של השומנים בתאים אמיתיים. באמצעות טכניקה שנקראת דינמיקה מולקולרית בקנה מידה גס, הם הריצו סימולציות ארוכות מרובות של כל קלטן גם במצב פעיל וגם במצב לא פעיל, בסך הכל כמילישנייה של זמן מדומה. הם עקבו איך שלושה שומנים "ויסותיים" — כולסטרול, שומן איתותי PIP2 והשומן המכוסה סוכר GM3 — ניגשים, נקשרים ומשתחררים מאיזורים שונים בכל קלטן. כדי להבטיח שאחרים יוכלו לשחזר ולבנות על מאגר נתונים עצום זה, הם תיעדו כל שלב בהגדרה ובניתוח באמצעות כלי עבודה פתוח שנקרא aiida-gromacs, והשוו את התוצאות מבוססות-הפיזיקה שלהם עם תחזיות ממודל בינה מלאכותית חדש (Chai‑1) שמנבא כיצד חלבונים נקשרים למולקולות קטנות.
כיסים נסתרות ואחיזה שומנית שמורה
הסימולציות חשפו תבניות קשירה חוזרות על עצמן לאורך כל משפחת הקולטנים. הכולסטרול, המוכר משיחות על תזונה, נראה נוטה להיקבע לא רק באתר ידוע קודם על אחד ההליקסים אלא גם ב"כיסי ממברנה עמוקים" בין ההליקסים, כאשר הראש הקוטבי שלו שקוע בצורה יוצאת דופן עמוק לתוך הממברנה. קלטן אחד, קלטן הסקרטין, הציג קשירת כולסטרול ארוכת־טווח במיוחד בכיסים מובחנים בצורות הפעילות והלא־פעילות שלו, מה שעשוי להעיד שכולסטרול משפיע באופן חזק על אופן האיתות שלו. PIP2 גילה התנהגות משומרת בולטת: הוא התקבץ סביב המשטח הפנימי של הקולטנים בצומת של שני הליקסים ובמקטע זנב קצר (TM6, TM7 ו‑H8), במיוחד כאשר הקולטנים היו במצב הפעיל. באתר זה, רשתות של חומצות אמינו בעלות מטען חיובי אחזו בקליפת הראש של ה‑PIP2 בעלת המטען השלילי, מה שמציע מנגנון שבו השומן הזה עשוי לייצב את הצורה הפעילה או לסייע בגיוס חלבוני שותפים בצד הפנימי של התא.
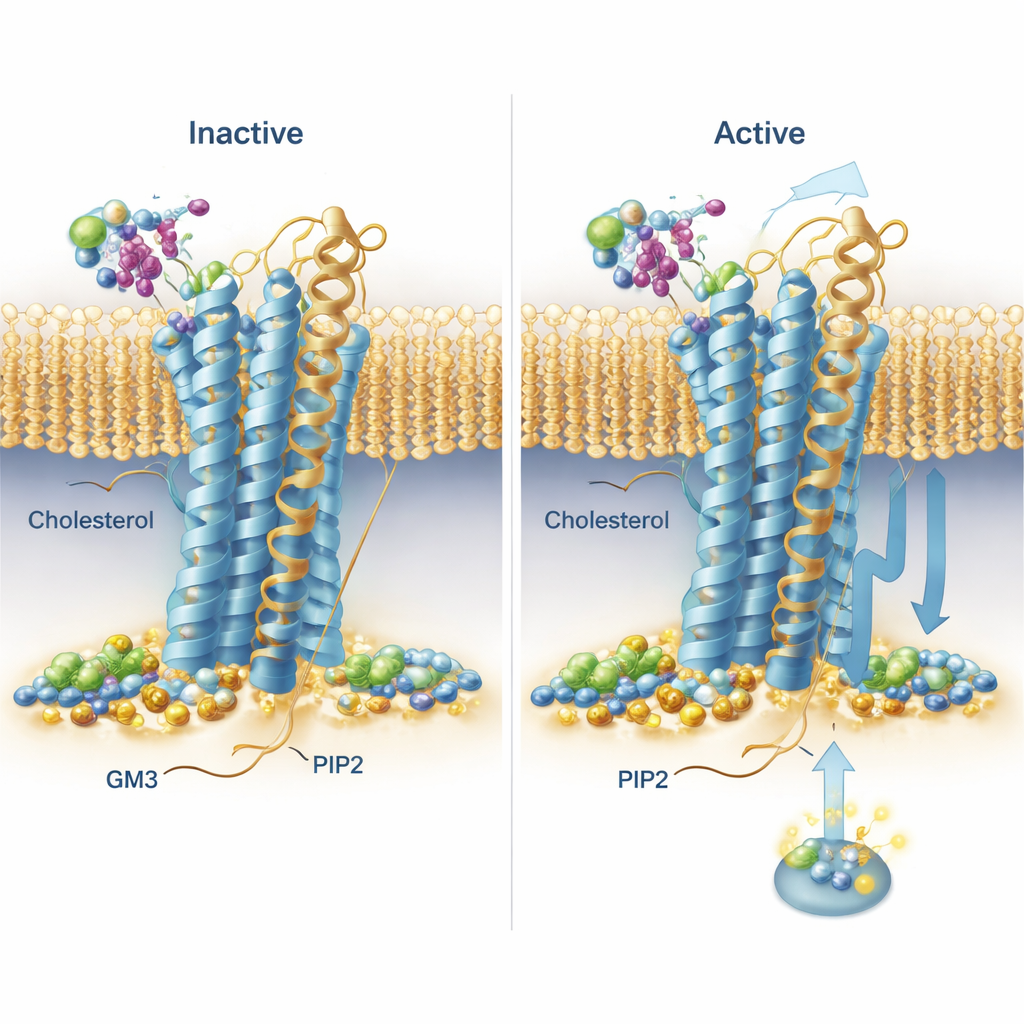
שומן מצופה סוכר שמניב תנועת קלטן
GM3, שומן מורכב בעל ראש סוכר, התקשר ברובו עם הראשים החיצוניים הגדולים של הקולטנים. הצוות הבחין שלחלק מתחומי החוץ של הקולטנים הייתה נדנוד וכיפוף משמעותי יחסית לממברנה, בעוד שאחרים היו יותר מוגבלים. עבור שני קולטנים רלוונטיים לתרופות — GLP‑1R ו‑GIPR — הם בחנו בפירוט את תפקיד GM3. בסימולציות שבהן GM3 היה נוכח, השומן או שנח דרוך בבסיס המתחם החיצוני וחריצי קשירת הליגנד (GLP‑1R) או שהצמיד את עצמו לקצה הרחוק של התחום החיצוני (GIPR), ובשני המקרים השפיע על חופשיות תנועת המרחבים האלה. כדי לבדוק את התחזיות האלה בתאים חיים, החוקרים השתמשו בטכניקה מבוססת אור (TR‑FRET) המדווחת על הקרבה של ראש מסומן של קלטן לממברנה. כאשר הם הפחיתו את רמות GM3 בעזרת מעכב מולקולרי קטן, הם ראו שינויים מדידים באופן שבו ראשים של קולטנים השתנו לאחר גירוי, תואם באופן כללי לרעיון ש‑GM3 מכוון את הגמישות של הקולטנים באופן תלוי קלטן ומצב.
מדוע השותפויות בין שומן לקלטן חשובות
לסיכום, המחקר מצייר את קולטני ה‑B1 לא רק כמפסקי הורמון אלא כחלק מריקוד מתואם בעצבנות עם השומנים שמסביב. כולסטרול יכול לשכון בכיסים חבויים ולהעדיף תוצאות איתות מסוימות, PIP2 יוצר "ידית" פנימית משומרת שעשויה לנעול קולטנים במצב הפעיל ולהנחות חלבוני שותף, ו‑GM3 מכוונן כיצד האזורים החיצוניים של הקולטנים נעים ומפגשים את הליגנדים שלהם. עבור קהל שאינו מומחה, המסר המרכזי הוא שהממברנה היא שכבת בקרה פעילה: הבדלים קטנים בהרכב השומנים יכולים לשנות את אופן פעולת אותו קלטן ברקמות שונות או במצבי מחלה שונים. על ידי מיפוי מפורט של האינטראקציות האלה ושיתוף נתוני הסימולציה הבסיסיים, עבודה זו מניחה יסוד לתכנון תרופות עתידיות שמנצלת או מתרחקת ממגעים שומניים מסוימים, ובכך עלולה להפוך טיפולים לבחירתיים ויעילים יותר.
ציטוט: Chao, K.W., Wong, L., Oqua, A.I. et al. Human class B1 GPCR modulation by plasma membrane lipids. Commun Biol 9, 317 (2026). https://doi.org/10.1038/s42003-025-09445-2
מילות מפתח: קולטנים משפחת G החלבוניים, שומני ממברנה, כולסטרול, PIP2, GM3