Clear Sky Science · he
פענוח ציר הבקרה החיסונית ERS–CAF באמצעות בינה מלאכותית מולטימודלית והערך החיזויי והטיפולי שלו בפאן‑סרטן
מסתכלים על גידולים בלי להשתמש בסקלפל
רופאי סרטן מזהים יותר ויותר כי מה שמקיף את הגידול יכול להיות חשוב לא פחות מהגידול עצמו. אבל דגימה חוזרת של השכונות החבויות הללו באמצעות ביופסיות פולשניות היא מסוכנת ולעתים בלתי מעשית. המחקר הזה מראה כיצד בינה מלאכותית (AI) יכולה לקרוא סריקות רפואיות שגרתיות ותמונות מיקרוסקופיות כדי להסיק על תהליכים חיסוניים וקבריים (דמויי צלקת) שקשה למדוד בתוך הגידולים, ובכך להפוך דימות יומיומי ל"ביופסיה דיגיטלית" שעובדת על סוגי סרטן שונים.
תאי תמיכה חבויים שמעצבים את הסרטן
רבים מהגידולים המוצקים מוקפים במעטפת קשיחה וסיבית שמיוצרת על‑ידי תאי תמיכה מיוחדים הנקראים פיברובלסטים. כאשר תאים אלה נמצאים תחת לחץ בתוך המפעל החלבוני של התא (הרשת האנדופלזמטית), הם מאמצים מצב תוקפני שמסייע לסרטן. בכורדומה, סרטן עצם נדיר, פיברובלסטים לחוצים אלה בונים מטריצה צפופה ועוזרים להרחיק תאי חיסון, מה שהופך טיפולים לפחות יעילים. סביבות פיברוטיות ודלות חיסון דומות מופיעות גם בסרטן הלבלב ושל המעי הגס, מה שמרמז שהביולוגיה הזו אינה ייחודית למחלה אחת. האתגר הוא שהשיטות הנוכחיות למדידת פיברובלסטים לחוצים ולהתנהגותם החוסמת חיסון מסתמכות על דגימות רקמה ובדיקות מולקולריות מורכבות, שקשות לחזרה ועלולות להחמיץ אזורים חשובים של הגידול.
ללמד את ה‑AI לראות ביולוגיה בלתי נראית
החוקרים שאלו האם סריקות MRI לפני ניתוח ושקופיות פתולוגיות שגרתיות בצביעה H&E מכילות כבר רמזים חזותיים על חוצץ החיסון שנגרם מפיברובלסטים לחוצים אלה. הם יצרו שלושה "ציוני ייחוס" מספריים מתוך רצפי RNA של הגידול: ציון אחד הקולט עד כמה פעיל תכנית הלחץ בפיברובלסטים, ציון שמסכם עד כמה נראה כי תאים אלה משדרים אותות לתאי חיסון, וציון שמתאר עד כמה מגוונת אוכלוסיות תאי התמיכה והחיסון שסביב הגידול. במקום לחזות אלפי גנים, ה‑AI הוכשר לחזות רק את שלושת הציונים הביולוגיים המשמעותיים האלה מתוך תמונות בלבד. לשם כך שילבו הצוות שני ענפים: ענף שמנתח מרקם וצורת MRI, וענף שסורק אלפי אזורים קטנים בשקופית הדיגיטלית ומשתמש במנגנון תשומת לב מונחה שפה כדי למקד אזורים שמתאימים לתיאורים מומחים של רקמה פיברוטית ודלה בחיסון.
מיזוג סריקות ושקופיות לאותות חזקים יותר
ב‑126 חולים בכורדומה עם MRI תואם, שקופיות פתולוגיה, נתוני RNA ומידע מעקב, מודל ה‑AI הממוזג עלה על מודלים שהשתמשו רק ב‑MRI או רק בשקופיות. הניבויים שלו לשלושת הציונים המולקולריים התאימו בקירוב למדידות המבוססות RNA ונשארו מכויילים היטב בין בתי חולים וסורקים שונים. כאשר פתולוגים סומנו באופן עצמאי אזורים פיברוטיים ומנוצלים מחיסון, "נקודות החום" של ה‑AI נטו להידלק באותם אזורים, מה שמרמז שהוא עקב אחר ביולוגיה ממשית ולא רק אחרי גודל הגידול. המודל גם קלט היבטים של פרוגנוזה: ציון לחוץ‑פיברובלסט ותוצאת אותות גבוהה יותר קשורים להישרדות גרועה יותר, בעוד שמגוון מיקרו‑הסביבה גבוה ניבא הגנה חלקית. הוספת ציוני ה‑AI האלו לגורמים קליניים שגרתיים שיפרה את היכולת להפריד בין מטופלים בסיכון גבוה ונמוך לאורך זמן.
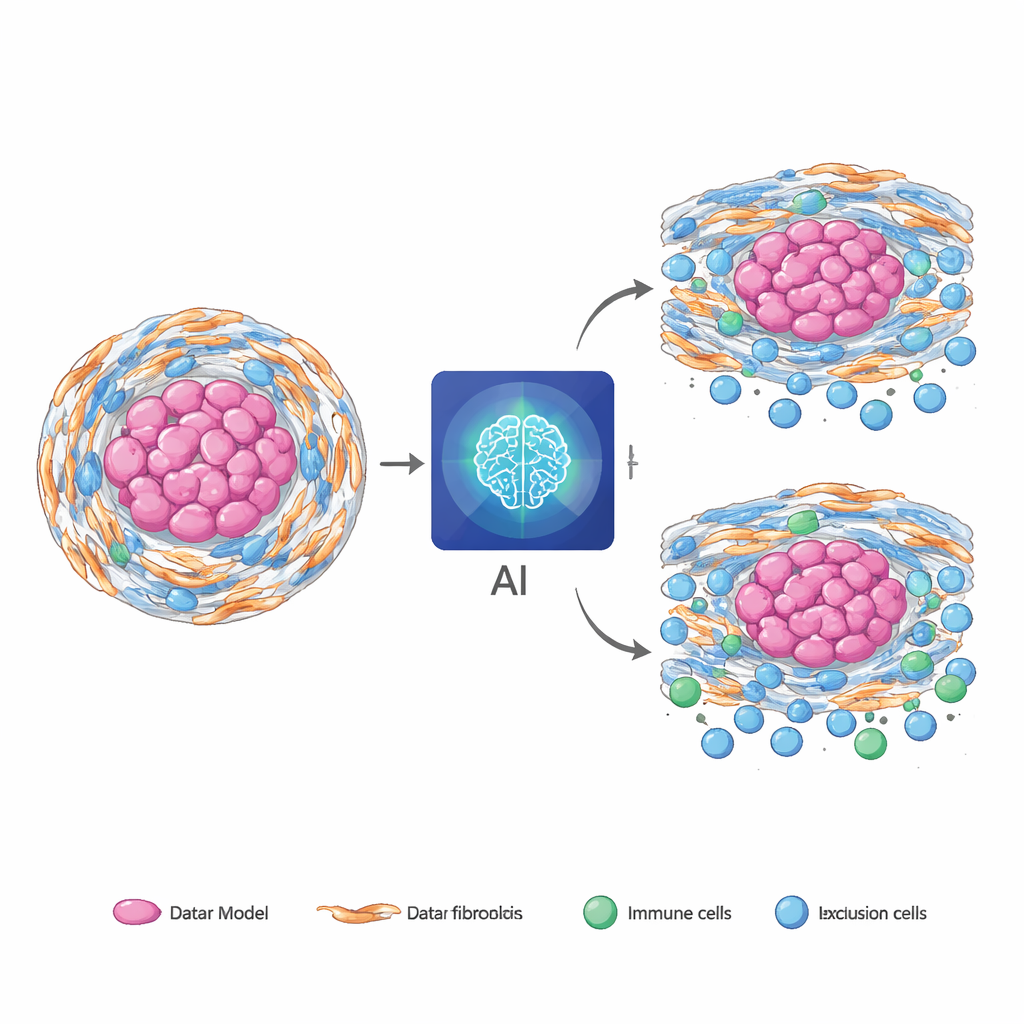
מגידולים נדירים לסרטן נפוץ
מבחן מפתח היה האם מודל שאומן כולו על כורדומה יוכל לשמש "כמו שהוא" בסוגי סרטן אחרים ושכיחים יותר. כאשר יושם ללא אימון חוזר על גידולי לבלב, קיבה ומעי גס ממאגרי נתונים ציבוריים גדולים, גרסת המודל שהסתמכה רק על שקופיות עדיין הראתה התאמה משמעותית בין ניבוי מבוסס תמונה לציוני RNA שחושבו מחדש. בחלק מהמקרים של סרטן אלה ציוני ה‑AI שיפרו את ניבוי ההישרדות מעבר למידע הקליני הסטנדרטי ועזרו להבחין אילו מטופלים סביר שיצליחו יותר בכימותרפיה. כדי להקל על פריסת הגישה במקומות בהם פתולוגיה דיגיטלית מוגבלת, הצוות זיקק את המודל המולטימודלי המלא לגרסת MRI‑בלבד ששמרה על רוב כוח הניבוי תוך ריצה מהירה יותר וצריכת משאבים נמוכה יותר.
מה זה עשוי להציע למטופלים
במבט כולל, התוצאות תומכות ברעיון שתמונות רפואיות שגרתיות מצפנות שקטה מידע על תאי תמיכה לחוצים, הוצאה חיסונית ומגוון מיקרו‑הסביבה—תכונות שבדרך כלל דורשות בדיקות מולקולריות יקרות. בעוד שהעבודה הנוכחית היא רטרוספקטיבית ודורשת אימות פרוספקטיבי, היא מצביעה על עתיד שבו סריקה ושקופית סטנדרטיות יכולות בצורה לא פולשנית לזהות גידולים עם חוצץ חיסון פיברוטי עוין, להנחות אילו מטופלים עשויים להפיק תועלת מבדיקות נוספות או מטיפולים מותאמים, ולבצע זאת על פני סוגי סרטן מרובים ללא עלות נוספת על המטופלים.
ציטוט: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
מילות מפתח: מיקרו‑סביבה גידולית, דימות סרטן, בינה מלאכותית, פיברובלסטים, אימונותרפיה