Clear Sky Science · he
יישום ועתיד הבינה המלאכותית בדימות אבחוני של סרטן הערמונית
מדוע סריקות חכמות חשובות לבריאות הגבר
סרטן הערמונית הוא אחד הסרטנים השכיחים ביותר בגברים, ואיתורו המוקדם יכול להוות את ההבדל בין בעיית בריאות נזילה למחלה מסכנת חיים. סקירה זו מסבירה כיצד הבינה המלאכותית (AI) משתלבת בסריקות רפואיות מודרניות כדי לזהות סרטן הערמונית מוקדם יותר, להעריך עד כמה הוא מסוכן, ולעקוב אחר יעילות הטיפולים. עבור הקוראים היא מציעה חלון אל הדרך שבה מחשבים הופכים לשותפים שקטים בחדר הקריאה, מסייעים לרופאים לקבל החלטות מהירות ועקביות יותר ובו בזמן מעוררים שאלות חדשות על נתונים, הוגנות ואמון.
מצילומים מטושטשים לתמונות עשירות בנתונים
רופאים מסתמכים על כמה כלים דימותיים לחיפוש סרטן הערמונית. אולטרסאונד הוא מהיר וזול אך מתקשה להפריד בין סרטן להגדלה או דלקת חסרי חשיבות. הדמיית תהודה מגנטית (MRI) מספקת תצוגות מפורטות של רקמות רכות והיא כיום הבדיקה המועדפת לאיתור סרטן ערמונית בעל משמעות קלינית, אך פענוחה אורך זמן ואף מומחים לעתים קרובות מחליפים על דעותיהם. סריקות PET/CT, המשתמשות במרקרים שנקשרים לחלבון הנקרא PSMA על תאי הסרטן, מצטיינות בגילוי פיזור לעצמות ובלוטות לימפה אך עלולות לפספס מוקדים זעירים והן יקרות. ה‑AI אינו מחליף את המכונות האלה; במקום זאת הוא מתיישב מעל התמונות שהן מייצרות. האלגוריתמים מנקים ומקטעים תחילה את הסריקות, ואז מחלץ דפוסים עדינים בעוצמה, במרקם ובצורה. הקווים הבלתי נראים הללו, בשילוב עם תוצאות מעבדתיות כמו רמות PSA בדם, משמשים לאימון מודלים שיכולים לסמן אזורים חשודים, לאמוד סיכון לסרטן ולהציע היכן לבצע ביופסיה או כיצד להעריך תגובת טיפול.
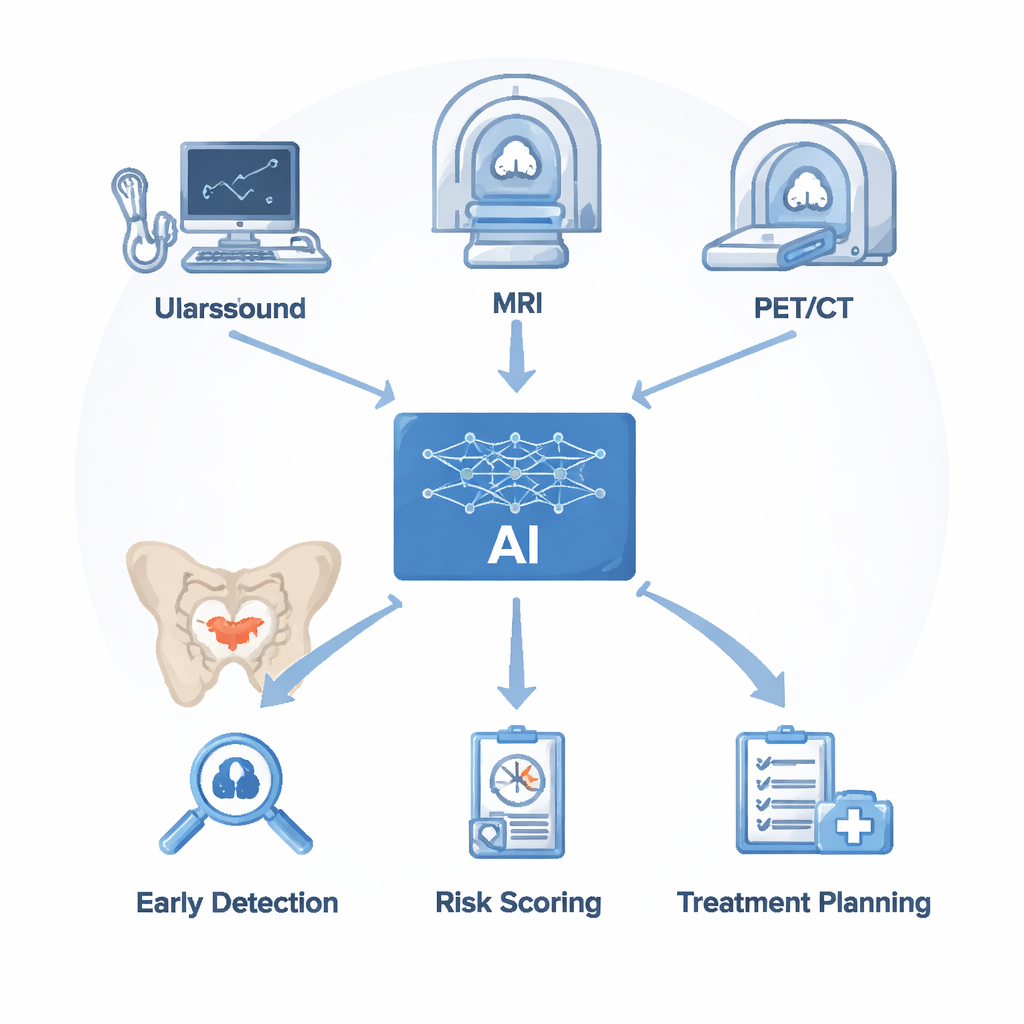
מלמדים את המחשבים לראות את מה שרדיולוגים מפספסים
באולטרסאונד מערכות AI לומדות ממאות דוגמאות לזהות אזורים סרטניים שעשויים להשתלב ברקע. מודלים של למידה עמוקה יכולים לאתר באופן אוטומטי את הערמונית ולהדגיש גידולים סבירים בזמן אמת, לעתים תואמים או עולים על סונוגרפיסטים מנוסים תוך שמירה על מהירות והפחתת פיספוס גשרות קטנות. גישות רדיוֹמיקה עושות צעד נוסף, וממירות תמונות אולטרסאונד לערכות גדולות של מספרים המתארים דפוסי רקמה שמורכבים מדי לעין האנושית. מודלי למידת מכונה הבנויים על תכונות אלה הציגו ביצועים טובים בהרבה משיטת האולטרסאונד המסורתית וה‑PSA לבדו, במיוחד אצל גברים שרמות ה‑PSA שלהם נמצאות באזור ה״אפור״ המבלבל, שבו שיטות ישנות מדווחות לעתים קרובות על שגיאות בכמעט חצי המקרים. רעיונות דומים מניעים AI ב‑MRI, שבו רשתות מתקדמות משרטטות אוטומטית את הערמונית ואת האזורים הפנימיים שלה, ומקטינות את הצורך בקונטור ידני מ‑כ־20 דקות לפחות לדקה בודדת ומשפרות משמעותית את ההסכמה בין קוראים שונים.
הערכות סיכון חדות יותר ומעקב טיפולי חכם יותר
ה‑AI זוהר במיוחד כשהוא משלב מידע ממספר רצפי MRI המראים אנטומיה, תזוזת מים וזרימת דם. מודלים מבוססי Transformer, שהותאמו מעיבוד שפה, מאחדים קלטים אלה כדי ליצור מפות הסתברות של גידולים בעלי חשיבות קלינית. בבדיקות על קבוצות חולים גדולות, מערכות כאלה התאימו או עלו על רדיולוגים בכירים, במיוחד לגבי גידולים קטנים מתחת לסנטימטר שבני אדם נוטים לפספס. ב‑dynamic contrast MRI, מודלים של סדרות זמן מסוגלים לקרוא את עקומות השינוי בעוצמה של הצבע המוזרק כדי להעריך כמה נושרות כלי הדם של הגידול — מדד המקושר למחלה אגרסיבית יותר וסיכוי גבוה יותר לשכיחה חוזרת. ב‑PSMA PET/CT, רשתות תלת־ממדיות מאומנות על סריקות גוף מלא מזהות אוטומטית גרורות בעצמות ובבלוטות לימפה, מודדות את העומס הסרטני הכולל ומקשרות אותו לאורך הזמן ללא התקדמות המחלה. כלים אחרים של AI משווים סריקות שנלקחו לפני ובמהלך טיפול הורמונלי או כימותרפי, וצופים תוצאות טיפול של מספר חודשים מוקדם בהרבה מכללים מסורתיים המבוססים על שינויים פשוטים בקליטה.
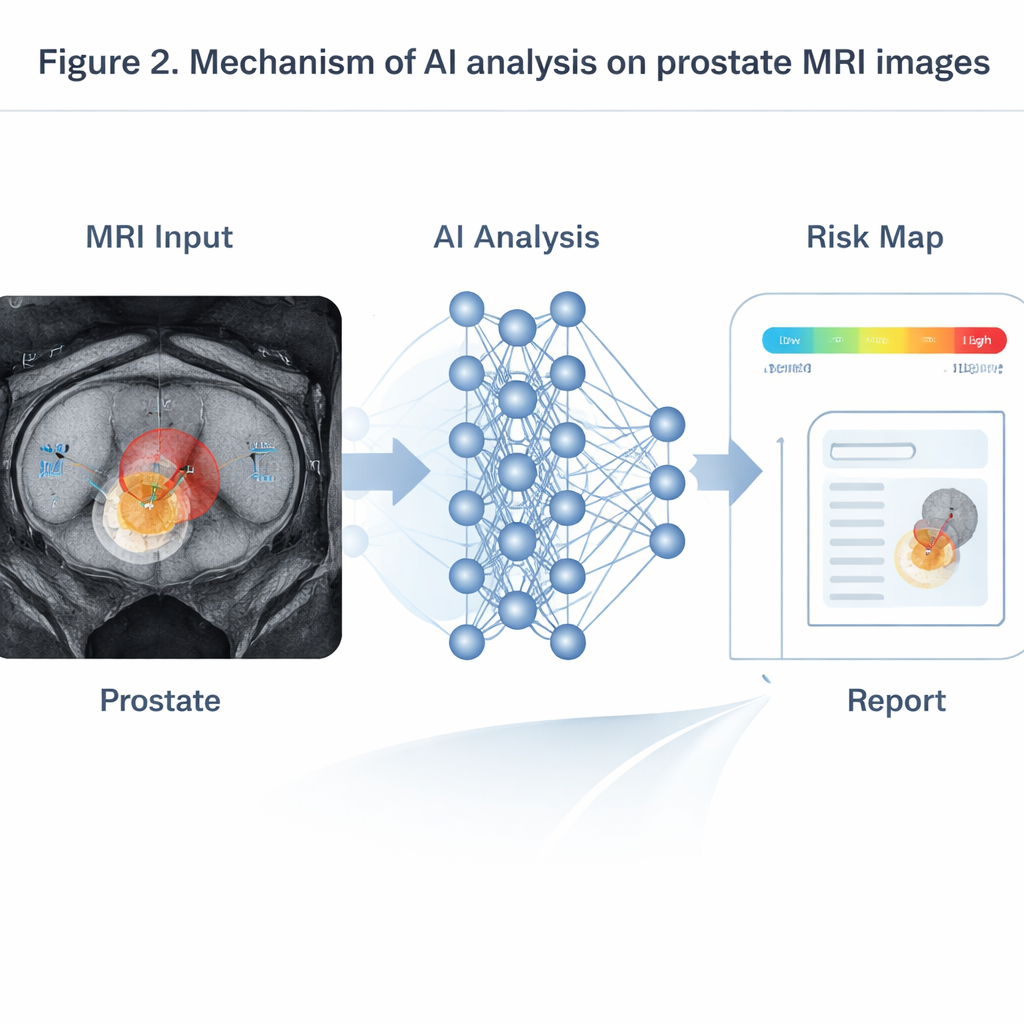
מכשולים: פערי נתונים, קופסאות שחורות ושימוש הוגן
למרות ההישגים הללו, פריסה בעולם האמיתי נתקעת במכשולים משמעותיים. נתוני דימות באיכות גבוהה ומסומנים היטב עדיין מוגבלים ומוטים כלפי בתי חולים אקדמיים גדולים, בעוד שסורקים ממרכזים קטנים ואוכלוסיות מגוונות מיוצגים פחות. הבדלים עדינים בין מותגי סורק, הגדרות ואיכות תמונה יכולים לגרום למודלים שאומנו במקום אחד להיתקל בקשיים במקום אחר. מערכות AI רבות עוצמתיות פועלות כ״קופסאות שחורות״, ומציעות ניקוד סיכון ללא הסבר ברור, מה שמערער את אמון הרופאים — במיוחד כשהמחשב מסתייג מניסיון קליני. הסקירה גם מעלה דאגות לגבי פרטיות, הגבלות שיתוף נתונים והסיכון שמודלים יעבדו פחות טוב לקבוצות מסוימות, ובכך יאריכו פערים בריאותיים אם לא יישמרו מעקב ותיקון בקפדנות.
לבנות שותפים אמינים במרפאה
מבט לעתיד: המחברים מתארים את ה‑AI כחבר צוות מהימן במקום אורקל מסתורי. הם מפרטים מאמצים לבניית מאגרי נתונים גדולים ומשותפים בבתי חולים תוך שמירה על פרטיות באמצעות טכניקות כמו federated learning, שבהן מחליפים עדכוני מודל בלבד — לא נתוני מטופלים גולמיים. כלים חדשים של "AI להסבר" שואפים להציג אילו אזורי תמונה הניעו החלטה ולחברם לפתולוגיה ידועה, מה שמעניק לרופאים סיבות מוחשיות להסכים או להתנגד. במקום מודלים בגישה אחידה, מערכות ממוקדות יתמקדו במשימות ספציפיות: סינון במרפאות עמוסות, הנחיית ביופסיות, מעקב טיפול או פוסט־מעקב למטופלים בסיכון גבוה. שילוב דימות עם נתונים גנטיים וקליניים יכול לחדד עוד יותר פרוגנוזה ולהתאים טיפולים אישית. עבור המטופלים, המסקנה מעודדת: אם אתגרים טכניים, אתיים ורגולטוריים אלה יטופלו היטב, דימות משופר בידי AI עשוי להביא לגילוי מוקדם יותר, פחות ביופסיות מיותרות, תשובות מהירות יותר ותוכניות טיפול מותאמות יותר לסרטן הערמונית.
ציטוט: Wang, X., Zhong, S., Fang, K. et al. Application and prospect of artificial intelligence in diagnostic imaging of prostate cancer. npj Digit. Med. 9, 168 (2026). https://doi.org/10.1038/s41746-026-02354-6
מילות מפתח: דימות סרטן הערמונית, בינה מלאכותית, MRI ואולטרסאונד, PSMA PET/CT, רדִיוֹמִיקָה