Clear Sky Science · he
מיזוג מולטימודלי של מודלים בסיסיים לפתולוגיה ורדיולוגיה לסיווג תת-סוגי גליאומה לפי WHO 2021
השמטת שתי נקודות מבט על גידולי המוח יחד
כאשר מאבחנים אדם עם גידול מוחי, הרופאים צריכים לדעת לא רק שקיים גידול, אלא גם מהו בדיוק סוגו. סוגי גידולים שונים מגיבים מאוד שונה לניתוח, לקרינה ולתרופות. כיום, סיווג מפורט זה בדרך כלל דורש בדיקות גנטיות שיכולות להיות איטיות, יקרות ולא זמינות בכל מקום. המחקר בודק האם מערכת מחשב מתוחכמת שמנתחת גם סריקות מוח וגם תמונות מיקרוסקופיות של רקמת הגידול יכולה להסיק באופן אמין את תת-הסוגים הללו, ובכך למהר ולהרחיב את הגישה לטיפול מדויק.
מדוע סוג הגידול חשוב
גליומות דיפוזיות במבוגרים הן בין סוגי סרטן המוח הקטלניים ביותר, אך לעתים קרובות נראות דומות בסריקות סטנדרטיות ותחת המיקרוסקופ. ההנחיות המודרניות מקבצות אותן לשלושה תת-סוגים גנטיים השונים מאוד באגרסיביות ובתוחלת החיים של המטופלים. הסטנדרט הזהב הנוכחי להבחנה בין תת-הסוגים מבוסס על בדיקות מולקולריות של DNA הגידול. בדיקות אלה דורשות רקמה נוספת, מעבדות מיוחדות והמתנה של ימים עד שבועות לתוצאות. המחברים שואלים האם MRI שגרתיים ופרוסות פתולוגיות דיגיטליות שנאספות ברוטינה יכולים להיות משולבים כדי לחלץ מספיק מידע שיחליף חלק מהבדיקות הגנטיות הללו.
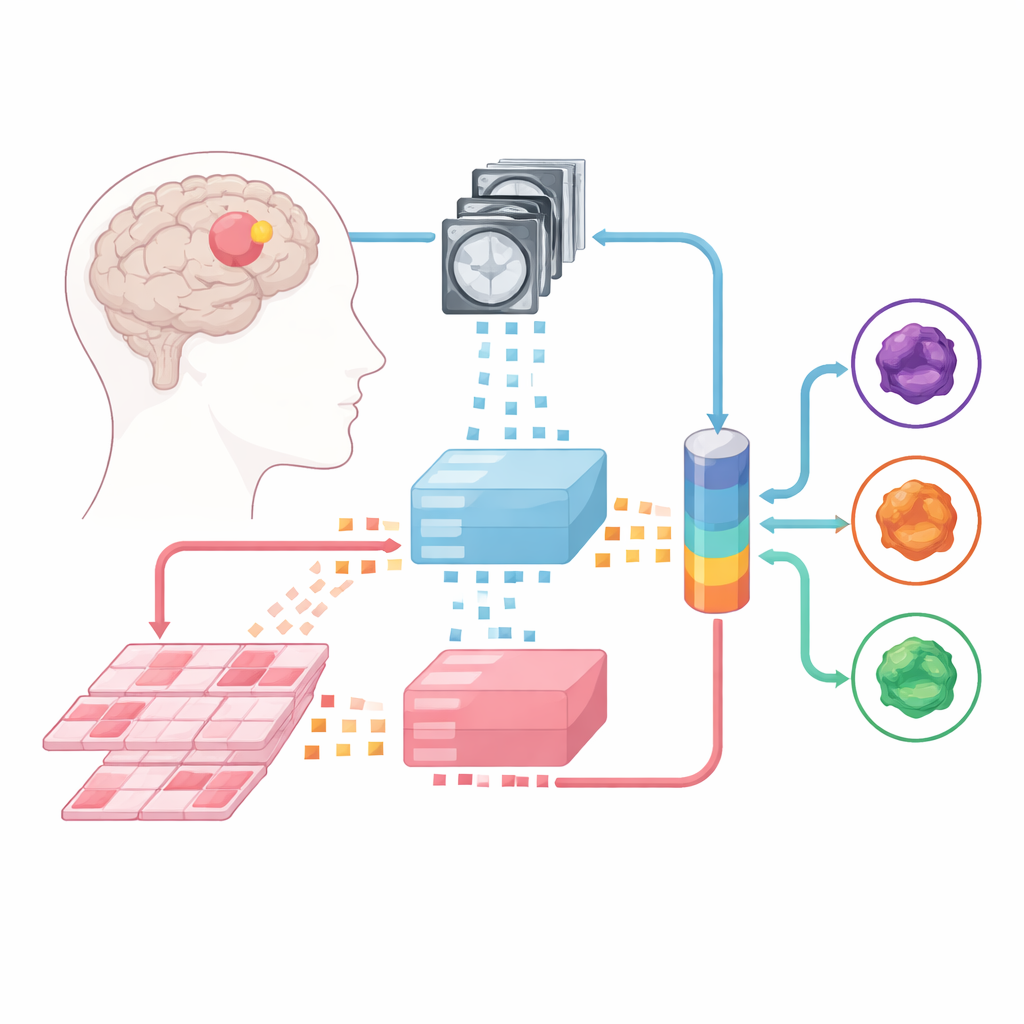
להדריך מכונות לקרוא סריקות ופרוסות
הצוות בנה על מודלים בסיסיים גדולים — מנתחי תמונה רבי-עוצמה שאומנו מראש על אוספים ענקיים של תמונות רפואיות. מודל אחד מעבד MRI מרובי-פרמטרים, ואחר מטפל בפרוסות פתולוגיות ברזולוציה גבוהה של רקמת הגידול. כל מקרה מחולק למקטעי תמונה קטנים, שהמודלים הבסיסיים ממירים לטביעות אצבע מספריות. מעל ה"מומחים" הסטטיים האלה, החוקרים אימנו שלושה סוגי מודלים למיזוג שלמדו לשלב מידע מ־MRI ומהפתולוגיה: ארכיטקטורת מיזוג מאוחרת, עיצוב מיזוג מוקדם, וארכיטקטורת תערובת־מומחים גמישה שיכולה להחליט דינמית כמה להסתמך על כל מקור.
למזג מודליות בלי התאמת מטופלים
מכשול מעשי לשיטות מולטימודליות כאלה הוא שבבתי חולים לעתים רחוקות קיימים אוספי נתונים גדולים שבהם לכל מטופל יש גם MRI וגם תמונות פתולוגיות זוגיות ומסודרות. במקום להסתמך על נתונים התאמתיים מושלמים, המחברים אספו מאגרים נפרדים: מאות מקרי MRI ממספר מרכזים ומאות מקרי פתולוגיה ממשאב אחר, ועוד קבוצה קטנה של 171 מטופלים מפרויקט סרטן ציבורי שהיו להם שניהם. במהלך האימון הם לעתים קרובות שילבו MRI של אדם אחד עם פרוסת פתולוגיה של אדם אחר, כל עוד הגידולים שייכים לאותו תת-סוג. להפתעתם, מודלים שאומנו על נתונים "לא זוגיים" כאלה עבדו באותה מידה כמו אלה שאומנו על זוגות אמיתיים, ובהירותם הייתה טובה יותר מאשר ממוצע פשוט של שני מודלים חד-ממדיים נפרדים.
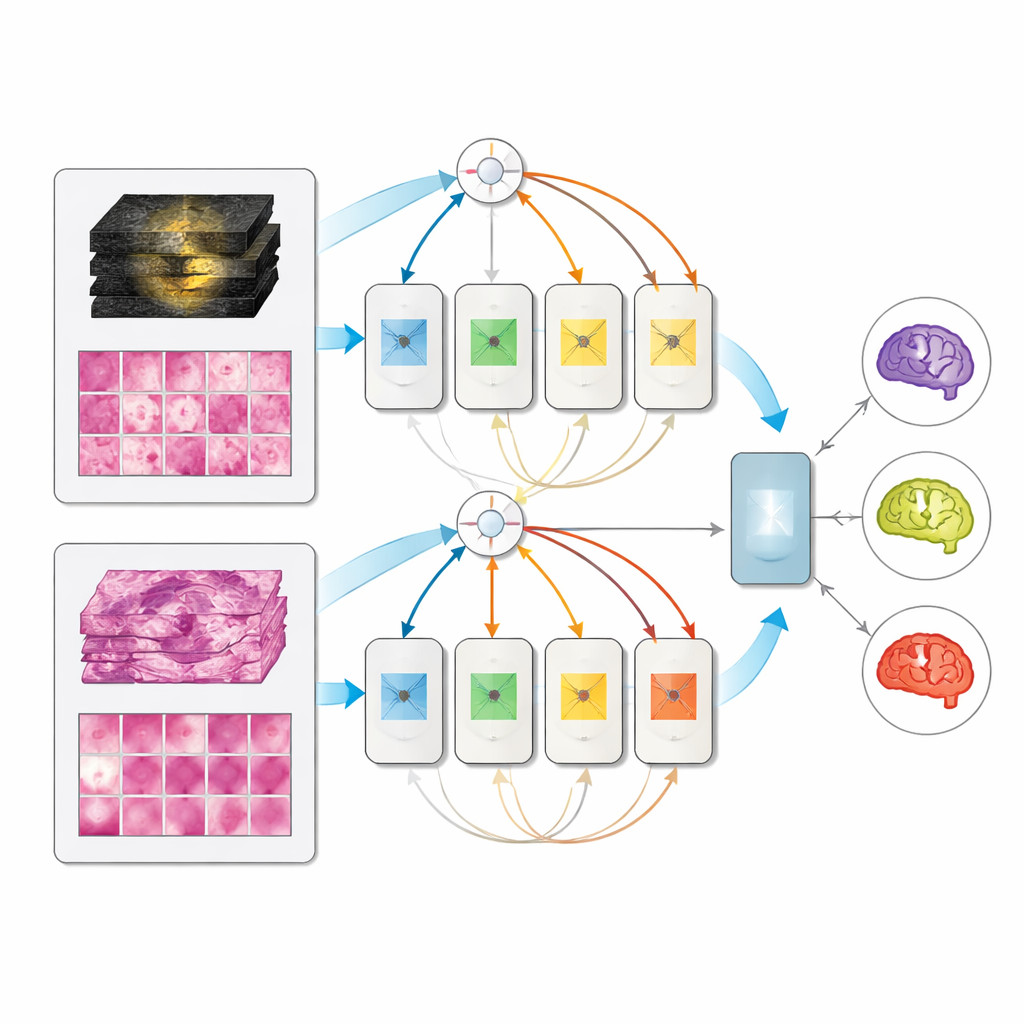
מודל אחד שמסתגל למה שקיים
בקבוצת המבחן המוחזקת של 171 מטופלים מאופיינים במלואם, כל המודלים המולטימודליים גברו על מקביליהם החד־כניסתיים, וארכיטקטורת תערובת־המומחים הציגה את הביצועים הטובים ביותר, והגיעה לציונים גבוהים מאוד בהבחנה בין שלושת תת-הסוגים. בולט שאם ניתנה במבחן רק MRI או רק פתולוגיה, המודל המולטימודלי לא קרס; הוא ביצע כראוי במידה דומה למודלים ייעודיים חד־מודאליים. משמעות הדבר היא שמתקן קליני יכול לפרוס מערכת מאוחדת אחת שמשתמשת במה שיש — סריקות לפני ניתוח בלבד, רקמה לאחר ניתוח בלבד, או שניהם יחד — במקום לתחזק כלים נפרדים לכל תרחיש.
לראות מה המודל רואה
כדי לבנות אמון בהחלטות המערכת, החוקרים בדקו היכן המודל "מביט" ואילו תכונות תמונה חשובות ביותר. מפות תשומת הלב הראו שהמודל המשותף מפזר את המוקד שלו באופן רחב יותר על פני הגידול וסביבתו, הן ב־MRI והן בפרוסות הרקמה, ושמיקוד יותר מפוזר נוטה ללכת יחד עם תחזיות תקינות. ניתוח עמוק יותר של התכונות הנלמדות חשף דפוסים שתואמים רמזים רפואיים ידועים: למשל, תכונות MRI המדגישות ליבות גידול עם הגברה בקונטרסט ומרחבי נוזל מעוותים סייעו להפריד גידולים אגרסיביים יותר, בעוד שתכונות רקמה שתפסו צורות ותבניות תאים קלאסיות סייעו לזהות תת-סוגים מסוימים של גליאומה. גם פערים מעניינים עלו: המודל לא קידד בחוזקה כמה סימנים סטנדרטיים של הגידולים האגרסיביים ביותר, מה שתומך ברעיון שהוא לעתים קרובות מתייחס לקבוצה זו כ"ברירת מחדל" אלא אם יש ראיות חזקות לתת־סוג נוח יותר.
מה הדבר עלול להעניק למטופלים
במונחים פשוטים, עבודה זו מראה שמערכת בינה מלאכותית שמשלבת סריקות מוח ותמונות מיקרוסקופיות יכולה לסווג גידולי מוח בדיוק רב יותר מאשר מערכות שמתבוננות בסוג תמונה אחד בלבד, ושהיא ניתנת לאימון גם כאשר שני סוגי התמונות אינם זמינים מאותם מטופלים. אם יאומתו תוצאות אלה בקבוצות גדולות ומגוונות יותר, כלים כאלה יכולים לסייע לרופאים להעריך תת-סוג גידול מוקדם ורחב יותר, במיוחד במקומות שבהם בדיקות גנטיות מוגבלות. אמנם הם אינם תחליף לבדיקות מולקולריות, אך הם עשויים לשמש כמדריכים מהירים ובעלי עלות נמוכה שמכוונים מנתחים ואונקולוגים לאבחנה הסבירה ביותר ולנתיב הטיפולי המתאים ביותר.
ציטוט: Saueressig, C., Scholz, D., Raffler, P. et al. Multimodal fusion of pathology and radiology foundation models for WHO 2021 glioma subtyping. npj Precis. Onc. 10, 118 (2026). https://doi.org/10.1038/s41698-026-01366-5
מילות מפתח: סיווג תת-סוגי גליאומה, דימות מולטימודלי, בינה מלאכותית, MRI ופתולוגיה, אבחון סרטן המוח