Clear Sky Science · he
תגובת מידוסטאורין ב-AML מעוצבת על ידי מצב תאי פרוגניטור דמוי-שַׁרָשׁ שמותאם באופן ברירתי על ידי חיקויי SMAC
מדוע חלק מתרופות ללוקמיה מפסיקות לפעול
עבור רבים החולים בסוג של סרטן דם הנקרא לוקמיה מיאלואידית חריפה (AML), תרופות מטרה חדשות הביאו תקווה — אך לא כולם נהנים מהן, ולעתים התגובה נחלשת. המחקר הזה שואל שאלה פשוטה אך קריטית: מדוע תאי לוקמיה מסוימים מתעלמים מתרופה נפוצה, מידוסטאורין, והאם אפשר למצוא שילוב חכם שיכריח את התאים העקשניים הללו למות?
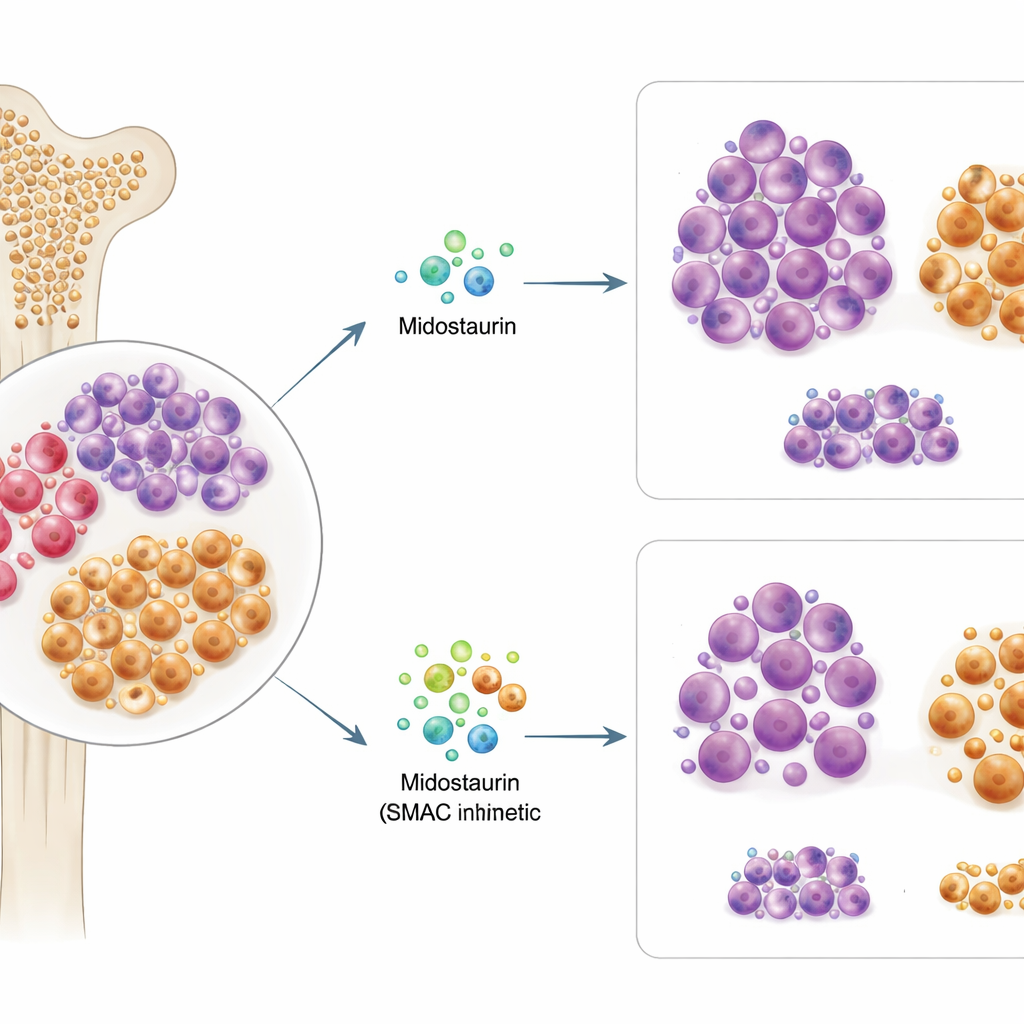
מבט מעבר למוטציה העיקרית
בערך אחד מכל שלושה חולי AML נושא שינוי בגֵּן בשם FLT3, שמניע את צמיחת הלוקמיה וזה הסיבה למתן מידוסטאורין. החוקרים בדקו דגימות מח עצם ודם מ-63 מטופלים עם AML הנושא מוטציית FLT3, וחשפו את התאים במעבדה למידוסטאורין ולמעל 500 תרופות סרטן נוספות. הם מצאו שרגישות התאים של מטופל כלפי מידוסטאורין ex vivo התאמה בקירוב לאופן שבו אותו מטופל הגיב אחר כך במרפאה. במפתיע, סוג המוטציה המדויק ב-FLT3 או עוצמתה לא חזה באופן אמין את הצלחת מידוסטאורין, מה שמרמז שגנטיקה לבדה אינה מסבירה מי יפיק תועלת.
מאגר מוסתר של "תאי זרע" עקשניים
בהעמקה נוספת השווה הצוות דפוסי חלבון ופעילות גנים בין תאים שרגישים למידוסטאורין לאלה שאינם. בדגימות שאינן מגיבות נצפו תכונות של תאים בלתי בוגרים ודמויי-גזע — תאים הקרובים לשורש יצירת הדם וחשודים בכך שהם פועלים כ"זרעים" שיכולים להניע מחדש את הלוקמיה. לעומתם, הדגימות שמגיבות הופיעו דמויות יותר לתאי חיסון ומיאלואידים שחלקית התבגרו. באמצעות שיטות מתקדמות ברמת התא היחיד זיהו המדענים אוכלוסייה מסוימת של תאי לוקמיה שמסומנת על ידי החלבונים המשטחיים CD38 ו-CD45RA והתנהגה כמו אותם פרוגניטורים. לתאים אלה נצפתה ארגון בלתי שגרתי של קרום התא החיצוני, מה שמרמז שהמולקולות הסינגנליות המרכזיות מסודרות בצורה שמקדמת הישרדות.
חיווט הישרדות: מתג של מסלולי איתות
מידוסטאורין נועד לחסום את איתות FLT3, שבמצב רגיל מזין שרשרת סיגנלים הכוללת מולקולה בשם STAT5 ויכולה לקדם גדילה תאית. כאשר הצוות בחן איתות בקווי תאים ודגימות מטופלים לאחר טיפול במידוסטאורין, הם ראו שני דפוסים מובחנים. בתאים הרגישים לפעולה של מידוסטאורין פעילות STAT5 ירדה מהר — תואם לכיבוי יעיל של FLT3. בתאים העמידים, עם זאת, דומיננטי מסלול אחר: PI3K/AKT, מסלול הישרדות קלאסי שעוזר לתאים לעמוד בפני מוות מתוכנת. תאים עמידים אלה שמרו על פעילות AKT או אפילו הגדילו אותה לאחר הטיפול, והראו רמות גבוהות יותר של חלבונים החוסמים אפופטוזה (מוות תאי מתוכנת). במילים אחרות, החיווט הפנימי בתאי הפרוגניטור-דמוי הללו נראה מוסב לטובת הישרדות גם כאשר FLT3 מוחלש.
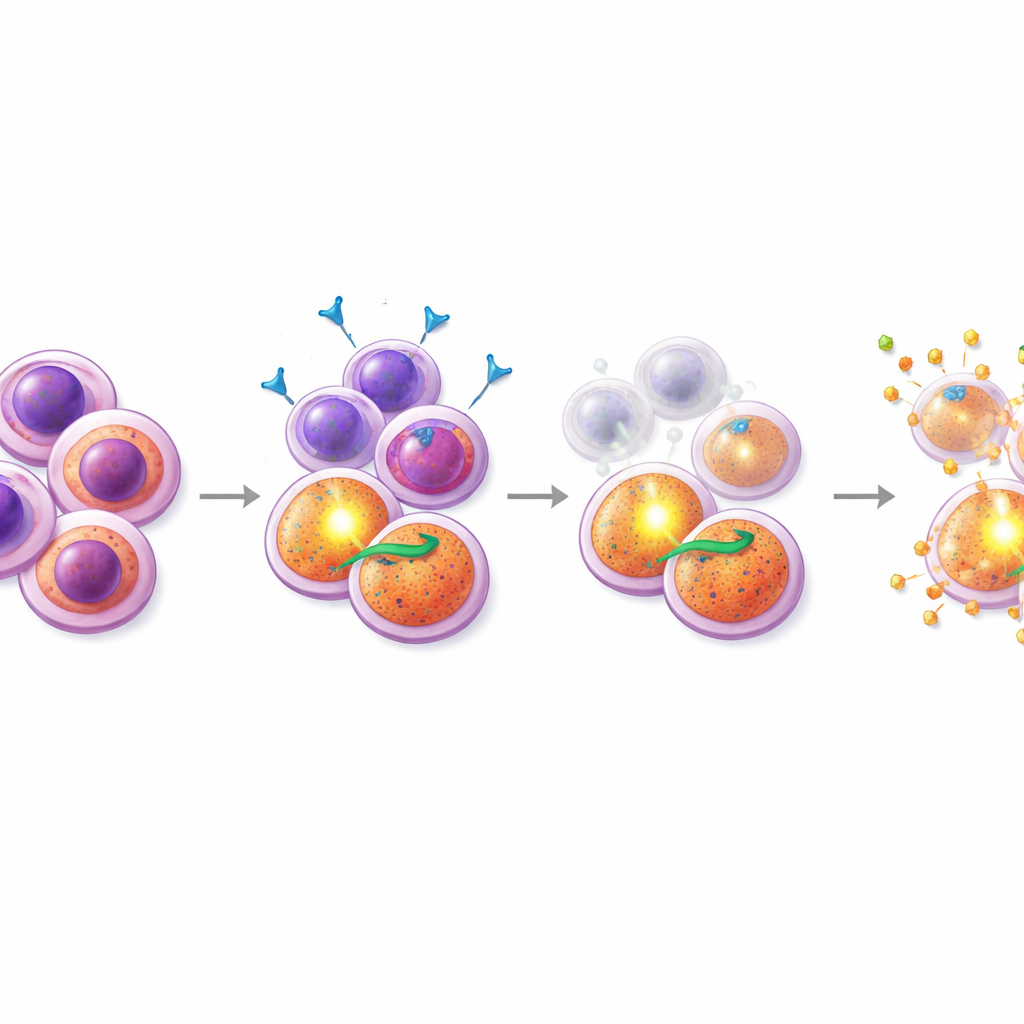
מציאת תרופת שותף שפוגעת בנקודת התורפה
בעזרת התובנה הזו סקרו החוקרים שילובים של מידוסטאורין עם מאות תרכובות נוספות, כשהם מתמקדים בתרופות המשפיעות על מוות תאי. קבוצה אחת בלטה במיוחד — חיקויי SMAC, תרופות המחלישות את החלבונים המעכבים אפופטוזה שעליהם מסתמכים תאים שמונעים על ידי PI3K/AKT. בדגימות של מטופלים עמידים ובקו תאים מוּטַנטי FLT3 עמיד, הוספה של חיקויי SMAC כמו בירינאפן לִמידוסטאורין ייצרה סינרגיה חזקה: יחד, התרופות הרגו הרבה יותר תאים מאשר כל אחת מהן לבד. באופן מכריע, ניסויי ציטומטריה בזרימה מפורטים הראו כי השילוב מידוסטאורין–חיקוי SMAC התרוקן באופן סלקטיבי את האוכלוסייה הפרוגניטור-דמויית CD38+CD45RA+ והוריד את רמות הסמן המשטחי האופייניות שלה, מה שמרמז שטיפול זה מכוון במיוחד ל"זרעים" הקשים להריגה. לעומת זאת, שילובים עם מעכב ה-BCL-2 המאושר ונטוקלקס היו יעילים יותר כנגד תת-אוכלוסייה שונה, עם רמות גבוהות של CD34, ולא הראו את אותו אפקט ממוקד על התאים העמידים.
מה משמעות הדבר עבור המטופלים
מחקר זה מציע שעמידות למידוסטאורין אינה רק עניין של מוטציית FLT3 עצמה, אלא גם של "מצב" תאי הלוקמיה — רמת הבגרות שלהם, ארגון הקרום וסיגנלי ההישרדות המועדפים. תת-אוכלוסיית פרוגניטור-דמוי CD38+CD45RA+ נראית כמאגד מרכזי של עמידות, שמשנה את האיתות מנתיב STAT5 הרגיל לתוכנית הישרדותית מבוססת PI3K/AKT. על ידי שילוב מידוסטאורין עם חיקויי SMAC הצליחו החוקרים להחזיר רגישות לתאים אלה ולהניע אותם למוות תאי במעבדה. אמנם נדרשים מחקרים קליניים נרחבים יותר, הממצאים מצביעים על עתיד שבו רופאים עשויים להשתמש בבדיקות פונקציונליות ובפרופילינג של מצב התא, ולא רק בריצוף DNA, כדי לבחור שילובי טיפול המכוונים הן לגוש הלוקמיה והן ל"הזרעים" העמידים ביותר שלה.
ציטוט: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
מילות מפתח: לוקמיה מיאלואידית חריפה, מעכבי FLT3, עמידות לתרופות, תאי גזע לוקמיים, חיקויי SMAC