Clear Sky Science · he
חיזוי חסרון ברקומבינציה הומולוגית ותשובות לטיפול באמצעות מודל יסוד מבוסס טומוגרפיה ממוחשבת: מחקר פרה‑קליני
מדוע זה חשוב למטופלים ולרופאים
טיפולי סרטן הפוגעים ב‑DNA, כגון סוגים מסוימים של כימותרפיה ותרופות ממוקדות חדשות, יכולים לפעול באופן מרשים בגידולים שמערכות התיקון שלהם כבר פגומות. האתגר הוא לזהות אילו גידולים נושאים חולשות נסתרות אלה בלי להסתמך על ביופסיות פולשניות חוזרות. מחקר זה בוחן האם סריקות שגרתיות בסגנון רפואי בעכברים, כשהן מפוענחות על‑ידי מודל עוצמתי של בינה מלאכותית, יכולות לחשוף עד כמה הגידול פגיע וכיצד הוא יגיב לתרופה ניסיונית חדשה.
נקודת תורפה נסתרת בתאי סרטן
רבים מהגידולים נושאים ליקויים במסלול תיקון DNA מרכזי הנקרא רקומבינציה הומולוגית. כאשר מסלול זה נכשל, התאים צוברים נזקים בחומרת התורשה שלהם, מצב הנקרא חסרון ברקומבינציה הומולוגית, או HRD. HRD עלול להגדיל את הסבירות להיווצרות סרטן, אך גם מהווה עקב אכילס: תרופות המגבירות את נזקי ה‑DNA יכולות להכריע תאים אלה המותשים כבר, ולהשמיד אותם ביעילות רבה יותר מתאים בריאים. כיום זיהוי HRD מסתמך בדרך כלל על בדיקות גנטיות או בדיקות מעבדה מיוחדות היקרות, גז־זמניות ולעתים דורשות לקיחת דגימות מהגידול. המחברים שאלו האם דימות—אותם סריקות X תלת‑ממדיות הנפוצות במרפאות—יכול להציע חלון מהיר, לא פולשני לתוך HRD.
שימוש בסריקות חכמות במקום ביופסיות נוספות
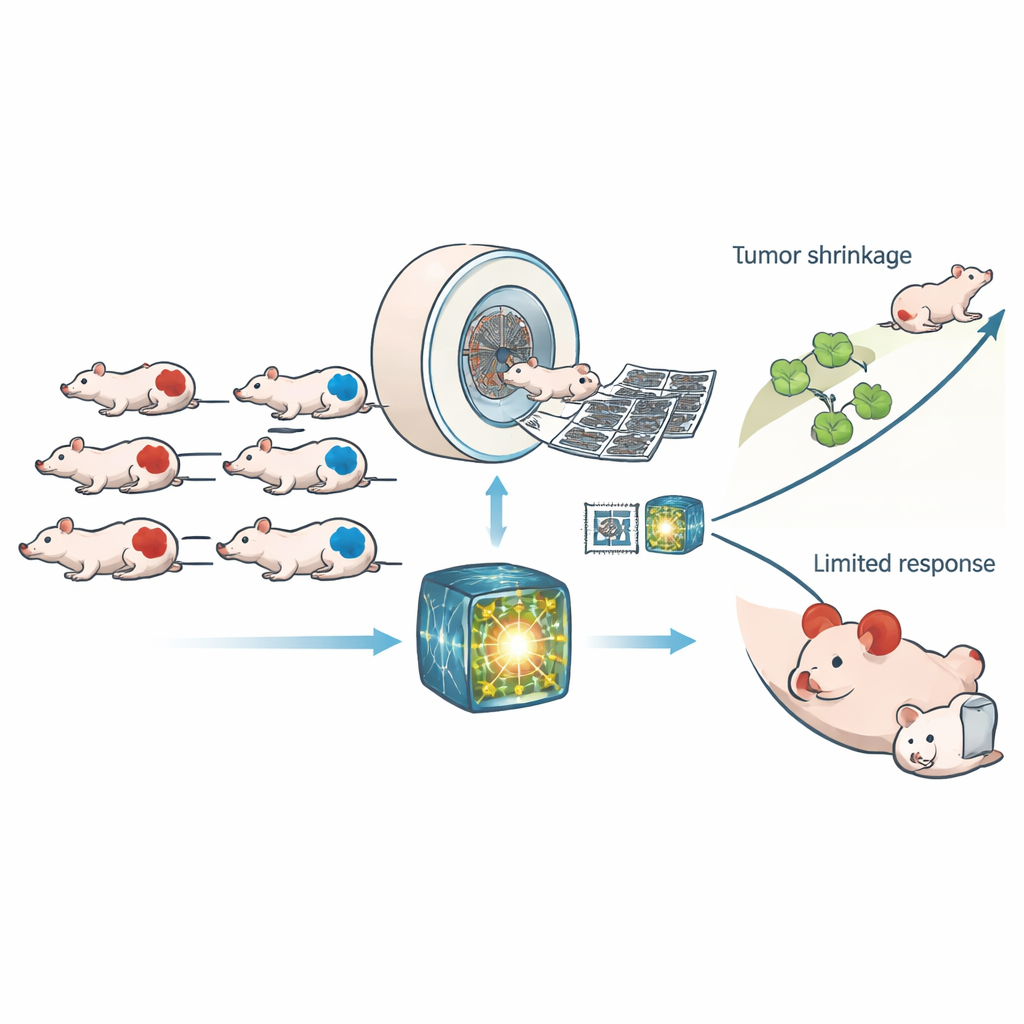
חוקרים עבדו עם 307 עכברים שנשאו השתלות גידול אנושיות שהיו או HRD או תקינות ביכולתם לתקן DNA. כל בעלי החיים עברו סריקות טומוגרפיה ממוחשבת (CT) ברזולוציה גבוהה לפני ואחרי קבלת טיפול בקרה או CP‑506, תרופה ניסיונית שהופכת לפעילה באזורים בעלי חוסר חמצן בגידולים וקושרת בין גדילי ה‑DNA. במקום להסתמך על כמה מדידות תמונה מעשה ידי אדם, הצוות השתמש ב"מודל יסוד" מודרני שאומן על מאגרי CT אנושיים גדולים כדי לחלץ אלפי דפוסים עדינים מכל סריקה. לאחר מכן אומן מסווג פשוט על אותם דפוסים כדי להכריע האם גידול הוא HRD, והמאפיינים הנלמדים שימשו גם לחיזוי כמה נזק ל‑DNA ועיכוב גדילה CP‑506 יגרום.
עד כמה המודל הדימויי עמד במשימה
מודל היסוד ביצע באופן מובהק טוב יותר הן מרדיוֹמיקה קלאסית והן מרשת למידה עמוקה סטנדרטית שאומנה מאפס. בסריקות מבחן חדשות הוא הבחין בין גידולים HRD ל‑non‑HRD עם שטח מתחת לעקומה של כ־0.88, רמת דיוק שתוחזקה תחת הגדרות אנרגיה שונות ב‑CT. כאשר שתי הגישות של ה‑AI הסכימו על סוג הגידול, הביצועים עלו אף יותר. ציון ה‑HRD המבוסס תמונה של המודל תאם בקירבה למעמד הגנטי האמיתי בכמה קווי גידול של הערמונית והמעי הגס, אם כי קו אחד עם התנהגות תיקון יוצאת דופן נותר קשה יותר לסיווג. חשוב לציין שתכונות ה‑CT המקושרות ל‑HRD לא היו רק ארטיפקטים סטטיסטיים: הן גם חזו כמה נזק ממושך ל‑DNA CP‑506 ייצר 48 שעות לאחר הטיפול וכמה זמן לקח לגידולים לשוב ולהגיע לגודל פי ארבעה בניסוי מקביל.
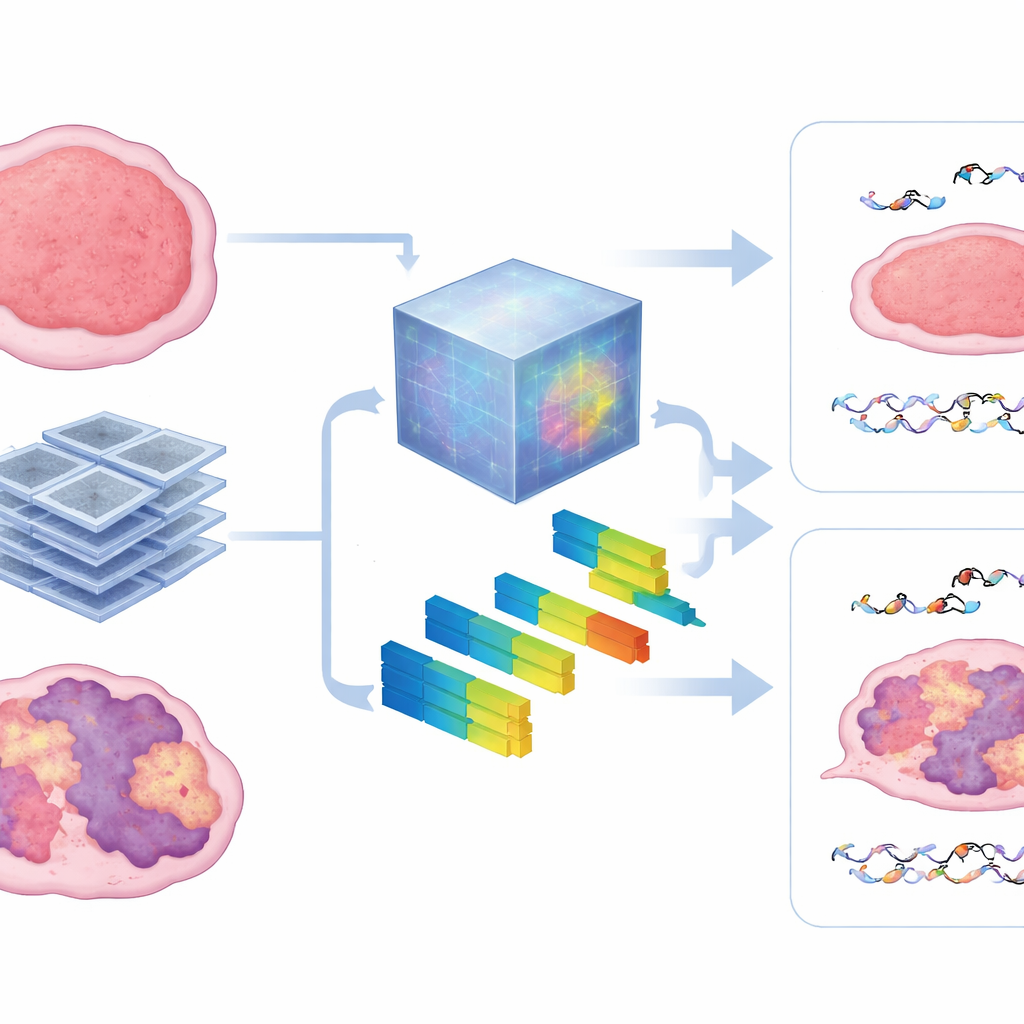
מה הסריקות חושפות בתוך הגידול
כדי להציץ בתוך הקופסה השחורה השוו המחברים את הדפוסים שלמד מודל היסוד לתכונות רדיומיות סטנדרטיות המתארות מרקם ועצמת תמונה. הם מצאו שהמודל הסתמך במידה רבה על מדדי הטרוגניות—כמה הגידול נראה דמוי כתמים, גס או בלתי סדיר ב‑CT. גידולים עם חתימות HRD חזקות הראו נטייה למרקמים פחות מסודרים, ותכונות אלו סייעו לחזות הן נזק מיקרוסקופי ל‑DNA והן שליטה מקרוסקופית בגידול. הגישה נותרה חזקה גם כאשר היו זמינים נתוני אימון מועטים יותר, דבר שמרמז שמודלים מאומנים מראש כאלה יכולים להתגבר על מכשול גדול במחקרים של חיות ניסוי, שבהם קשה לאסוף מאגרי דימות גדולים.
מניסויים בעכבר לטיפול עתידי בחולים
עבודה פרה‑קלינית זו מראה שסריקת CT יחידה, המפורשת דרך בינה מלאכותית עוצמתית ואומנת מראש, יכולה ללכוד אותות של תיקון DNA לקוי ולצפות עד כמה החזק גידול יגיב לתרופה הפוגעת ב‑DNA. עבור קורא שאינו מומחה, המסקנה היא שסורקים שנראים שגרתיים עשויים בקרוב לבצע משימה כפולה—לאתר גידול ולחשוף עד כמה הוא שביר—בלי פרוצדורות נוספות. לפני שזה יהפוך לחלק מהטיפול השגרתי, השיטה חייבת להיבדק ולזכות לאימות בחולים אנושיים. אם מאמצים אלה יצליחו, טביעות אצבע מבוססות CT של HRD יכולות לסייע לרופאים להתאים אנשים במדויק יותר לטיפולים כמו CP‑506 ותרופות קרובות, לשפר תוצאות ולחסוך לאחרים מטיפולים רעילים ובלתי יעילים.
ציטוט: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
מילות מפתח: חסרון ברקומבינציה הומולוגית, דימות של סרטן, רדיוֹמיקה, מודלי יסוד, טיפול המגרה נזקים ב‑DNA