Clear Sky Science · he
פיתוח ואימות של מודל מבוסס בינה מלאכותית לאבחון גידולים אך לא ממאירים, גבוליים וממאירים של האדנקס
מדוע זה חשוב לבריאות נשים
גידולים שחלתיים ואחרים באדנקס הם ממצאים שכיחים בבדיקת אולטרסונוגרפיה של האגן, אך ההבחנה בין אלו שאינם מזיקים לאלו שמעידים על סרטן בשלב מוקדם נותרת מאתגרת, אפילו למומחים. המחקר הזה מדווח על מערכת בינה מלאכותית חדשה בשם Clinical‑OMTA, שמנתחת תמונות אולטרסונוגרפיה ועוזרת לרופאים למיין גידולים אלו לשלוש קטגוריות מרכזיות — שפיר, גבולי וממאיר — כך שנשים יקבלו את הטיפול המתאים וייוחסכו ניתוחים מיותרים.
שלושה סוגי גידולים, שלוש בחירות שונות מאוד
לא כל גידולי האדנקס שווים. גידולים שפירים לעתים ניתנים למעקב או להסרה בניתוח פשוט. גידולים ממאירים הם סרטן מסכן חיים שדורש ניתוח מיוחד וכימותרפיה. גידולים גבוליים נמצאים במצב תווך: הם עלולים להישנות אך נוטים להופיע אצל נשים צעירות שרוצות לשמור על פוריותן, ולכן המנתחים מנסים להסיר רק את הנדרש. לצערנו, באולטרסונוגרפיה שלוש הקטגוריות הללו עשויות להיראות דומות מאוד. במיוחד גידולים גבוליים יכולים לחקות שקים תפקודיים או סרטן אגרסיבי, מה שמקשה על קבלת החלטות וטומן לחץ עבור המטופלות והמטפלים.
להפוך סריקות מורכבות לתשובות ברורות
אולטרסונוגרפיה היא בדרך כלל הבדיקה הראשונה והזמינה ביותר לגידולי אדנקס, אך פענוח תמונות גרעיניות ומשתנות מאוד דורש ניסיון רב. מערכות ניקוד ומחשבי סיכון קיימים, כמו המודל ADNEX הנפוץ, משלבות מאפייני אולטרסונוגרפיה ספציפיים עם מידע קליני פשוט כמו גיל וסמן דם (CA125), אך עדיין נשענות על תיאור מדויק של התמונות על ידי בני אדם. עבודה עדכנית בלמידה עמוקה — ענף של בינה מלאכותית הלומד דפוסים ישירות מהפיקסלים — מציעה אפשרות לעקוף חלק מהסובייקטיביות הזו על ידי אימון מחשבים לזהות חתימות תמונה עדינות של סוגי גידולים שונים.
עוזר בינה מלאכותית שאומן בבתי חולים רבים
בהתבסס על עבודות קודמות, המחברים עיצבו את Clinical‑OMTA, מודל דו‑מסלולי שמפריד תחילה בין גידולים שפירים ללא‑שפירים ואז מבדיל בין גבוליים לממאירים. המערכת מעבדת תמונות אולטרסונוגרפיה בגווני אפור ויכולה גם לקבל כקלט אופציונלי את הגיל וערכי CA125. ללימוד ובדיקה של המודל אספו החוקרים מאגר נתונים גדול ומגוון: 2381 נשים מ‑23 בתי חולים ברחבי סין, סרוקות ב‑38 סוגי מכשירי אולטרא‑סאונד. ברוב המקרים האבחנה אושרה ניתוחית; קבוצה קטנה של ציסטות שנחשבו בבירור לשפירות אושרה במעקב אולטרסונוגרפי של לפחות שישה חודשים. הנתונים חולקו לסטי אימון, ערכות מבחן פנימיות ושתי קבוצות מבחן חיצוניות בלתי תלויות לחלוטין, כולל תמונות סטילס וסריקות וידאו קצרות של השחלות. 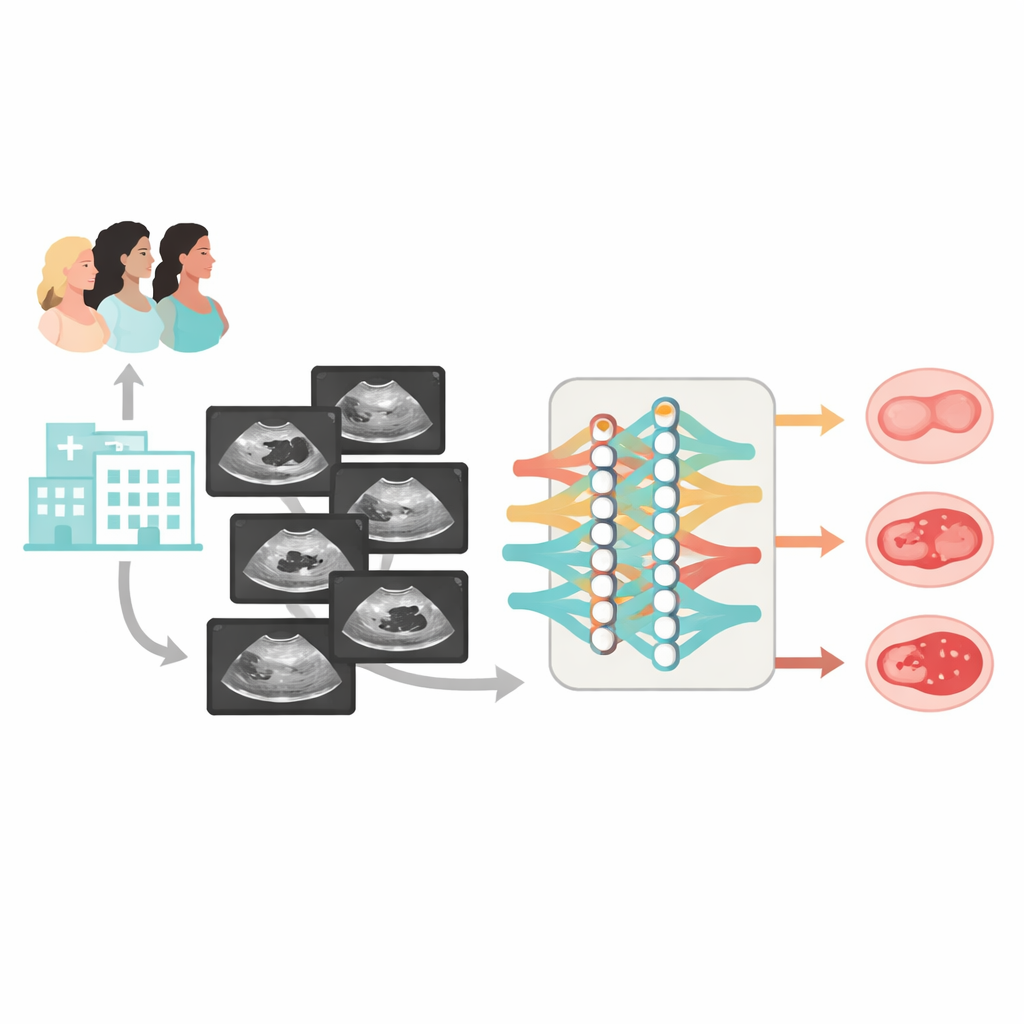
עד כמה הבינה המלאכותית הצליחה בתנאי אמת
בתמונות מבחן חיצוניות, Clinical‑OMTA הפרידה נכון בין גידולים שפירים, גבוליים וממאירים בדיוק דומה לזה של מודל ADNEX ושל שיפוטו של מבצע אולטרסאונד מומחה. ביצועי המודל היו יציבים בין מותגי אולטרסאונד שונים, שיטות סריקה (דרך הבטן או דרך הנרתיק) ושני בתי החולים החיצוניים, מה שמרמז שהמודל לא מותאם ביתר למכשיר או מרכז ספציפי. המערכת עבדה היטב גם בקליפים של וידאו, לא רק בפריימים סטטיים. מעניין שכניסת הגיל וה‑CA125 כמידע נוסף לא שיפרה את החלטות המודל מעבר לשימוש בתמונות בלבד, מה שמשקף ממצאים קודמים שמראים שסמן דם זה מוסיף מעט כאשר זמינות תמונות באיכות גבוהה. 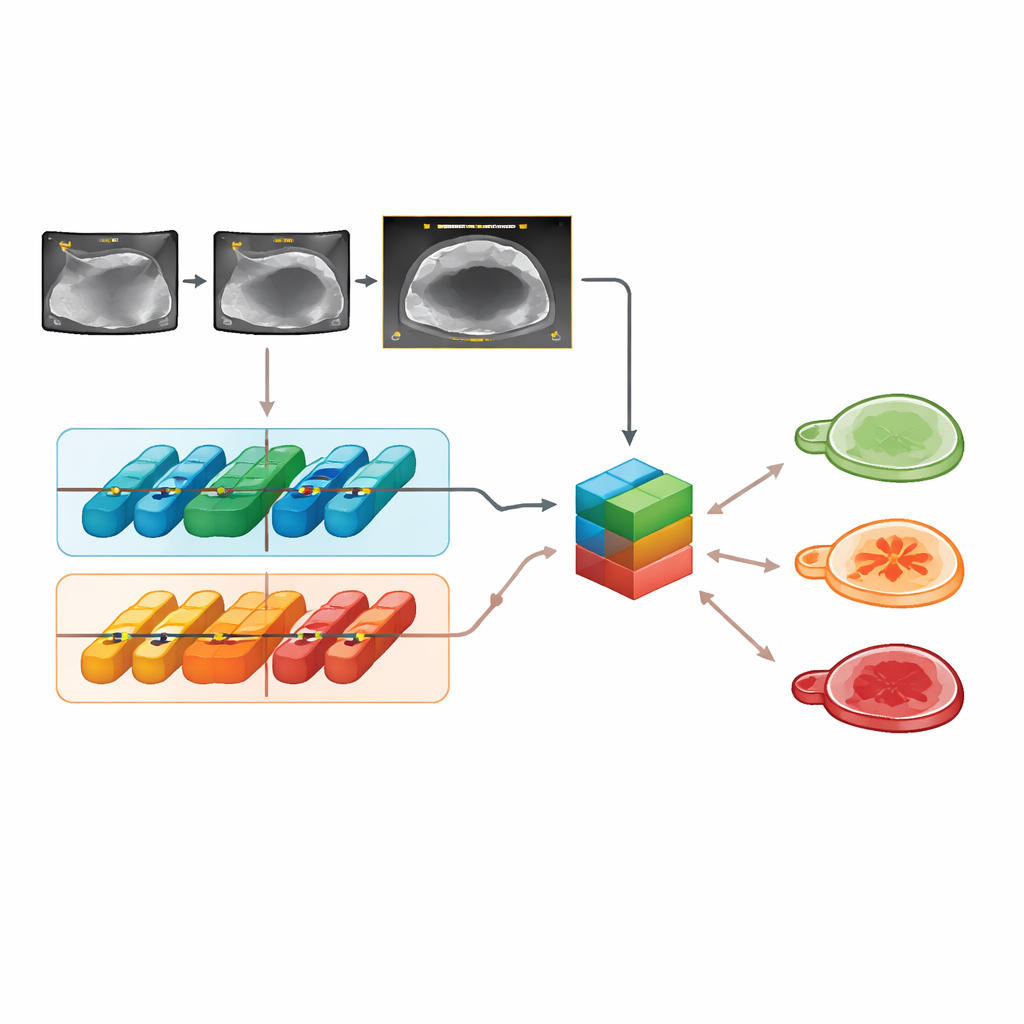
עוזרת לרופאים פחות מנוסים והמגבלות שלה
החוקרים ביקשו מ‑11 רדיולוגים — זוטרים, בינוניים ובעלי ניסיון רב — לסווג את אותם המקרים, תחילה ללא עזרה ואחר כך עם פלט המערכת ומפות חום שמבליטות אזורי תמונה שהמודל רואה כחשובים. בעזרת Clinical‑OMTA דיוקם של רופאים זוטרים זינק בכ־18–20 נקודות אחוז, וכמו כן הקוראים בעלי ניסיון בינוני השתפרו בצורה בולטת והגיעו לביצועים קרובים לאלה של מומחים. ההסכמה בין הקוראים, שאפיינה בעבר מידה של הוגנות עד מתונות, עלתה לרמות גבוהות מאוד כאשר השתמשו בכלי. יחד עם זאת, המחקר מציין כי התאמה חזקה כזו עלולה לשקף "הטיית אוטומציה", שבה קלינאים נשענים יתר על המידה על ה‑AI, במיוחד במקרים הגבוליים המעמעמים ביותר. המחברים מדגישים לכן שמפות החום הן כלי מחקר, לא הסבר עצמאי, וששילוב הנחיית ה‑AI בחינוך הקליני וקבלת ההחלטות חייב להיעשות בזהירות.
מה המשמעות עבור המטופלות
בסך הכול Clinical‑OMTA מראה שמערכת בינה מלאכותית שאומנה על נתוני אולטרסונוגרפיה מגוונים יכולה להשיג ביצועים ברמת מומחה במיון גידולי אדנקס לקטגוריות שפיר, גבולי וממאיר, תוך שיפור משמעותי של מיומנות ועקביות בקרב רדיולוגים פחות מנוסים. מכיוון שהמערכת עובדת על פני מכשירים ומרכזים שונים, היא עשויה בסופו של דבר להשתלב במכשירי סריקה או לשמש כתוכנה עצמאית לתמיכה ברופאים במרפאות עמוסות או עם משאבים מוגבלים. המחברים מזהירים כי יש צורך במחקרים פרוספקטיביים ובינלאומיים נוספים לפני שימוש שגרתי, במיוחד בסביבות עם ציוד זול יותר או מפעילים שאינם בעלי התמחות מיוחדת. עם זאת, העבודה שלהם מצביעה על עתיד שבו יותר נשים, ללא קשר למקום הטיפול, יוכלו להנות מפענוח ברמת מומחה של סריקות שחלה ומהתאמה וטיפול בזמן ראוי.
ציטוט: Wu, Y., Dai, W., Li, X. et al. Development and validation of an artificial intelligence-based model for diagnosing benign, borderline, and malignant adnexal masses. npj Precis. Onc. 10, 106 (2026). https://doi.org/10.1038/s41698-026-01320-5
מילות מפתח: אולטרסונוגרפיה של השחלה, בינה מלאכותית, גידולים באדנקס, גידולי שחלה גבוליים, תמיכה בהחלטה קלינית