Clear Sky Science · he
הכללה של קטעי גידול אוטומטיים בתמונות מיקרוסקופיות של שקופיות שלמות בהיסטופתולוגיה על פני סוגי סרטן שונים
מדוע זה חשוב לטיפול בסרטן
אבחון סרטן עדיין מסתמך על מומחים שבוחנים שקופיות זכוכית של רקמה צבעונית במיקרוסקופ—משימה גוזלת זמן שמסבכת יותר עם עלייה במספר המקרים ומחסור בפתולוגים. מחקר זה שואל שאלה פשוטה אך עוצמתית: האם מערכת בינה מלאכותית אחת יכולה לזהות reliably אזורים סרטניים בתמונות מיקרוסקופ דיגיטליות עבור סוגי גידול רבים, במקום לבנות כלי נפרד לכל סרטן? אם כן, היא עשויה להקל בעומסי העבודה, לזרז את האבחון ולהרחיב ניתוחים מתקדמים אפילו לסרטנים נדירים שבהם הנתונים דלים.
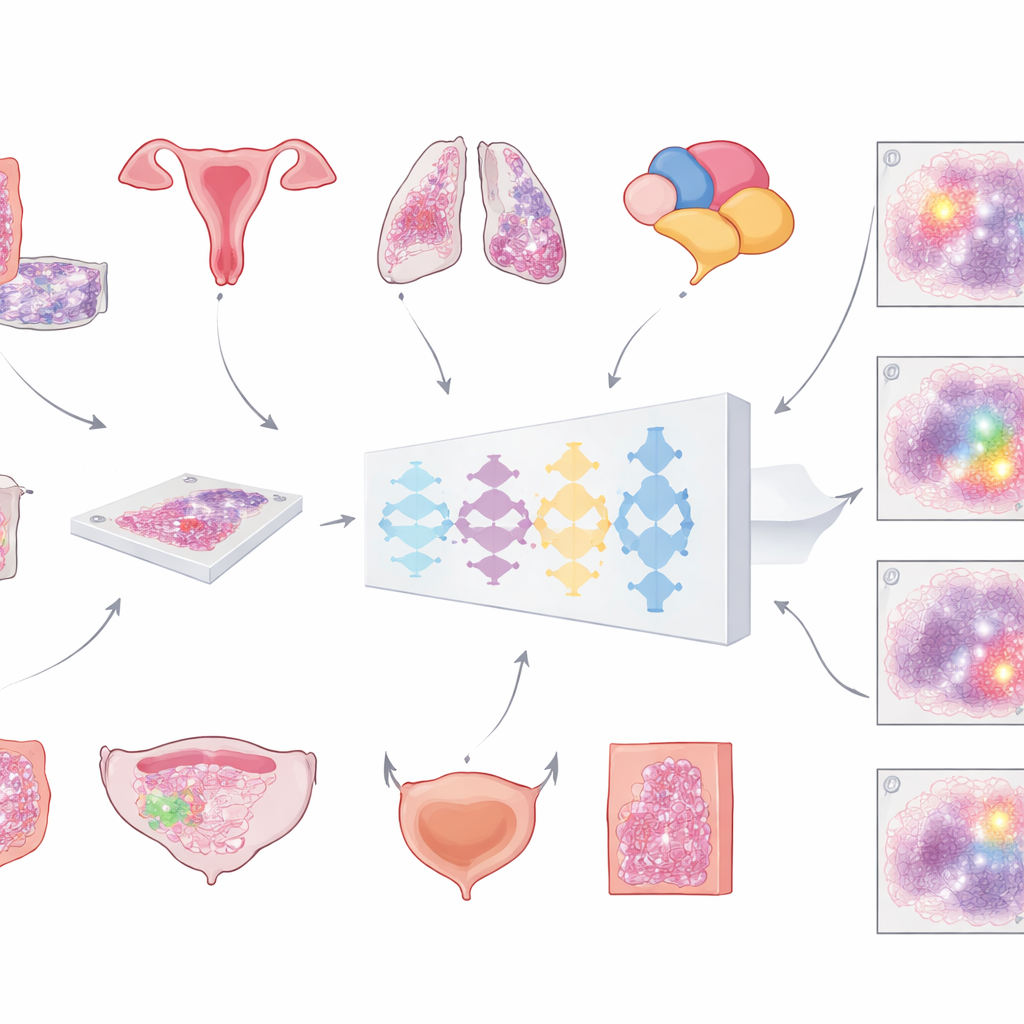
משקופיות זכוכית לעוזרים דיגיטליים
בתי חולים מודרניים סורקים יותר ויותר שקופיות מיקרוסקופ כדי ליצור תמונות "שלמות‑שקופית" ענקיות ומפורטות של גידולים. הצעד הקריטי הראשון לכל ניתוח ממוחשב הוא להפריד בין רקמה סרטנית לכל השאר—תאים נורמליים, שומן, שטחי זכוכית ריקים וארטיפקטים. עד כה, רוב הכלים האוטומטיים אומנו על סוג סרטן אחד בלבד, מה שגבילה את תחום היישום שלהם. הצוות מאחורי עבודה זו שאף לבנות מודל אוניברסלי אחד שיוכל לזהות אזורי גידול בסוגי סרטן נפוצים רבים בשקופיות צבועות בצביעת המיינה הרוטינית: המטוקסילין ואאוזין. החזון היה כלי כללי שניתן לחבר לרבים מתהליכי האבחון מבלי לעצב אותו מחדש בכל פעם.
להכשיר מודל אחד כדי לראות סרטן רב
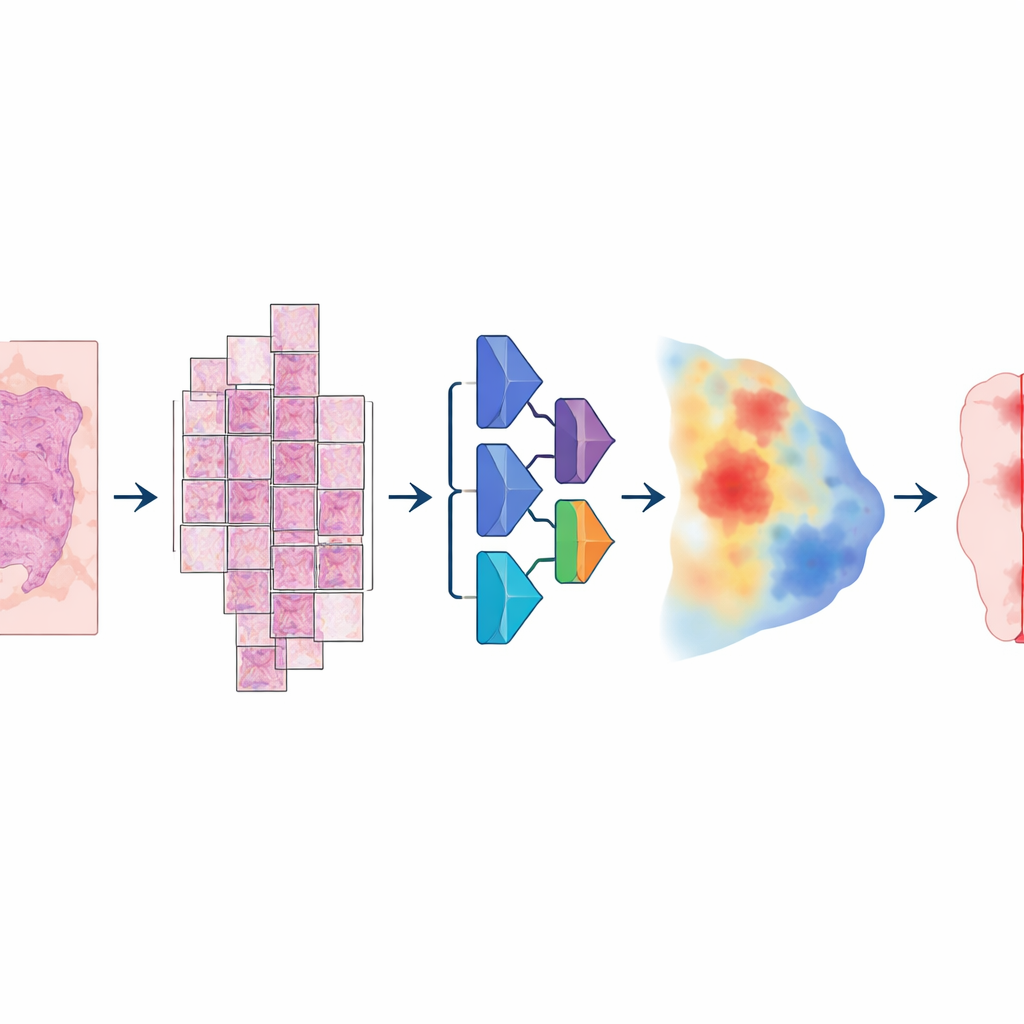
כדי לבנות את המודל, החוקרים אספו אוסף יוצא דופן בגודלו ובמגוון שלו של שקופיות דיגיטליות: יותר מ‑20,000 תמונות שלמות‑שקופית מיותר מ‑4,000 חולים עם סרטן המעי הגס, רירית הרחם, ריאה וערמונית. כל הדגימות הגיעו מרקמות מקובעות פורמלין ומוטמעות פארפין וסורקו בשני סורקי שקופיות ברזולוציה גבוהה שונים. פתולוג תיאר בקפידה את אזורי הגידול על כל שקופית, וסיפק את "האמת הקרקעית" שהמחשב ילמד ממנה. המודל עקב אחר צנרת מרובת שלבים: כל תמונה עצומה נחתכה לריצ'ים חופפים גדולים, הועברה דרך רשת עצבית עמוקה שהעריכה, לכל פיקסל, את ההסתברות להיות גידול, ואחר כך הורכבה חזרה למפת חלקה שהומרה בסופו של דבר למסכת גידול‑לעומת‑לא‑גידול נקייה.
העמדת המערכת למבחן
קריטית לכך, הצוות לא הסתפק בביצועי ההכשרה. הם בדקו את אותו מודל על יותר מ‑3,000 חולים נוספים בשישה סוגי סרטן—כולל סרטן השד ושלפוחית השתן שלא הופיעו כלל בהכשרה—ועל שקופיות מבתי חולים וסורקים שונים. הדיוק נמדד בעיקר בעזרת ציון חפיפה סטנדרטי (מקדם Dice), שמגיע ל‑100% כאשר מתאר הגידול של המחשב תואם במדויק את זה של הפתולוג. עבור דגימות גידול גדולות ושמורות במעי הגס, ברירית הרחם, בריאה, בערמונית ובשד, החפיפה הממוצעת עלתה על 80% ולעיתים קרובות על 90%. באוספים חיצוניים גדולים של The Cancer Genome Atlas, שנלקחו ממעבדות וסורקים רבים ברחבי העולם, הביצוע שוב נשאר מעל 80%, מה שמעיד שהמודל מתכלל היטב מעבר למוסד שאצלו הוא אומן.
איפה הוא מתקשה וכיצד הוא מושווה
החולשה העיקרית הופיעה בסרטנים של שלפוחית השתן בשלבים המוקדמים שנדגמו על ידי פרוצדורה שמייצרת חתיכות רקמה זעירות ומפורקות. במקרים אלה, המודל לעיתים קרובות לא סמן כלל גידול, במיוחד כאשר שטח הגידול היה קטן מאוד. עם זאת, כאשר זיהה גידול, החפיפה עם קווי המתאר של הפתולוג היתה גבוהה, ושינויים פשוטים בספים הסופיים שיפרו את התוצאות—רמז לכך שהרשת הבסיסית זיהתה את התבנית אך העיבוד שלאחריה היה נוקשה מדי. החוקרים גם בנו ארבעה מודלים "מומחים", כל אחד אומן על סוג סרטן בודד, ומצאו שאף אחד מהם לא עלה בצורה משמעותית על המודל הכללי בתחום שלו. לעומת זאת, מערכות המומחים נכשלו ברובה כאשר הוחלו על סוגי סרטן אחרים, בעוד שהמודל הכללי נשאר חסון. בהשוואה לכלי סגמנטציה רפואי פופולרי וכללי יותר שמשתמש ברמזים ממשתמש, המודל החדש בדרך כלל הופיע כטוב או טוב יותר תוך שהוא נשאר אוטומטי לחלוטין.
מה זה אומר עבור חולים ורופאים
ללא‑מומחים, המסקנה המרכזית היא שמערכת בינה מלאכותית מתוכננת היטב אחת יכולה לסמן באופן אמין רקמת סרטן על שקופיות דיגיטליות במספר סוגי גידול מרכזיים, ללא צורך בגרסאות מותאמות לכל מחלה או סורק. היא אינה מחליפה את הפתולוג, אך יכולה לסמן מראש אזורי גידול סבירים, לתמוך במדידות עקביות ולפנות את המומחים להתמקד במקרים המאתגרים ביותר. הגרסה הנוכחית עדיין מפספסת כמה גידולים קטנים מאוד או בשלבים מוקדמים—במיוחד דגימות של שלפוחית השתן המפורקות וסוגי רקמה דומים לנקבים—ולכן אינה מתאימה עדיין לזיהוי שיירי הסרטן החלשים ביותר. עם זאת, המחקר מראה שסגמנטציה רחבה "פאן‑סרטן" של גידולים אפשרית בתנאים מציאותיים ויכולה לשמש כצעד ראשון חזק לכלים אוטומטיים עתידיים שמעריכים דרגת סרטן, חוזים תגובה לטיפול או מנחים טיפולים מותאמים אישית.
ציטוט: Skrede, OJ., Pradhan, M., Isaksen, M.X. et al. Generalisation of automatic tumour segmentation in histopathological whole-slide images across multiple cancer types. npj Precis. Onc. 10, 107 (2026). https://doi.org/10.1038/s41698-026-01311-6
מילות מפתח: פתולוגיה דיגיטלית, למידה עמוקה, סגמנטציה של גידול, סריקת שקופיות שלמות, מודל פאן‑סרטן