Clear Sky Science · he
אובדן MicroRNA-29b מקדם דיכוי של STING בתיווך DNMT3b ומחליש את החיסון נגד גידול מזורח בעמידות לקרינה בסרטן קולורקטלי עם מוטציית KRAS
מדוע מחקר זה חשוב
עבור רבים החולים בסרטן הרקטום והמעי הגס, הקרינה היא חלק מרכזי בטיפול לפני הניתוח. עם זאת, חלק מהגידולים מצטמקים במידה מועטה בלבד, והסרטן לעתים קרובות חוזר או מתפשט. מחקר זה בוחן לעומק שינוי גנטי שכיח בסרטן הקולורקטלי — מוטציית KRAS — כדי להסביר מדוע גידולים אלה נוטים לעמוד בעמידות לקרינה ולתרופות אימוניות חדשות, ומציע אסטרטגיה להחזיר את מערכת החיסון של הגוף לפעולה נגדם.
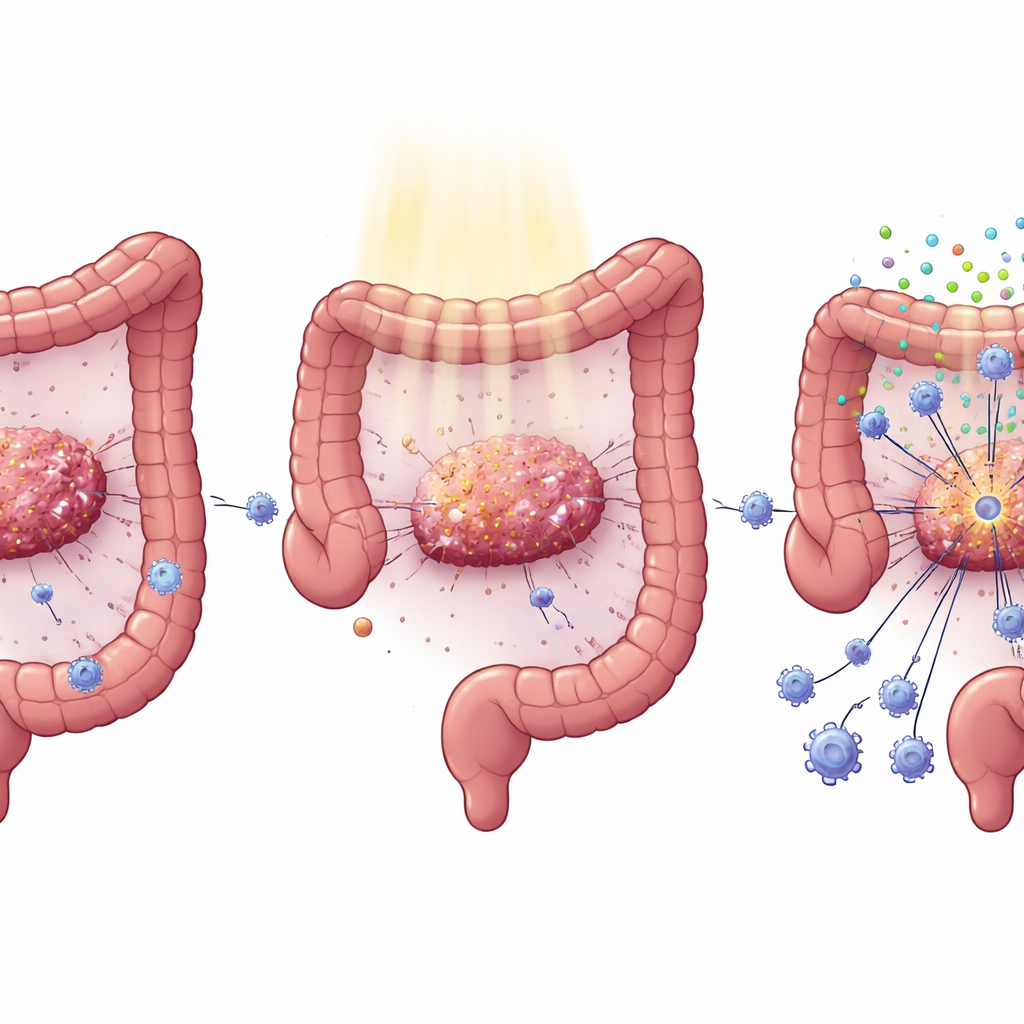
מוטציה שכיחה שמסתירה את הגידול מפני התקפת מערכת החיסון
סרטן הקולורקטום נושא לעתים קרובות מוטציות בגן KRAS, שהוא מניע ראשי לצמיחת הגידול ולהתפשטותו. קלינאים כבר שמו לב שגידולי KRAS-מוטנטיים נוטים להגיב באופן גרוע לטיפולים ממוקדים ולקרינה. על ידי כריית מאגרים גדולים של נתוני סרטן ובחינת דגימות חולים, המחברים מצאו כי גידולים עם KRAS מוטנטי מציגים פחות תאי CD8 הממיתים סרטן ופעילות חלשה יותר של אותות אינטרפרון המחזקים את המערכת החיסונית. בחולים שקיבלו כימורדיותרפיה סטנדרטית לפני ניתוח רקטלי, אלה עם KRAS תקין צברו הרבה יותר תאי CD8 בתוך הגידולים לאחר הטיפול מאשר אלה עם מוטציות ב‑KRAS, מה שמסייע להסביר את התוצאות הטובות יותר שלהם.
מערכת האזעקה החסרה בתוך תאי הגידול
הקרינה לא רק פוגעת בדנ״א של הגידול; היא גם יכולה לפעול כמו פנס חירום, ולגרום לתאי סרטן לשחרר שברי DNA שמפעילים מסלול אזעקה פנימי שנקרא cGAS–STING. כאשר STING פעיל, התאים מייצרים אינטרפרונים מסוג I ואותות אחרים שמאיישים ומפעילים תאים חיסוניים, כולל תאי T ותאי עצם מסרטן (dendritic). החוקרים הראו שבתאי קולורקטלנדמה שהונדסו לשאת KRAS מוטנטי, מערכת האזעקה הזו מוחלשת: לאחר קרינה, תאים אלה ייצרו הרבה פחות אינטרפרון ומולקולות קשורות. בעכברים, השתקת KRAS בגידולים החזירה את רמות ה‑STING, הגברת את אותות האינטרפרון, והביאה ליותר תאי CD4 ו‑CD8, פחות תאי T רגולטוריים ושליטה טובה יותר בגידול — לא רק בגידולים שהוקמו לקרינה אלא גם בגידולי "אבסקופל" מרוחקים שלא קיבלו קרינה.
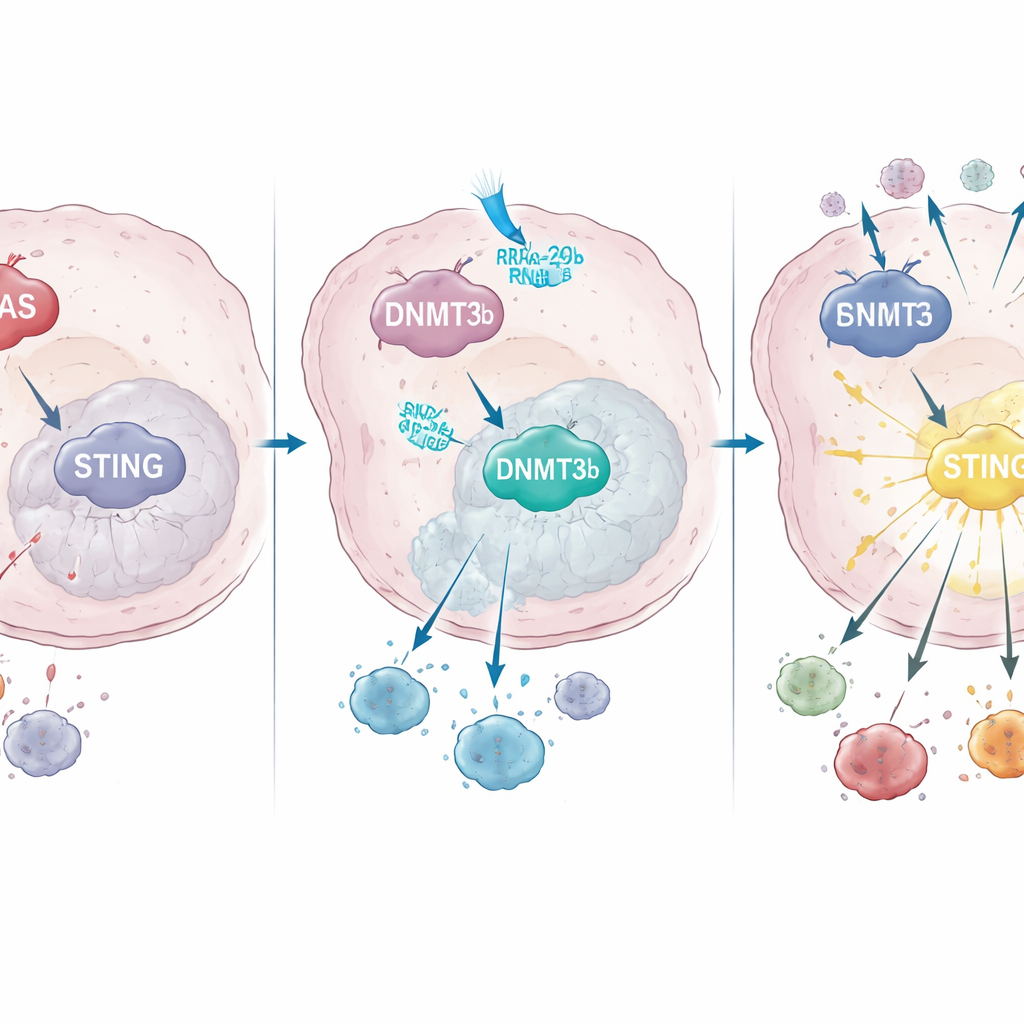
כיצד KRAS משנה את השליטה בגנים כדי לכבות את STING
בהעמקה נוספת מצאה הצוות שמוטציית KRAS מעלה את הפעילות של אנזים המשנה דנ״א שנקרא DNMT3b, שמוסיף קבוצות מתיל לאזורים מסוימים בדנ״א וכבה גנים סמוכים. בקווי תאים סרטניים ובדגימות חולים, רמות גבוהות של DNMT3b הלכו יד ביד עם רמות נמוכות של STING. קטע מפתח במקדם ה‑STING — אזור "ממפעיל" הדנ״א — היה ממותל במידה רבה בגידולים עם KRAS מוטנטי, אך לא באלה עם KRAS תקין. חולים שבהם הגידולים הצליחו עדיין להעלות את רמת ה‑STING אחרי כימורדיותרפיה הראו חדירה גדולה יותר של תאי CD8 והישרדות טובה יותר, מה שמדגיש כמה נתיב זה חשוב להצלחת הטיפול.
RNA קטן שיכול להעיר מחדש את האזעקה
המחברים שאלו אז מה גורם לרמות ה‑DNMT3b להיות כל כך גבוהות בסרטן עם KRAS מוטנטי. באמצעות רצף microRNA, זיהו RNA רגולטורי קטן, microRNA‑29b‑3p, שבאופן רגיל שומר על DNMT3b במגבלות אך מדוכא בחוזקה על ידי KRAS המוטנטי. שימור RNA זה בתאי KRAS‑מוטנטיים המגודלים במעבדה הוריד את ה‑DNMT3b, החיה מחדש את ה‑STING והעצים את ייצור האינטרפרון לאחר קרינה; חסימתו גרמה להשפעה הפוכה. בדוגמאות גידול, חולים עם KRAS מוטנטי נטו להצביע על רמות נמוכות של microRNA‑29b‑3p, רמות גבוהות של DNMT3b ורמות נמוכות של STING, ואלה עם רמות גבוהות יותר של microRNA‑29b‑3p חיו זמן רב יותר, וקשרו את השרשרת המולקולרית הזו לתוצאות קליניות.
שיטה ממוקדת להעברת גן שמחזקת קרינה ואימונותרפיה
כדי לתרגם את הממצאים לפוטנציאל טיפולי, הקבוצה הנדסה נגיף חסר-נזק (AAV) שמספק microRNA‑29b‑3p תחת בקרה של מקדם פעיל בעיקר בתאי קולורקטל. במודלים של עכברים הנושאים גידולי קולורקטל עם KRAS‑מוטנטי, מתן ה‑AAV יחד עם קרינה מקומית הקטין באופן דרמטי הן את הגידולים שהוקדמו לקרינה והן גידולים מרוחקים שלא קיבלו קרינה. הגידולים הראו פחות DNMT3b, יותר STING, יותר אותות אינטרפרון וחדירה כבדה של תאי T ותאים חיסוניים אחרים. כאשר אותו טיפול עם microRNA‑29b‑3p שודך למעכב נקודת בקרה חיסונית הפונה ל‑PD‑1, ההישרדות השתפרה עוד יותר, ותועלת זו הייתה תלויה בתאי CD8, מה שאישר שמערכת החיסון ביצעה את העבודה המכרעת.
מה זה יכול להצביע עבור חולים
בהגדרה פשוטה, המחקר הזה מגלה כיצד סרטן קולורקטלי עם מוטציית KRAS "חותך את החוט" למערכת אזעקה פנימית שהקרינה בדרך כלל מפעילה, ומאפשר לו להתחמק מהתקפת המערכת החיסונית. על ידי השבה של RNA קטן יחיד, microRNA‑29b‑3p, הצליחו החוקרים להוריד את DNMT3b, להעיר מחדש את ה‑STING ולהפוך גידולים "קרים" מבחינה אימונולוגית ל"חמים" שמגיבים טוב יותר הן לקרינה והן לבידוד נקודות בקרה חיסוניות. למרות שהעבודה עדיין בשלב שלפני‑קליני, היא מצביעה על טיפולים עתידיים שמשלבים קרינה עם גנטי‑תאי ממוקד בגידול כדי להתגבר על עמידות בסרטן קולורקטלי עם KRAS‑מוטנטי, ובכך להעניק תקווה שהטיפולים הקיימים יעבדו עבור רבים יותר מהחולים.
ציטוט: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
מילות מפתח: סרטן קולורקטלי עם מוטציית KRAS, עמידות לקרינה, נתיב STING, microRNA-29b, אימונולוגיה של גידול