Clear Sky Science · he
מודל למידה עמוקה מובן לתחזית תת‑הסוגים המולקולריים של סרטן האנדומטר מהצלבות צבועות H&E
מדוע זה חשוב לבריאות נשים
סרטן האנדומטר, שמתחיל ברירית הרחם, הוא אחד הסרטנים הנפוצים בקרב נשים, ושיעור התמותה ממנו עולה ברחבי העולם. כיום ידוע לרופאים שהמחלה מופיעה בפועל בכמה "טעמים" מולקולריים שמגיבים שונה לניתוח, לקרינה, לכימותרפיה ולתרופות חיסוניות חדשות. כיום גילוי תת‑הסוגים אלה דורש בדיקות גנטיות יקרות וארוכות שאינן זמינות בקלות בכמה בתי חולים. במחקר זה נחקר האם מערכת בינה מלאכותית (AI) שעוצבה בקפידה יכולה לקרוא שקופיות פתולוגיות שגרתיות — התמונות הורדרדות‑סגולות של הרקמה שנעשות לכל מטופלת — ולהסיק באופן מדויק את התת‑הסוגים המולקולריים, ובכך להרחיב את הזמינות של טיפול מותאם אישית.
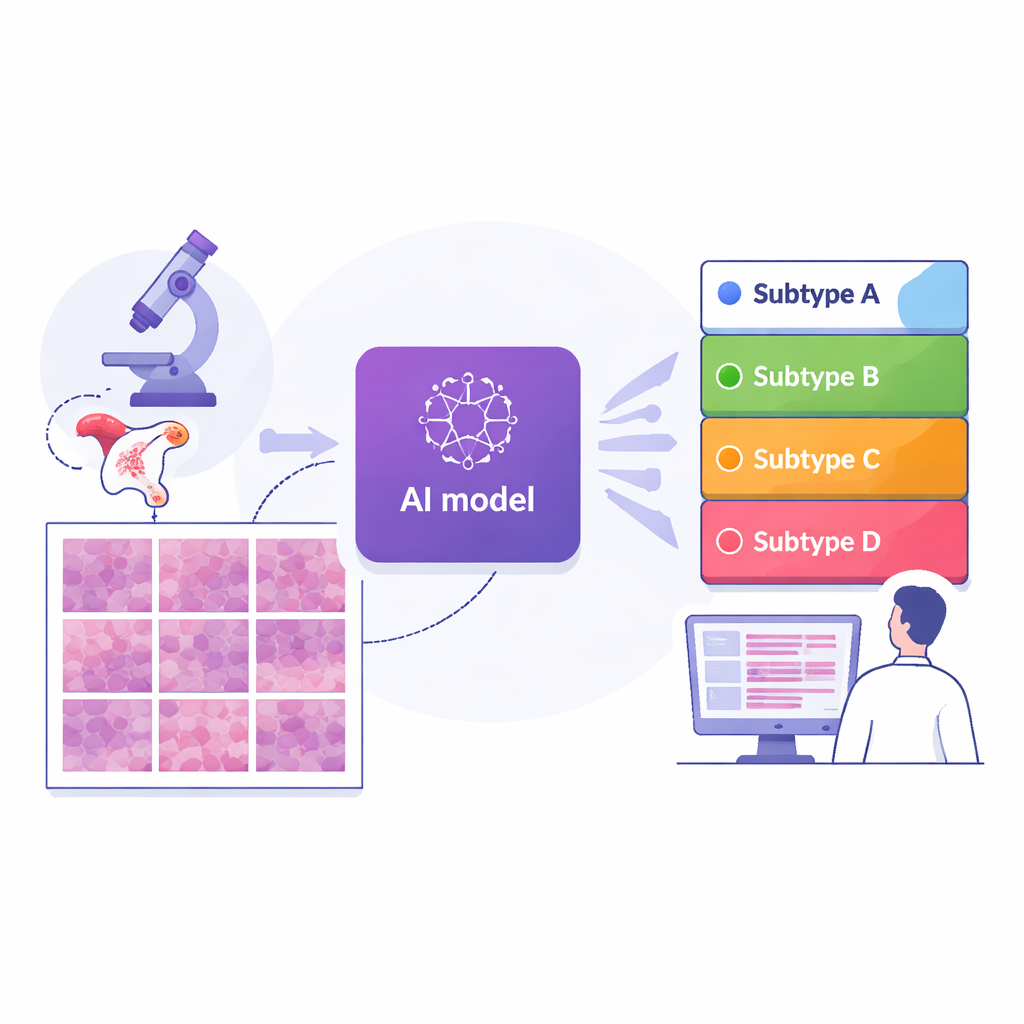
מבט קרוב על גיוון הגידול
לא כל סרטני האנדומטר מתנהגים אותו הדבר. חלקם גדלים לאט ונשארים מוגבלים ברחם; אחרים מתפשטים מוקדם וקשים יותר לטיפול. הנחיות מודרניות מחלקות גידולים אלה לארבעה תת‑סוגים מולקולריים המבוססים על שינויים ב‑DNA ועל אופן תיקון הנזק הגנטי בתאים. קטגוריות אלה מסייעות לחזות את ההסתברות לתוצאה ולכוון החלטות כגון היקף הניתוח והאם מטופלת עשויה להרוויח מטיפולי חיסון. עם זאת, הבדיקות הגנטיות והצבעים המיוחדים הדרושים יקרים, תלויות בפרשנות מומחים ולעיתים אינן זמינות בבתי חולים קטנים או בעלי משאבים מוגבלים. פתולוגים שיערו זמן רב שרבים מההבדלים המולקולריים משאירים רמזים חזותיים באופן שבו התאים והרקמה התומכת נראים במיקרוסקופ — אך הרמזים האלה יכולים להיות עדינים ומורכבים מדי עבור העין האנושית כדי לשפוט בעקביות.
לימוד מחשבים לקרוא שקופיות פתולוגיות
החוקרים אספו תמונות דיגיטליות של 364 שקופיות רקמה מ‑324 נשים שטופלו במרכז סרטן גדול בשנגחאי, יחד עם שתי קבוצות השוואה עצמאיות: 296 שקופיות ממאגר ציבורי בינלאומי ו‑36 משני בית חולים בסוז'ו. לכל מקרה כבר הוקצה אחד מארבעת תת‑הסוגים המולקולריים באמצעות בדיקות גנטיות מתקדמות. הצוות חיצה כל תמונת שקופית מלאה לאלפי אריחים קטנים ואימן מודל למידה עמוקה — סוג של AI המשמש לזיהוי תמונה — לצפות בכל אריח ולהעריך עד כמה סביר שהוא שייך לכל תת‑הסוג. על‑ידי חישוב ממוצע של תחזיות האריחים על פני כל השקופית, המערכת ייצרה תחזית תת‑סוג יחידה לכל מטופלת, בדומה לאופן שבו רופאים שוקלים את הגידול כמכלול.
עד כמה המערכת הופיעה
בקבוצת שנגחאי הראשית, ה‑AI הגיע לרמת דיוק גבוהה: הציון הכולל שלו להבחנה בין ארבעת תת‑הסוגים (נמדד באמצעות סטטיסטיקה סטנדרטית שנעה מ‑0.5 עבור ניחוש עד 1.0 להפרדה מושלמת) היה בערך 0.87. הביצועים נותרו חזקים — סביב 0.84 — כאשר נבדקו על שתי הקבוצות החיצוניות שנלקחו מבתי חולים ומערכות סריקה שונות לשקופיות, מה שמרמז שהשיטה די עמידה. בהשוואה למספר אסטרטגיות AI מובילות המשתמשות בסכמות תשומת‑לב או איגוד מסובכות יותר, מודל זה מקצה‑לסוף, המבוסס על שלד ניתוח תמונה מודרני, בדרך כלל הציג ביצועים טובים יותר. וחשוב מכך, המחברים תכננו את המערכת כך שתהיה ברת־הסבר: הם השתמשו בכלי ויזואליזציה כדי להדגיש בדיוק אילו אזורים בכל אריח ה‑AI הסתמך עליהם בקבלת החלטותיו.
מה ה‑AI "ראה" בסביבת המיקרו‑גידול
כדי להבין אילו תכונות הובילו את התחזיות, הקבוצה קישרה את מפת החום של ה‑AI לתצפיות פתולוגיות קלאסיות ולמדידות מפורטות של צורות ותצורות תאים בודדים. גידולים בתת‑סוג אחד הראו חדירה צפופה של תאי חיסון ברקמה התומכת, בעוד שתת‑סוג אחר נטה להכיל תאים מבניים דחוסים בצפיפות. קבוצה שלישית הציגה שכבות מוצקות של תאים גידוליים חריגים מאוד, ותת‑הסוג המקושר להתנהגות תוקפנית גילה מבנים פפילריים דמויי‑אצבע ושחידת גרעינים מאוד לא סדירה. על‑ידי סגמנטציה וניתוח של כ־245 מיליון תאים, החוקרים כימתו הבדלים בגודל התא, בשונות ובמרווחים, והראו כיצד צירופים מסוימים תואמים לתת‑סוגים ספציפיים. ממצאים אלה תומכים ברעיון שהבדלים מולקולריים משאירים חותם מוכר בארכיטקטורת הרקמה שהמכונות יכולות לזהות באופן שיטתי.
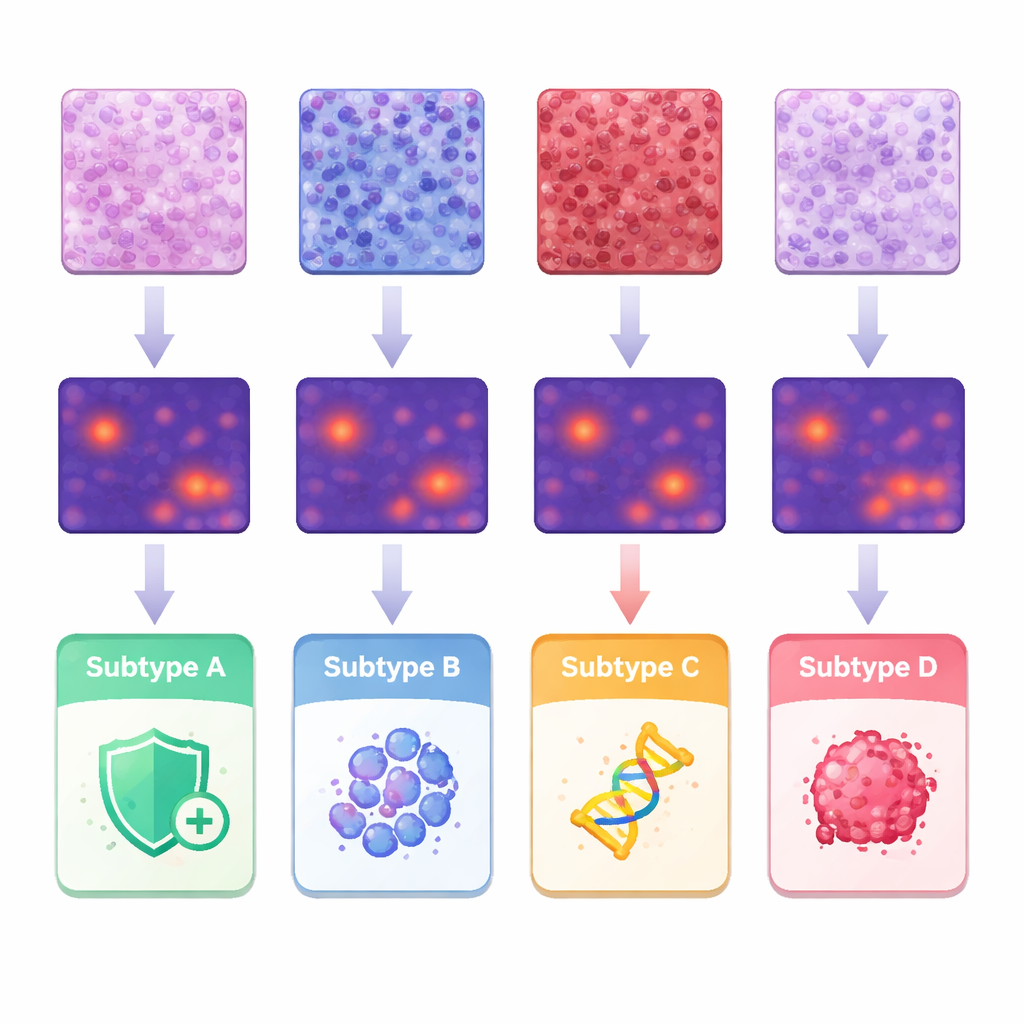
מראיה של הוכחה קונספט לעזרה קלינית
עבודה זו אינה שואפת להחליף בדיקות גנטיות; במקום זאת היא מציעה כלי מיון "H&E‑ראשון" המשתמש בצביעה הסטנדרטית שכבר מוכנה לכל ביופסיה. בפועל, מפה של הסתברויות תת‑סוג שנוצרה על‑ידי AI יכולה לסייע לפתולוגים להחליט אילו בדיקות לאמת להזמין קודם, להעדיף שימוש מוגבל ברקמה עבור המבחנים המידעיים ביותר ולהאיץ החלטות טיפול, במיוחד בבתי חולים שבהם פרופיל מולקולרי מלא קשה להשגה. המחקר מדגיש גם מגבלות נוכחיות, כגון ביצועים חלשים יותר עבור תת‑הסוג הנדיר ביותר והצורך במאגרי נתונים גדולים ומגוונים יותר לפני יישום קליני. עם זאת, הוא מציע דוגמה משכנעת לכך שתמונות מיקרוסקופיות שגרתיות מכילות מספיק מידע נסתר כדי ש‑AI יתקרב לתוויות מולקולריות מורכבות, ובכך פותח דרך לשירות מבוסס נתונים והוגן יותר לנשים עם סרטן האנדומטר.
ציטוט: Guo, Q., Cui, H., Zhang, Y. et al. An interpretable deep learning model for predicting endometrial cancer molecular subtypes from H&E-stained slides. npj Precis. Onc. 10, 71 (2026). https://doi.org/10.1038/s41698-026-01280-w
מילות מפתח: סרטן הרחם, פתולוגיה דיגיטלית, למידה עמוקה, תת‑הסוגים מולקולריים, אונקולוגיה מדויקת