Clear Sky Science · he
סינטילימאב ניאו-אדג'ובנטי, פקסליטאקסל קשור אלבומין וקרבופלטין לסרטן נבוב הוושט מקומי מתקדם בר-הסרה: מחקר קליני וחקר מנגנונים
שינוי המגמה מול סוג קטלני של סרטן הגרון
סרטן הוושט הוא אחד הסרטנים הקטלניים ביותר בעולם, ולעתים קרובות מאובחן רק לאחר שהוא התפשט עמוק לחזה. רבים מהחולים עדיין יכולים לעבור ניתוח, אך גם עם הכימותרפיה והקרינה הטובים ביותר כיום, הסיכון להישנות המחלה גבוה. במחקר זה בוחנים גישה חדשה לחיזוק ההגנות הטבעיות של הגוף לפני הניתוח ובוחנים במיקרוסקופ כיצד הגידולים והתאים שבסביבתם משתנים בתגובה. הממצאים מרמזים על טיפולים יעילים יותר ופותחים דרך לטיפול מותאם אישית באמת.
תכנית שלושה-תרופות חדשה לפני הניתוח
החוקרים גייסו 24 אנשים בסין עם צורת סרטן הוושט הנפוצה והאגרסיבית הנקראת קרצינומה קשקשית. אצל כולם היו גידולים מתקדמים אך עדיין ניתנים להסרה בניתוח. לפני הכניסה לחדר ניתוח קיבל כל מטופל שלושה מחזורים של טיפול משולב: סינטילימאב, נוגדן שמפעיל את המערכת החיסונית ומסייע לתאי T לזהות את הסרטן; יחד עם שתי תרופות כימותרפיות סטנדרטיות, פקסליטאקסל קשור לאלבומין וקרבופלטין. לאחר שלב "ניאו-אדג'ובנטי" זה עברו המטופלים ניתוח להסרת גידול הוושט, וברובם המשיכו לאחר מכן עם סינטילימאב.
כיווץ גידול חזק יותר ותוצאות הישרדות מעודדות
כאשר המנתחים והפתולוגים בדקו את הגידולים המוסרים, הם גילו שלשלב לפני הניתוח הייתה השפעה של כיווץ עמוק ברבים מהחולים. כ-42% הראו תגובה פתולוגית משמעותית, כלומר נותר רק אחוז קטן של תאי סרטן חיים. אחד מכל שלושה חולים לא הראו כלל תאי סרטן ברואים באזור הגידול הראשי. בסריקות ומעקב קליני התוצאות אף הן היו מבטיחות: שלוש שנים לאחר הטיפול, כשלושה מתוך ארבעה חולים היו בחיים ללא סימני הישנות המחלה, וכמעט ארבעה מתוך חמישה היו עדיין בחיים. חשוב לציין שתופעות הלוואי של התכנית המוגברת היו ניתנות לניהול, ללא מקרי מוות הקשורים לטיפול והסרה ניתוחית נותרה בטוחה ובת-ביצוע.
כיצד השכונה של הגידול מעצבת את התגובה
לא כל מטופל נהנה מאותה תועלת, ולכן הצוות חקר מדוע. הם התרכזו במיקרו-סביבה של הגידול — השכונה המורכבת של תאי סרטן, תאי מערכת החיסון ומולקולות איתות. באמצעות מדידות חלבון ממוקדות על דגימות גידול שחולקו בקפידה השוו בין אלה שענו היטב לטיפול ובין אלה שלא. לפני הטיפול הם מצאו 14 חלבונים שהבדילו בין שתי הקבוצות. חלבון משטח אחד, CD44, בלט: גידולים עם רמות גבוהות יותר של CD44 נטו להגיב טוב יותר לטיפול המבוסס סינטילימאב. לאחר הטיפול ירדו ברמות חלבונים רבים המעורבים בפעילות חיסונית ובתיקון DNA אצל המגיבים, מה שמרמז שהטיפול המשולב הפר את מערכות התמיכה של הסרטן ועיצב מחדש את הנוף החיסוני המקומי.
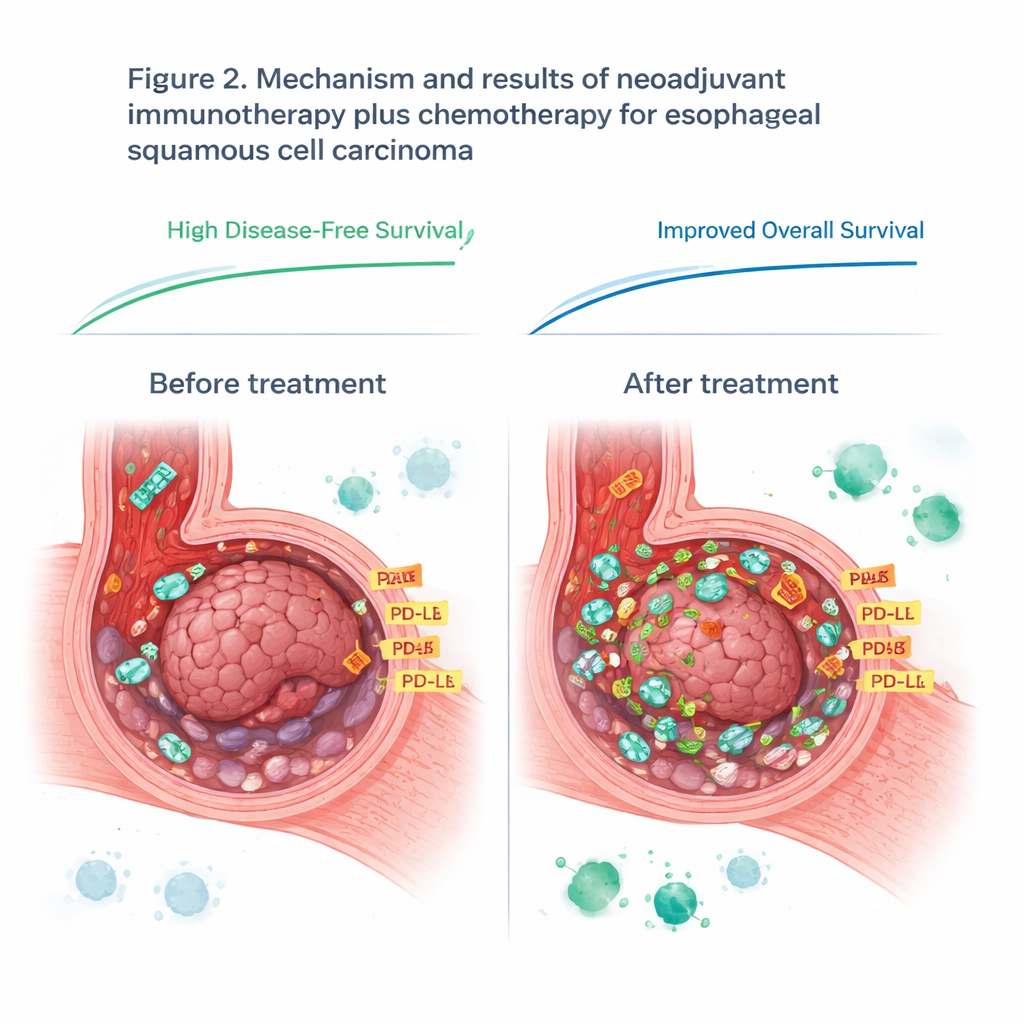
מחשבה מחדש על סימן חיסוני פופולרי
המחקר בדק גם את PD-L1, חלבון שמשמש לעתים קרובות כמצפן להחלטה מי עשוי להפיק תועלת מתרופות עוצרות ציר חיסוני. לפני הטיפול רמות PD-L1 בדגימות הגידול לא חזו מי יצליח, דבר שמאתגר את הנוהג הקיים בסוג סרטן זה. עם זאת, רמות PD-L1 עלו אצל כל מטופל במהלך הטיפול, כנראה כי המערכת החיסונית המופעלת הציפה את הגידול באותות דלקתיים. לאחר הטיפול רמות PD-L1 גבוהות יותר ברקמת הגידול שנותרה היו מקושרות קרוב יותר לאופן שבו האימונותרפיה עבדה. זה מציע שהזמן חשוב: תמונה בודדת של PD-L1 לפני הטיפול עלולה לפספס שינויים מכריעים שמתפתחים ברגע שהמערכת החיסונית מעורבת.
מה משמעות הדבר עבור מטופלים ולעתיד
לאנשים המתמודדים עם ניתוח בשל סרטן וושט מתקדם, מחקר זה מציע שתי מסרות תקווה. ראשית, שילוב סינטילימאב עם כימותרפיה לפני הניתוח נראה ככזה שמצמצם את הגידולים ביתר עומק ועשוי לשפר את הסיכוי להישרדות לטווח הארוך, מבלי להוסיף תופעות לוואי מסכנות חיים. שנית, העבודה מראית כי הגידול ומיקרו-הסביבה שלו אינם קבועים; הם מעוצבים מחדש על ידי הטיפול בצורות שאפשר לעקוב אחריהן באמצעות חלבונים כגון PD-L1 ו-CD44. בעתיד, טביעות אצבע מולקולריות כאלה יכולות לסייע לרופאים לבחור ולהתאים טיפולים בזמן אמת, ולהפוך יותר גידולים "קרים" המתעלמים מהמערכת החיסונית ל"חמים" המזמינים מתקפה חיסונית חזקה ומתמשכת.
ציטוט: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
מילות מפתח: סרטן הוושט, אימונותרפיה, טיפול ניאו-אדג'ובנטי, מעכבי PD-1, מיקרו-סביבה של הגידול