Clear Sky Science · he
עיצוב טיפול אינדיבידואלי בעזרת אלגוריתמים משפר הישרדות במודל עכבר של סרטן השד המשולש-שלילי
מדוע כימוֹתרפיה חכמה משמעותית
כימוֹתרפיה מצילה חיים, אך ברוב המקרים ניתנת עדיין באופן «ממוסך לכלל»: מטופלים עם סרטן דומה מקבלים לעתים קרובות את אותו מינון ובאותו לוח זמנים. משמעות הדבר יכולה להיות תופעות לוואי קשות אצל חלק מהמטופלים ותועלת לא מספקת אצל אחרים. המחקר המתואר כאן שואל שאלה פשוטה אך חזקה: מה אם נוכל להשתמש באלגוריתמים ממוחשבים כדי לכוונן את הכימוֹתרפיה לכל פרט בזמן אמת, כמו תרמוסטט שמווסת חימום בבית? באמצעות מודל עכבר מתקדם של סרטן שד אגרסיבי, החוקרים מראים כי מינון מותאם כזה יכול להאריך הישרדות ולהגביל את התפתחות העמידות לתרופה.
הבעיה בלוחות זמנים שגרתיים של תרופות נגד סרטן
כיום, רבים מהמטופלים מקבלים את המינון הגבוה ביותר של כימוֹתרפיה שהם יכולים לשאת, בניתוקים קבועים. פרוטוקול זה, המכונה מינון מקסימלי נסבל, אינו מתחשב בקצב הגדילה הייחודי של גידול מסוים, באופן שבו גוף המטופל מעבד את התרופה או באופן שבו אותו גידול מגיב לאורך זמן. כתוצאה מכך, גידולים עלולים להצטמצם בתחילה אך לשוב מאוחר יותר כגרסאות עמידות יותר לתרופה, בעוד המטופלים סובלים מתופעות לוואי חזקות. ניסיונות מוקדמים לשפר זאת, כגון כימוֹתרפיה «מטרונומית» במינונים קטנים ותכופים יותר, הניבו תוצאות מעורבות בניסויים קליניים ולא הגדירו בבירור כיצד לבחור מינונים ותזמונים מיטביים. יש צורך ברור בגישה יותר רציונלית ואינדיבידואלית לתזמון הכימוֹתרפיה.
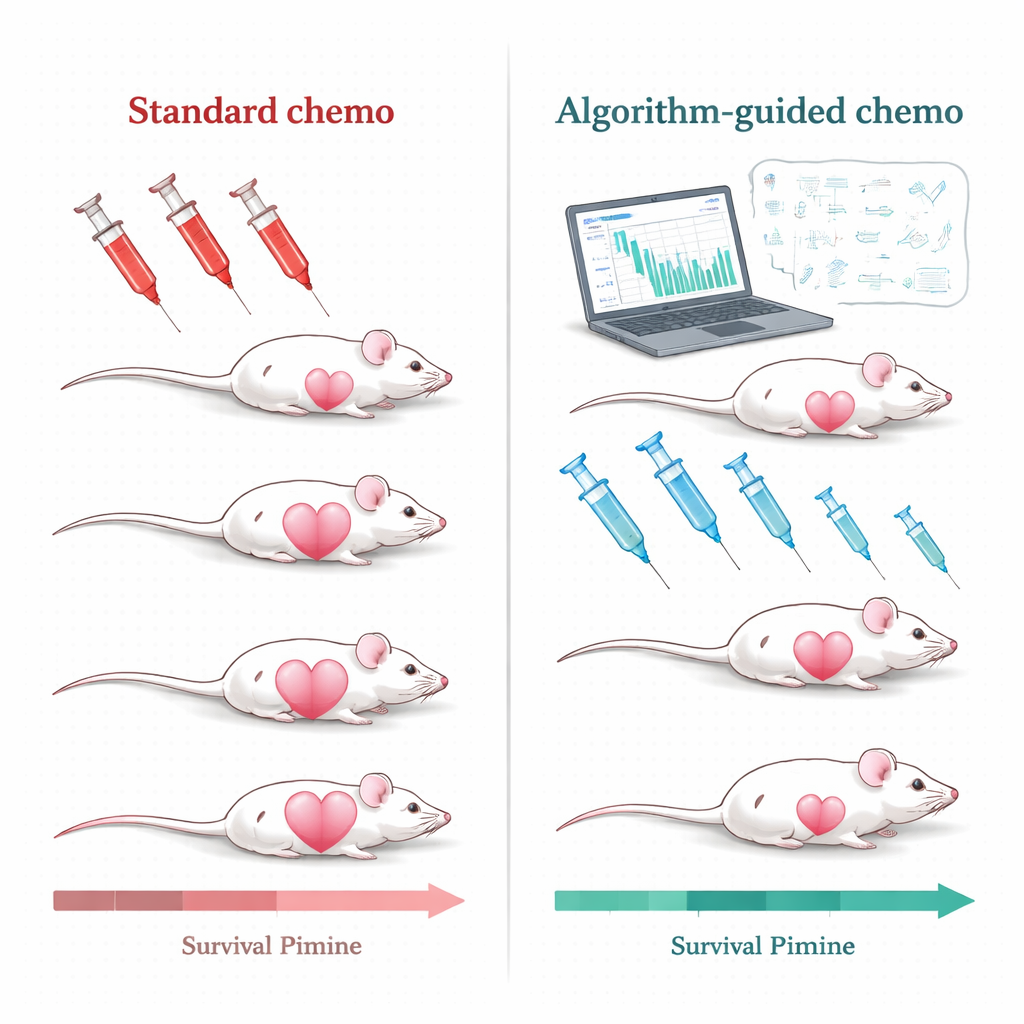
שימוש באלגוריתמים להתאמת הטיפול
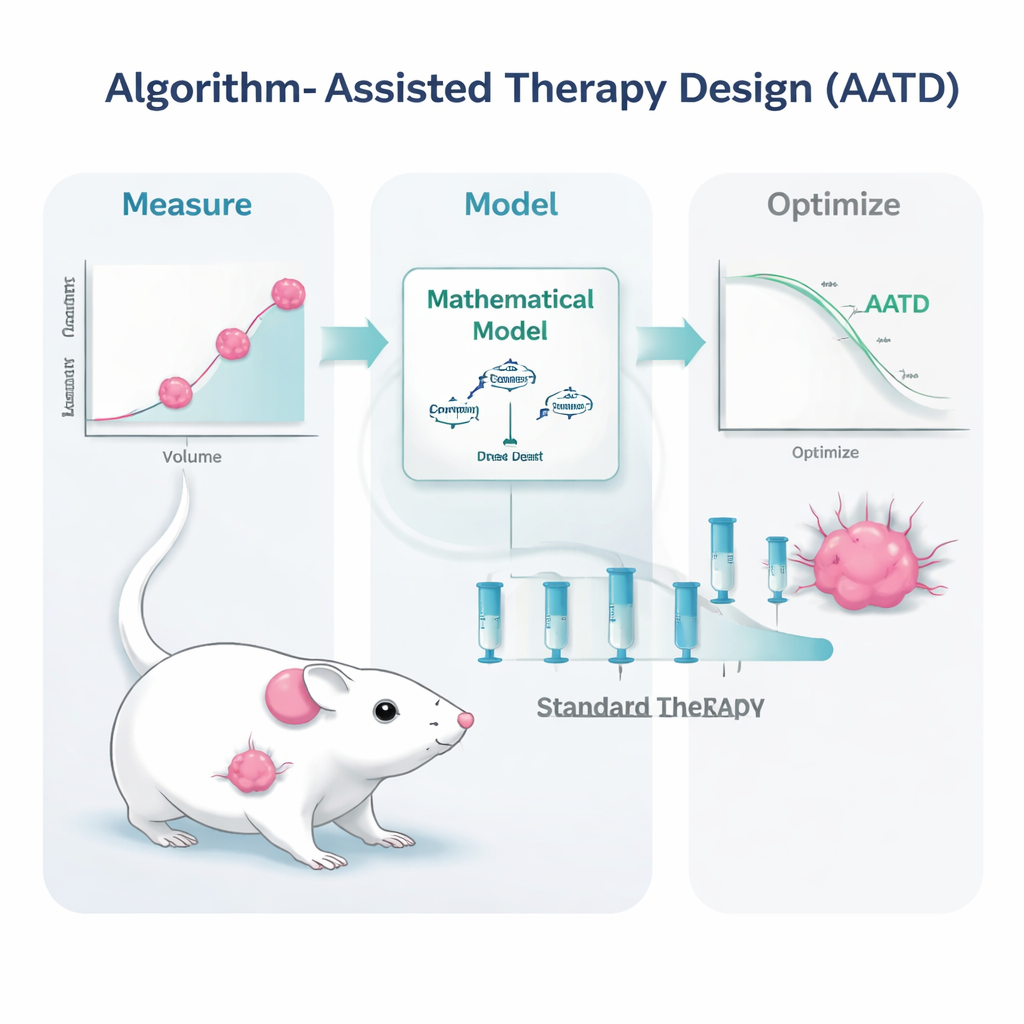
צוות המחקר התמודד עם האתגר הזה בעכברים הנושאים גידולים משולשים-שליליים, צורה של סרטן השד שבני אדם מתקשים במיוחד לטפל בה ועדיין מסתמכת כמעט לחלוטין על כימוֹתרפיה. העכברים טופלו בתרכובת תרופתי נפוצה, דוקסורוביצין בליפוזום פיגוליזי. במקום לחזור על טיפולים במינון גבוה רק כאשר הגידולים צמחו חזרה לגודל קבוע, המדענים בנו מודלים מתמטיים המתארים כיצד הגידול גדל, נסוג תחת טיפול, וכיצד התרופה נעה במחזור הדם. הם הזינו למודלים מדידות פשוטות וריאליסטיות מבחינה קלינית: קריאות חוזרות של גודל הגידול ורמות התרופה בדם. מתוך קלטים אלה, אלגוריתם מחשב יצר תוכניות טיפול מותאמות אישית לכל עכבר.
שתי דרכים להיעזר במחשב
המחקר בחן שתי וריאציות של עיצוב טיפול בסיוע אלגוריתם. בגישה אחת, שנקראת PDPK, המחשב השתמש בנתונים מוקדמים כדי לעצב לוח זמנים של 30 יום הכולל מינונים יחסית קטנים וחוזרים, שמטרתם לשמור על רמת תרופה בדם יציבה אך נמוכה — גבוהה דיה כדי לשלוט בגידול, אך נמוכה די לצמצום רעילות. בגישה השנייה, שנקראת בקרה חזויה מודלית (model predictive control), האלגוריתם עדכן את התוכנית מדי יום על בסיס המדידה העדכנית של הגידול, והתאים את גודל המינון כדי לדחוף את הגידול בירידה מתמשכת. שתי השיטות נשענו על אותה רעיון בסיסי: להשתמש ב»תאום דיגיטלי« ריאלי של העכבר הנושא הגידול כדי לסמלץ רבות של דפוסי מינון אפשריים מראש ולבחור את אלה הסבירים להצליח ביותר במסגרת מגבלות בטיחות.
הישרדות ארוכה יותר ופחות עמידות לתרופות
בהשוואה לפרוטוקול הסטנדרטי של מינון גבוה המופעל על ידי חזרת הגידול, ההבדלים היו בולטים. בטיפול המקובל, גידולים לעתים התקטנו במהירות בתחילה אך בסופו של דבר חזרו, והחזרת מינונים גדולים עידדה הופעת מחלה עמידה לתרופה. לעומת זאת, מרבית הטיפולים שעוצבו על ידי האלגוריתם שמרו על שליטה הדוקה יותר על הגידולים, האריכו את הזמן עד הישנות ובמקרים רבים מנעו סימנים ברורים של עמידות במהלך תקופת המחקר. בקרב עשרות עכברים, גם קבוצות PDPK וגם קבוצת הבקרה החזויה חיו תקופות משמעותית ארוכות יותר בהשוואה לחיות בלוח הסטנדרטי, כאשר מספר אסטרטגיות מבוססות אלגוריתם הראו רווחי הישרדות חזקים ומשמעותיים סטטיסטית.
מה זה עלול означать עבור מטופלים בעתיד
למרות שעבודה זו בוצעה בעכברים, מרכיביה המרכזיים — מדידת גודל הגידול, ניטור רמות התרופה בדם והפעלת מודלים ממוחשבים — כבר אפשריים במטופלים אנושיים באמצעות דימות מודרני וכלי מעבדה. המחקר מציע שבמקום לשאול «מהו המינון התקני?», רופאים יבקשו יום אחד לשאול, «בהינתן התנהגות הגידול ודרך עיבוד התרופה אצל מטופל זה, איזה מינון ותזמון יהיו הטובים ביותר כרגע?» קיימים אתגרים מעשיים, כגון הצורך במדידות תכופות יותר והלוגיסטיקה של מינונים גמישים, אך המסר ברור: כימוֹתרפיה לא חייבת להיות גסה ואחידה. בעזרת אלגוריתמים היא יכולה להפוך לכלי מדויק, מסתגל, שמציע למטופלים סיכוי טוב יותר לשליטה לטווח ארוך על סרטן אגרסיבי.
ציטוט: Gombos, B., Léner, V., Drexler, D.A. et al. Algorithm-assisted individualized therapy design improves survival in a mouse model of triple-negative breast cancer. npj Precis. Onc. 10, 84 (2026). https://doi.org/10.1038/s41698-025-01245-5
מילות מפתח: כימוֹתרפיה מותאמת אישית, סרטן השד המשולש-שלילי, טיפול בעזרת אלגוריתם, מודל מתמטי של גידול סרטני, מינון דוקסורוביצין