Clear Sky Science · he
טרנסקריפטומיקה מרחבית חושפת הטרוגניות מולקולרית ומטרות טיפוליות ספציפיות-תת בסרטן הריאה התאי‑הקטן
מדוע מחקר סרטן הריאה הזה חשוב
סרטן ריאה תאי‑קטן הוא אחד מסוגי הסרטן המסוכנים ביותר, פוגע בעיקר באנשים עם היסטוריית עישון וחוזר לעתים במהירות לאחר כימותרפיה. רופאים יודעים שלא כל גידול מסוג זה מתנהג אותו הדבר, אך הם חסרו כלים לראות כיצד סוגי תאים סרטניים ותאי מערכת החיסון מסודרים בתוך כל גידול. במחקר זה השתמשו בטכנולוגיה חדשה שקוראת את פעילות הגנים באלפי נקודות קטנות על פני preparat של הגידול, ויוצרת "מפה מולקולרית" של כל דגימה. בשילוב עם ניתוח חישובי מותאם, החוקרים גילו דפוסים חבויים שעשויים להצביע על טיפולים מדויקים יותר, התואמים לתת‑הסוגים.
מיפוי הגידולים במקומם
הצוות ניתח דגימות גידול מ‑21 חולים עם סרטן ריאה תאי‑קטן בשלב מוגבל שעברו ניתוח לפני קבלת כל טיפול תרופתי. במקום לטחון את הרקמה ולאבד את כל המידע המרחבי, הם החילו טרנסקריפטומיקה מרחבית: שיטה שמודדת אילו גנים מופעלים בנקודות רבות ומוגדרות בחתך רקמה. כל נקודה נשארת במיקומה המקורי, מה שמאפשר לקשר בין פעילות גנים לבין המיקום בו נמצאים תאי הסרטן, התאים הרגילים ותאי החיסון. מעל לכך הוסיפו שני כלים מרכזיים: מדד חדש בשם "Edgeindex" לכימות עד כמה תאי הגידול חודרים לרקמות השכנות, וכן רשת עצבית מלאכותית — צורת למידת מכונה — שמסמנת באופן אוטומטי אילו נקודות הן גידול ואילו אינן.
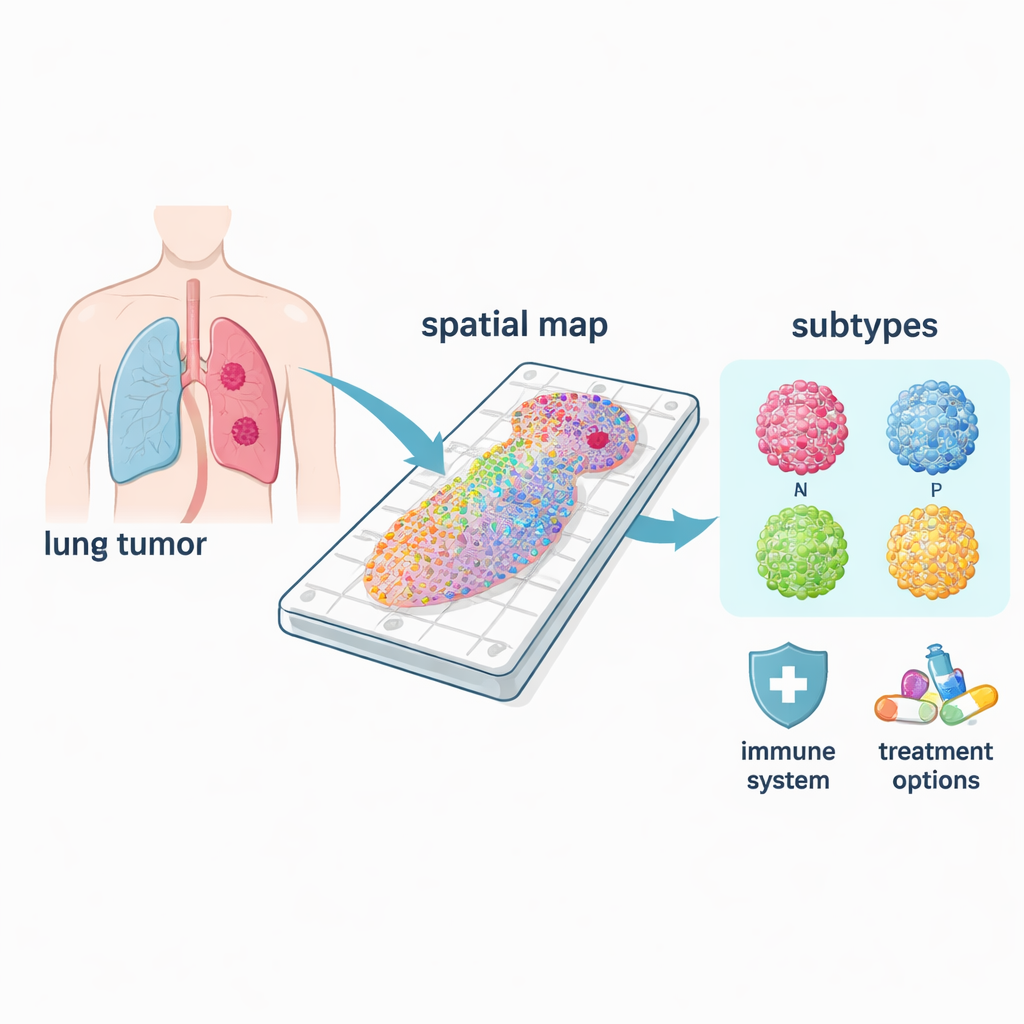
סוגי סרטן שונים במחלה אחת
סרטן ריאה תאי‑קטן אינו מחלה אחת אחידה אלא כולל לפחות ארבעה תתי‑סוגים מולקולריים עיקריים, שלרוב מכונים ASCL1, NEUROD1, POU2F3 ו‑YAP1, על שם גנים מרכזיים שמגדירים אותם. באמצעות המפות המרחביות שלהם יכלו החוקרים לראות היכן כל תת‑סוג שולט בתוך הגידולים וכיצד הביולוגיה שלהם שונה. הצורות הנפוצות ASCL1 ו‑NEUROD1 נקשרו באופן חזק לתכניות חלוקת תאים, בהתאם למוניטין שלהן כרבות חלוקה. לעומת זאת, אזורי POU2F3 היו מקושרים למסלולים הקשורים למערכת החיסון, בעוד אזורי YAP1 הראו אותות הקשורים לחילוף חומרים ולשיקום רקמות — תכונות שעשויות להיות קשורות להתפשטות ולעמידות לטיפול. מפני שהדפוסים האלה מפורקים במרחב, השיטה מאפשרת לזהות את תת‑הסוג ה"מניע" האמיתי בתוך גידול מעורב, דבר שמבחני בולק לרוב מפספסים.
הקצה החודר והשינוי החיסוני
אחת החידושים המרכזיים במחקר, Edgeindex, מודדת עד כמה תאי הגידול מתערבבים עם רקמת הסביבה שאינה גידולית. ציונים נמוכים משקפים גידולים קומפקטיים ומוגדרים היטב, בעוד ציונים גבוהים מצביעים על איים מפוזרים ושוליים פולשים ומקוטעים. גידולים עם Edgeindex גבוה הועשרו בתכניות גנטיות הקשורות למטריצה חוץ‑תאית, גרורות ומוות תאי. בנוסף הם הראו תמונה חיסונית משנה באופן בולט: פחות תאי T מסייעים ושחקנים אדפטיביים אחרים, אך יותר תאים מולדים כגון תאי NK מסוימים ומונוציטים. המחברים מפרשים זאת כ"שיקום נישה אימונולוגית", שבו הגידול דוחק החוצה תגובות חיסוניות מדויקות ומותירות הגנה פחות יעילה, בעיקר מולדת, שאינה שולטת במלואה במחלה.
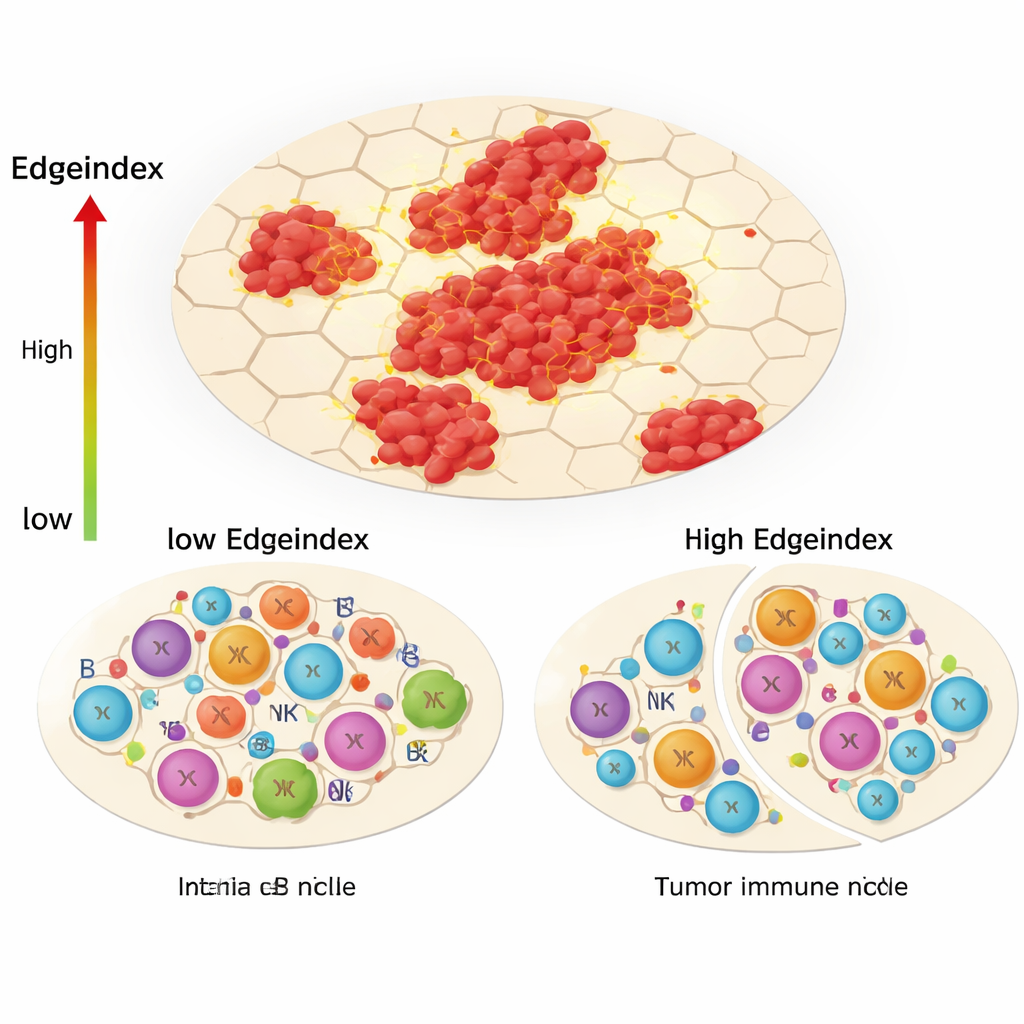
מגוון חבוי בתוך ומסביב לגידולים
מעבר לתת‑הסוג ודפוסי החדירה, הנתונים המרחביים חשפו כי גם אוכלוסיות תאי הסרטן וגם המיקרו‑סביבות המקיפות אותן היו פנימית־מגוונות. על‑ידי אשכול נקודות בתוך כל גידול, הצוות ספר כמה שכונות ביטוי‑גנים מובחנות התקיימו באזורי הסרטן וברקמה הסמוכה שאינה גידולית. גיוון גבוה יותר בתוך הגידול קושר למסלולים הקשורים לחיסון, בעוד תבניות מסוימות ברקמה הסובבת נקשרו לפעילות מחזור‑תא ולוויסות גנטי. החוקרים גם בחנו עד כמה אזורים שונים "תקשרו" באמצעות מולקולות איתות ידועות. גידולים עם תקשורת אינטנסיבית יותר בין אזורים נטו להראות אותות חזקים יותר הקשורים לחיסון, מה שמחזק את הרעיון שפעילות חיסונית וצמיחה סרטנית קשורות זו בזו במרחב.
מעקב אחר התפתחות הגידול לאורך זמן
כדי לאמוד כיצד תאי הגידול משתנים ככל שהמחלה מתקדמת, הצוות ביצע ניתוח "פseudotime" שמסדר תאים לאורך מסלול התפתחותי בהתבסס על פעילות הגנים שלהם. בדגימות השונות זיהו בשיטתיות גן אחד, UCHL1, כמרכזי במסלולים אלה. רמות גבוהות של UCHL1 הופיעו לצד פעילות מחזור‑תא חזקה בנקודות הגידול, בעוד שרמות נמוכות יותר התקשרו למסלולים חיסוניים ומות תאים. מכיוון ש‑UCHL1 הוא חלבון מסוג עצבי שנקשר בעבר לסרטן ריאה אגרסיבי, ממצאים אלה מחזקים את האפשרות שהוא עשוי להיות מטרה תרופתית שימושית, במיוחד לתאים הדמויי‑נוירו‑אנדוקרין שמניעים את סרטן הריאה התאי‑הקטן.
מה משמעות הדבר למטופלים
באופן פשוט, המחקר הזה הופך צלחות מיקרוסקופ שטוחות של סרטן ריאה תאי‑קטן למפות עשירות רב‑שכבתיות שמראות היכן ממוקמים תתי‑הסוגים השונים, עד כמה הם פולשניים, כיצד הם מתקשרים עם סביבתם וכיצד מערכת החיסון מגיבה או נכשלת. מדד ה‑Edgeindex והשיטה המיפוי מדגישים אילו גידולים במיוחד פולשניים ואילו תאי חיסון נוכחים או חסרים בגבול. על ידי קישור דפוסים מרחביים אלה לחולשות ספציפיות‑תת‑סוג — כגון תרופות שמכוונות DLL3, BCL‑2, AURKA, IGF‑1R/PARP או נקודות ביקורת חיסוניות — העבודה מקרבת את התחום להתאמת אסטרטגיית טיפול מותאמת לכל חולה. אמנם כלים אלה עדיין זקוקים לבחינה במחקרים גדולים יותר, אך הם מציעים תוואי דרך לטיפולים מדויקים וייתכן שיעילים יותר בסוג סרטן שזקוק בדחיפות לאפשרויות טובות יותר.
ציטוט: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
מילות מפתח: סרטן ריאה תאי‑קטן, טרנסקריפטומיקה מרחבית, הטרוגניות בגידול, מיקרו‑סביבת חיסון של הגידול, אונקולוגיה מדויקת