Clear Sky Science · he
תכונות פתולוגיה חישובית של ארכיטקטורת החיסון חוזות תוצאות קליניות חשובות בסרטן ריאות תאי קטן (SCLC)
למה מגן הגוף חשוב בסרטן הריאה
סרטן ריאות תאי קטן הוא אחת הצורות האגרסיביות ביותר של סרטן הריאה, והוא לרוב מתפשט במהירות וחוזר לאחר טיפול. רופאים יכולים לראות גידולים במיקרוסקופ, אבל הדפוסים המפורטים של האופן בו תאי הסרטן ותאי החיסון יושבים זה לצד זה מורכבים מדי לשיפוט בעין. במחקר זה מוצעת שיטה ממוחשבת בשם PhenopyCell שקוראת את הדפוסים החבויים הללו משקופיות ביופסיה שגרתיות ומשתמשת בהם כדי לחזות כמה זמן סביר שהמטופלים יחיו וכמה טוב הם יגיבו לכימותרפיה. עבור מטופלים ובני משפחותיהם, תובנה כזו עשויה יום אחד לסייע בהתאמת טיפול במקום להסתמך על גישה אחידה לכולם.
הבנה מקרוב של סרטן ריאה קטלני
סרטן ריאות תאי קטן מהווה כ‑15% מהמקרים של סרטן ריאה אך גורם לחלק גדול מהמיתות משום שהוא גדל ומתפשט במהירות. הוא מחולק בדרך כלל ל״מחלה מוגבלת״, שיכולה להיכנס לשדה קרינה אחד, ו״מחלה נרחבת״, שהתפשטה יותר. הטיפול הראשוני הסטנדרטי כולל כימותרפיה מבוססת פלטינה, לעתים בשילוב עם אימונותרפיה. גידולים רבים נראים כאילו נעלמים תחילה, אך הסרטן חוזר לעיתים בתוך שנה, ופחות מאחוז אחד בעשרה שורדים לאורך זמן. הבדיקות הקיימות בהתבסס על גודל הגידול, התפשטות והמראה מיקרוסקופי בסיסי אינן מצליחות ללכוד מדוע חלק מהמטופלים מסתדרים טוב יותר מאחרים עם אותם תרופות.
להדריך מחשבים לקרוא שכונות הגידול
החוקרים בנו את PhenopyCell כדי להפוך שקופיות רקמה מוכתמות סטנדרטיות למפת מפורטת של ״שכונות״ תאים. בעזרת כלי למידה עמוקה קיימים, הם קודם כל לימדו מחשב לזהות ולסמן תאי גידול ותאי חיסון בודדים בתמונות דיגיטליות של ביופסיות מ‑281 מטופלים שטופלו בשלוש מרכזים בארה"ב. לאחר מכן חלקו כל שקופית לאזורי גידול, רקמה סמוכה ואזורי אי‑גידול מרוחקים וחישבו מעל למאה תכונות מספריות. תכונות אלה מתארות, למשל, עד כמה צפופים תאי החיסון סביב אשכולות גידול, כמה רחוקים תאי החיסון מתאי הסרטן, עד כמה מגוון התערובת של התאים ועד כמה סדיר הסידור של התאים על פני השקופית.
דפוסים חבויים שקושרו להישרדות ותגובת תרופה
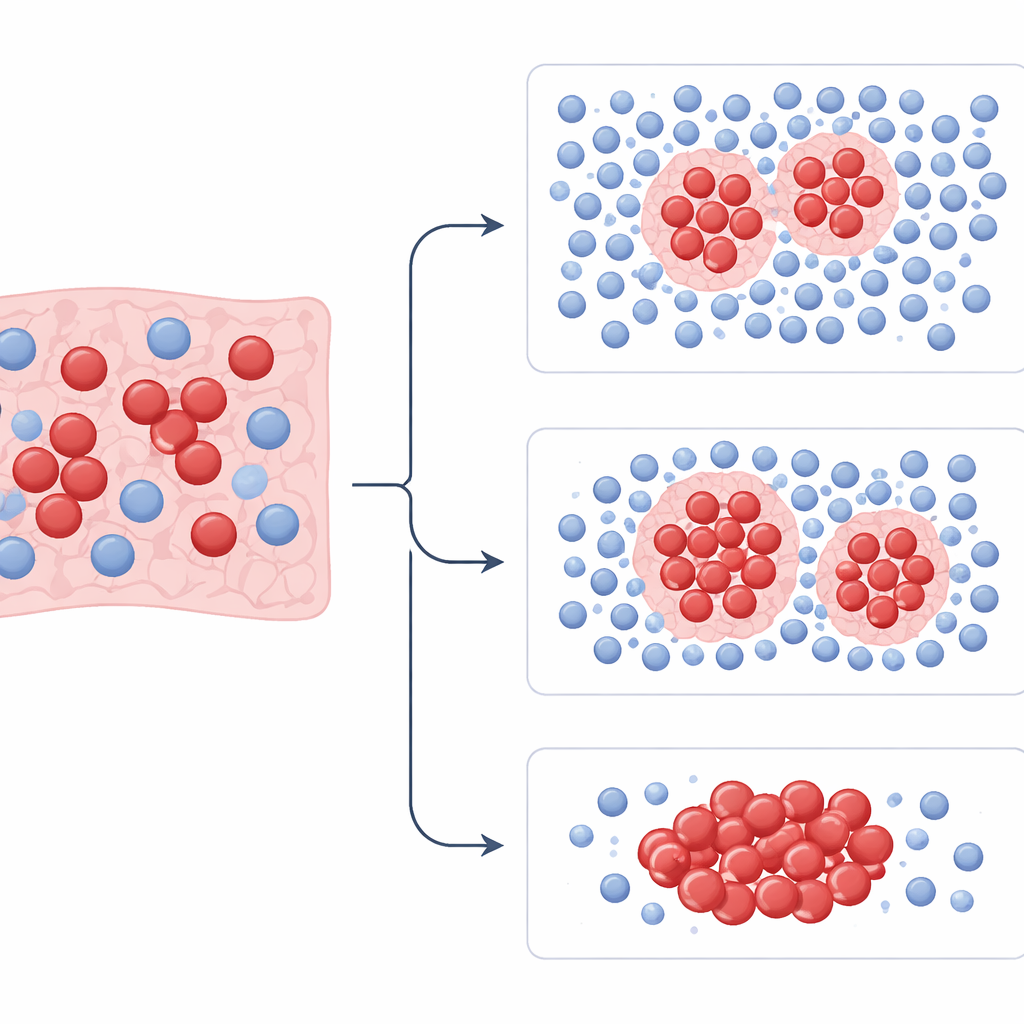
עם מדידות אלה ביד, הצוות אימן מודלים להפריד מטופלים לקבוצות בסיכון גבוה ונמוך ולחזות מי יגיב לכימותרפיית פלטינה. הם אימנו את המודלים על מקרים מבית חולים אחד ואז בדקו אותם על מטופלים מהשניים האחרים. בכל מערכי הנתונים, הדפוסים שתפס PhenopyCell היו קשורים בעוצמה להישרדות הכוללת וליעילות הכימותרפיה. מטופלים שבהם הגידולים הציגו כיסים מאורגנים רבים של תאי חיסון העוטפים בחוזקה אשכולות גידול נטו לחיות זמן רב יותר. כאלה עם תאי חיסון מפוזרים או דלילים וחלוקה לא אחידה של תאי הגידול היו בעלי סיכוי גבוה יותר למחלה אגרסיבית ותוצאות רעות. קשרים אלה נשמרו גם לאחר התחשבות בגיל, מין וגורמים קליניים נוספים, ונצפו גם במחלות במצב מוגבל וגם בנרחבות.
מעבר לקופסאות שחורות ובדיקות מיקרוסקופ שגרתיות
המחקר השווה גם את PhenopyCell למודלים חדשים של בינה מלאכותית ״בסיסיים״ ולמדדים מסורתיים של תאי חיסון הנקראים לימפוציטים חודרים-גידול. חלק מהמודלים הגדולים של למידה עמוקה הגיעו לדיוק גבוה בקבוצת האימון המקורית אך הופיעו בביצועים לא עקביים כשנבדקו על מטופלים חיצוניים, מה שהעלה חששות לגבי יציבותם. ספירות פשוטות של תאי חיסון, אם מוערכות על ידי מחשב או על ידי פאתולוג, גם הן לא חזו בצורה מהימנה את ההישרדות. בניגוד לכך, המיקוד של PhenopyCell באופן שבו תאי החיסון והגידול מסודרים במרחב — לא רק כמה מהם קיימים — סיפק אותות אמינים וקלים יותר לפרש. התכונות שהוא משתמש בהן ניתנות לקישור ישיר לרעיונות ביולוגיים כמו הדחקת חיסון, אזורים של רקמה מתה וצורות גידול משתנות.
מה זה יכול להספיק למטופלים
ללא התמחות מיוחדת, המסר המרכזי הוא ש׳ארכיטקטורת׳ הגידול — איך תאי הסרטן ומגיני הגוף תופסים את שדה הקרב — מכילה רמזים חשובים לגבי התנהגות המחלה וכיצד היא תגיב לטיפול. PhenopyCell מראה שאפשר לחלץ רמזים אלה מאותן שקופיות ביופסיה שגרתיות שנלקחות כבר בטיפול הרגיל, ללא הליכים נוספים. אמנם המחקר רטרוספקטיבי ומתבסס ברובו על מטופלים שקיבלו רק כימותרפיה, אך הוא מציע שכלים עתידיים עשויים לסייע לרופאים לזהות מי בסיכון הגבוה ביותר, מי עשוי להרוויח מטיפולים אגרסיביים או חדשניים ומי יכול להימנע מתופעות לוואי בלתי נחוצות. יהיה צורך במחקרים גדולים, פרוספקטיביים, במיוחד בקרב מטופלים המקבלים אימונותרפיות מודרניות, לפני שמערכת כזו תוכל להנחות החלטות שגרתיות, אך עבודה זו מנחה נתיב ברור לעבר טיפול מותאם אישית יותר בסרטן ריאות תאי קטן.
ציטוט: Barrera, C., Jain, P., Corredor, G. et al. Computational pathology features of immune architecture predict clinically relevant outcomes in small-cell lung cancer (SCLC). npj Precis. Onc. 10, 119 (2026). https://doi.org/10.1038/s41698-025-01225-9
מילות מפתח: סרטן ריאות תאי קטן, פתולוגיה חישובית, מיקרו‑סביבת הגידול, ארכיטקטורת תאי חיסון, חיזוי תגובת טיפול