Clear Sky Science · he
סטרטיפיקציה לפי מינון מרשם משפרת חיזוי מינוני VMAT המבוסס על למידה עמוקה בסרטן ריאה מקומי מתקדם
מדוע תכניות הקרנה חכמות חשובות
כאשר רופאים מטפלים בסרטן ריאה מתקדם באמצעות קרינה, הם הולכים על חבל דק: עליהם למסור מספיק אנרגיה לשלוט בגידול תוך שמירה על איברים סביבתיים עדינים. עיצוב תכניות כאלה איטי ומורכב ותלוי במידה רבה במיומנות המתכנן. המחקר בוחן כיצד בינה מלאכותית יכולה לחזות את דפוס הקרינה בחזה, ובחשיבותו מראה שכשמדריכים את ה-AI עם קבוצות מינון מסודרות זה הופך את התחזיות ליותר מדויקות ושמישות קליניים.
כיצד מטפלים בסרטן ריאה באמצעות קרניים ממוקדות
רוב החולים בסרטן ריאה שאינו תאי קטן מקומי מתקדם אינם מועמדים להסרה כירורגית של הגידול. במקום זאת הם מקבלים לעיתים קרובות כימותרפיה יחד עם קרניים מעוצבות באופן מדויק שמסתובבות סביב החזה בקשתות — טכניקה הידועה כ־VMAT. המטרה היא להרוות את הגידול במנה גבוהה ואחידה תוך הגבלת הקרינה לריאות, ללב, לושט ולעמוד השדרה. השגת איזון זה בדרך כלל דורשת מספר סבבי ניסוי ותעיה, שצורכים זמן ועלולים לעכב החלטות טיפול. אם הרופאים יכלו להעריך במהירות איזה דפוס מינון בר־השגה עבור מטופל נתון, הם היו יכולים לבחור את האסטרטגיה הטובה ביותר במהירות רבה יותר.
להדריך אלגוריתם לראות דפוסי מינון
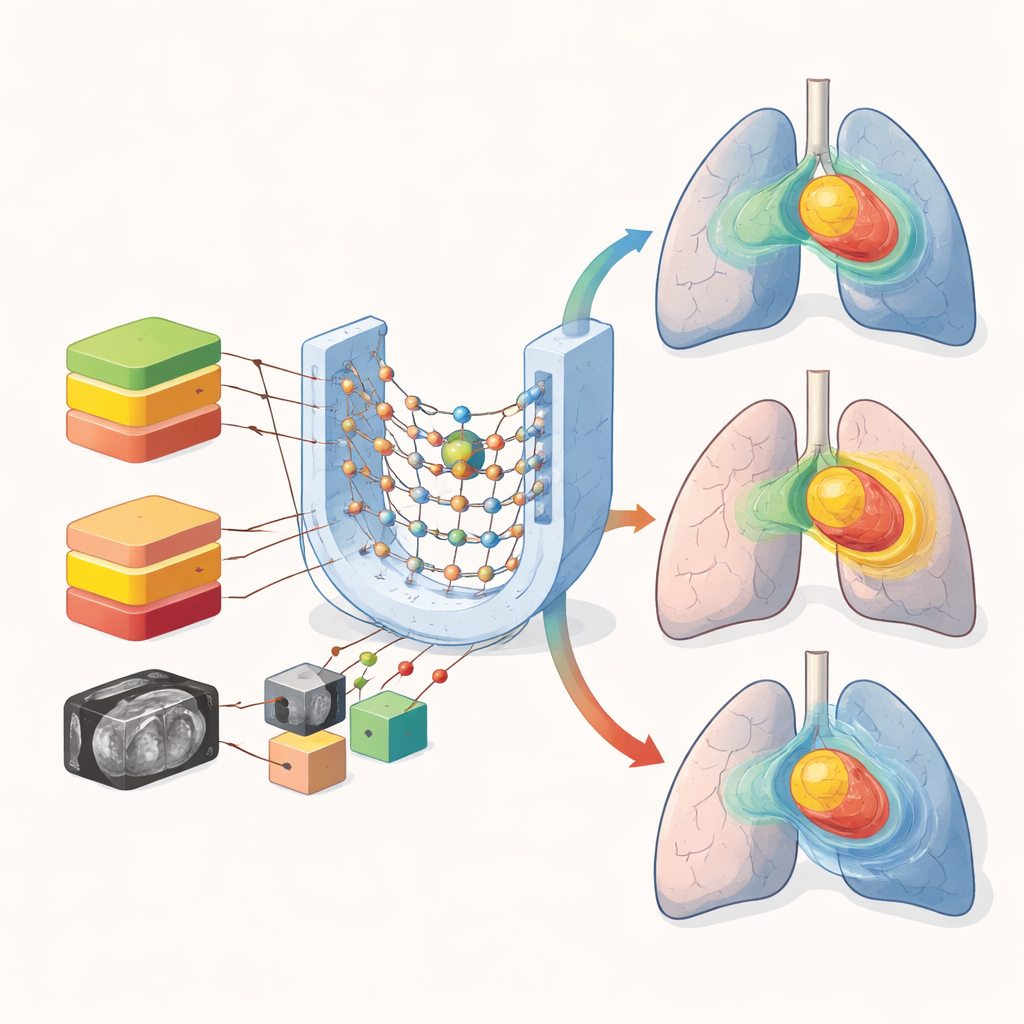
החוקרים פנו ללמידה עמוקה, סוג של בינה מלאכותית שלומדת דפוסים ישירות מתוך תמונות. הם אספו סדרות CT ותכניות טיפול גמורות מ־72 חולי ריאה שטופלו ב־VMAT. עבור כל מטופל הם חישבו מחדש כיצד אותה קונפיגורציית קרניים תמסור שלוש כמויות כוללות שונות: 50, 54 ו־60 גריי (Gy), היחידות הסטנדרטיות לקרינה. כל מקרה הומר לרשת תלת־ממדית שסימנה את הגידול, איברים מרכזיים ותמונת ה־CT הבסיסית. תשעה ערוצים של מידע אלו הוזנו ל־3D U‑Net, עיצוב רשת עצבית נפוץ שיכול ללמוד כיצד המינון נוטה לזרום דרך הגוף בהתבסס על אנטומיה.
מדוע חשוב לקבץ לפי מינון מרשם
שאלה מרכזית הייתה כיצד לטפל בעובדה שלחולים מוצאים מרשמים עם מינונים כוללים שונים. הצוות בנה ארבעה דגמי AI זהים בשאר ההיבטים. שלושה היו "מרשם בודד", כל אחד מאומן רק על תכניות ברמת מינון אחת (50, 54 או 60 Gy). הדגם הרביעי ערבב מקרים של 50 ו־60 Gy יחד מבלי לספר לרשת איזה מרשם היא רואה. כשהם נבדקו על חולים חדשים, הדגמים הספציפיים לפי מרשם השיגו התאמה טובה יותר למינון האמיתי בגידול, ושמרו הן על כיסוי והן על נקודות חמות קרובות לתכניות הקליניות, בדרך כלל בתוך מספר גריי. לעומת זאת, הדגם המעורב עשה טעויות משמעותית גדולות יותר באזורים בעלי המינון הגבוה ביותר של הגידול ובסביבת עמוד השדרה, שם המינון חייב להישאר מתחת למגבלות בטיחות מחמירות.
להגן על איברים חיוניים תוך האצת התכנון
באופן מעניין, עבור איברים רבים כגון הריאות, הלב והושט, הדגמים המעורב והמורטב (המסווגים לפי מינון) הופיעו בעלי ביצועים דומים. שגיאות ממוצעות במינון לאותם מבנים גדולים נותרו מתונות בכל הגישות. החולשה העיקרית של ערבוב המרשמים התבררה במבנים קטנים ורגישים כמו עמוד השדרה, שבהם ירידה חדה במינון היא חיונית. בדיקות ויזואליות של מפות המינון החזויות הראו שכל הדגמים תפסו את הצורה הכללית של אזור המינון הגבוה בגידול, אך ערבוב המרשמים הוביל לטשטוש גדול יותר במדרגות חדות ובאזורים בעלי מינון נמוך בריאות. ההבדלים האלה, אף שהן עדינים מבחינה מספרית, יכולים להיות משמעותיים כאשר הרופאים מחליטים האם מרשם גבוה בטוח.
מה משמעות הדבר לחולים ומרפאות
עבור החולים, עבודה זו לא מחליפה את חישוב המינון המוקפד שכבר מתבצע במערכות קליניות, אך היא עשויה לעזור להבטיח שזמן ומאמץ יתמקדו בתכניות שהן אכן בר־הגשמה ובטוחות. בהדגשה כי קיבוץ נתוני אימון לפי מינון מרשם משפר במידה ניכרת את דיוק תחזיות ה‑AI — במיוחד לגבי כיסוי הגידול והגנת עמוד השדרה — המחקר מצביע על בחירת עיצוב מעשית שיכולה להפוך את הסיוע הממוחשב ליותר אמין. עם בדיקות נוספות בקבוצות חולים גדולות ומגוונות יותר, דגמים כאלה יכולים להפוך לכלים יומיומיים שנותנים לרופאים תצוגה מהירה, מבוססת אנטומיה, של פשרות קרינה צפויות ותומכים בתכנון טיפול טוב, עקבי ומהיר יותר.
ציטוט: Chaipanya, T., Nimjaroen, K., Chamchod, S. et al. Prescription‑dose stratification improves deep learning‑based VMAT dose prediction in locally advanced NSCLC. Sci Rep 16, 8707 (2026). https://doi.org/10.1038/s41598-026-43192-6
מילות מפתח: הקרנות סרטן ריאה, חיזוי מינון בלמידה עמוקה, תכנון VMAT, אופטימיזציית תכניות טיפול, איברים בסיכון