Clear Sky Science · he
קומפוזיטים מזוּנְנִים בתנוקסיקאם מביוגלס/כיטוזן להנדסת רקמות עצם: תכונות במעבדה, שחרור תרופה ממושך ופעילות אנטימיקרוביאלית
מרפאים שברים בחומרים חכמים יותר
כשעצם ניזוקה קשות, רופאים זקוקים לעתים ליותר מאשר פלטות וברגים מתכתיים. הם צריכים להרגיע כאב ונפיחות, להילחם בחיידקים חבויים ולעודד צמיחת עצם חדשה. המחקר הזה בוחן חומר חכם יחיד שמנסה לבצע את כל אלה בבת אחת: סָקָף זעיר בדומה לעצם שמשחרר לאט תרופה אנטי־דלקתית בעודו נקשר בחוזקה לשלד ומעכב חיידקים מזיקים.
טלאי עצם מסוג חדש
החוקרים התמקדו בבעיה עיקשת באורתופדיה: פגמים גדולים בעצם הגורמים לכאב, לדלקת ולפגיעות לזיהום. כדורי־כאב ותרופות אנטיביוטיות סטנדרטיות מתפזרות בכל הגוף ועלולות שלא להגיע לריכוזים גבוהים מספיק באתר הפגוע. צוות החוקרים חתר לבנות "טלאי עצם" מקומי שיושב ישירות באזור הפגוע, תומך ברקמה המתפתחת ומשחרר תרופה בעקביות על פני שבועות, וכל זאת בדרך עדינה כלפי הגוף.
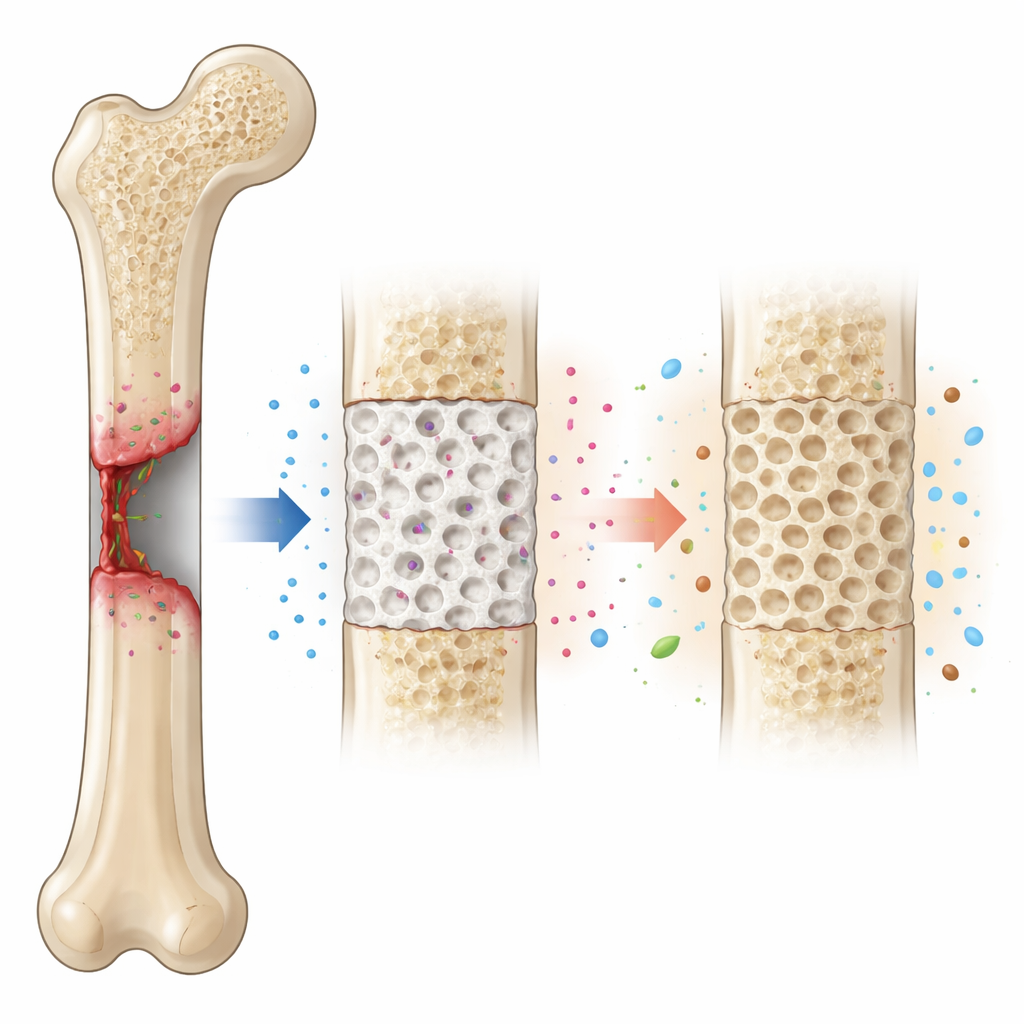
שילוב של זכוכית, סוכר טבעי והקלה על כאב
החומר שתוכנן משלב שלושה מרכיבים מרכזיים. הראשון הוא ביוגלס, סוג מיוחד של זכוכית הידוע ביכולתו להיצמד בחוזקה לעצם על ידי יצירת שכבת מינרל דקה הדומה לגבישים הטבעיים של העצם. השני הוא כיטוזן, חומר ביודגרדבילי שמקורו בקונכיות רכיכות, היוצר מבנים נקבוביים וגמישים ובעל תכונות אנטי־מיקרוביאליות עדינות. השלישי הוא תנוקסיקאם, תרופה נפוצה להקלת כאב ודלקת. באמצעות תהליך כימי הנקרא סול–ג׳ל, הטמיעו החוקרים כמויות שונות של תנוקסיקאם (1, 2 ו־3 אחוזים לפי משקל) בתערובת ביוגלס וכיטוזן, ולאחר מכן לחצו את האבקות שהתקבלו לדיסקות קטנות.
בדיקה כיצד הטלאי מתנהג בגוף
כדי לחקות את התנאים בגוף האדם, הדיסקות הושרו במשך יותר מחודש בנוזל המדמה במדויק את פלזמת הדם האנושית. שימוש בכלים מתקדמים הראה כיצד פני השטח שלהם השתנו. ספקטרוסקופיה ומדידות קרני־X הראו שכל המדגמים צמחו במהירות ציפוי של הידרוקסיאפטיט, אותו מינרל שמרכיב חלק ניכר מהעצם הטבעית. השכבה החדשה הפכה מסודרת ושופעת יותר עם הזמן, במיוחד במדגם העמוס ביותר בתרופה. תמונות ממיקרוסקופ אלקטרוני חשפו פני שטח נקבוביים מאוד המלאים בחורים מקושרים. נקבוביות כזו חשובה: היא מאפשרת לנוזלי גוף, לחומרי תזונה ולתאים היוצרים עצם לחדור ולהעגן, ועוזרת להשתיל להתמזג עם רקמה חיה.
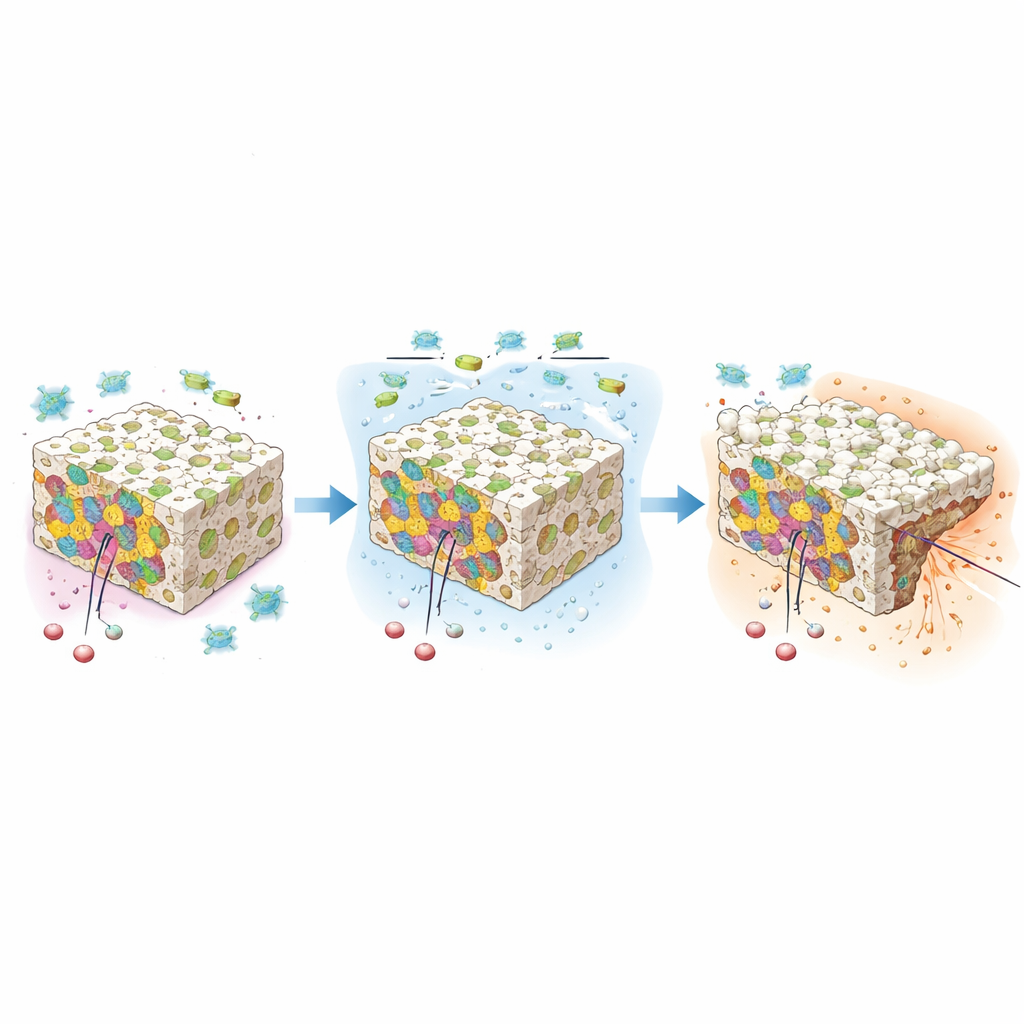
תרופה איטית ויציבה והגנה מובנית מפני חיידקים
המדענים גם עקבו כיצד תנוקסיקאם שוחרר מהדיסקות במשך 33 יום. כל שלוש הגרסאות שחררו את התרופה בשלוש שלבים: פרץ מהיר ראשוני, תקופה אמצעית של שחרור קבוע וזנב איטי יותר. באופן כללי, השחרור התאמן בהתנהגות מדורגת אפסית (zero‑order), כלומר התרופה יצאה בקצב כמעט קבוע—אידיאלי לשמירה על שליטה יציבה בכאב ובדלקת ללא קפיצות או ירידות חדות. המדגם העמוס ביותר בתרופה שחרר את הכמות הכוללת הגדולה ביותר ועדיין שמר על שליטה. במקביל, לחצו את החומרים לפלסטיות קטנות והניחו אותן על צלחות עם חיידקים. הקומפוזיטים יצרו אזורי הריגה ברורים נגד זנים גרם־חיוביים וגרם־שליליים, כולל Staphylococcus aureus ו‑Escherichia coli. המדגם עם כמות התנוקסיקאם הגבוהה ביותר הראה את האפקט האנטיבקטריאלי החזק ביותר בסך הכל.
ממה זה עשוי להצביע לעתיד תיקוני העצם
במבט כולל, הממצאים מצביעים על כך שהקומפוזיטים מביוגלס–כיטוזן טעונים בתנוקסיקאם יכולים לבצע שלושה תפקידים בו‑זמנית: הם נקשרים לעצם על ידי גידול שכבת מינרל טבעית, מספקים מקור מקומי ומתמשך להקלה בכאב ובדלקת ועוזרים לדכא חיידקים מסוכנים סביב הפציעה. אמנם העבודה בוצעה בניסויים במעבדה ולא בחולים, אך היא מרמזת על שתלים לעתיד שיפעלו לא רק כמרווחים פאסיביים, אלא כשותפים אקטיביים בריפוי—תומכים בצמיחת עצם חדשה בזמן שמספקים תרופה בדיוק במקום בו היא דרושה ביותר.
ציטוט: El-khooly, M.S., Elkelish, A., Abdel-Aal, A.A. et al. Tenoxicam-loaded bioglass/chitosan composites for bone tissue engineering: in vitro characterization, sustained drug release, and antimicrobial activity. Sci Rep 16, 8258 (2026). https://doi.org/10.1038/s41598-026-42389-z
מילות מפתח: הנדסת רקמות עצם, מבנה משחרר־תרופה, קומפוזיט ביוגלס־כיטוזן, שחרור תנוקסיקאם, ביומַטֶּרִיָּל אנטיבקטריאלי