Clear Sky Science · he
מחקר קליני‑פתולוגי רב‑מרכזי של ספקטרום הגידולים המיוקוגניים בעזרת פתולוגיה כמותית
מדוע הדבר חשוב למטופלים ולרופאי שיניים
עמוק בתוך עצם הלסת, גידולים נדירים יכולים לגדול בשקט במשך חודשים או שנים לפני שהם מתגלים. גידולים אלו, הנקראים מיוקומות ואוטודונטיות ומיוקופיברומות, אינם סרטניים, אך עלולים להתרחב, להחליש את העצם ולסבך את הניתוח. במשך עשרות שנים העריכו פתולוגים אותם בעיקר בעין, מה שהוביל לשוני בתיאור ובמיון של אותו סוג נגע בין בתי חולים. מחקר זה מביא כלים חזקים לניתוח תמונה לשקף המיקרוסקופ, ומראה כיצד בינה מלאכותית (AI) יכולה לסייע לרופאים לראות את הגידולים האלה בצורה ברורה ועקבית יותר.
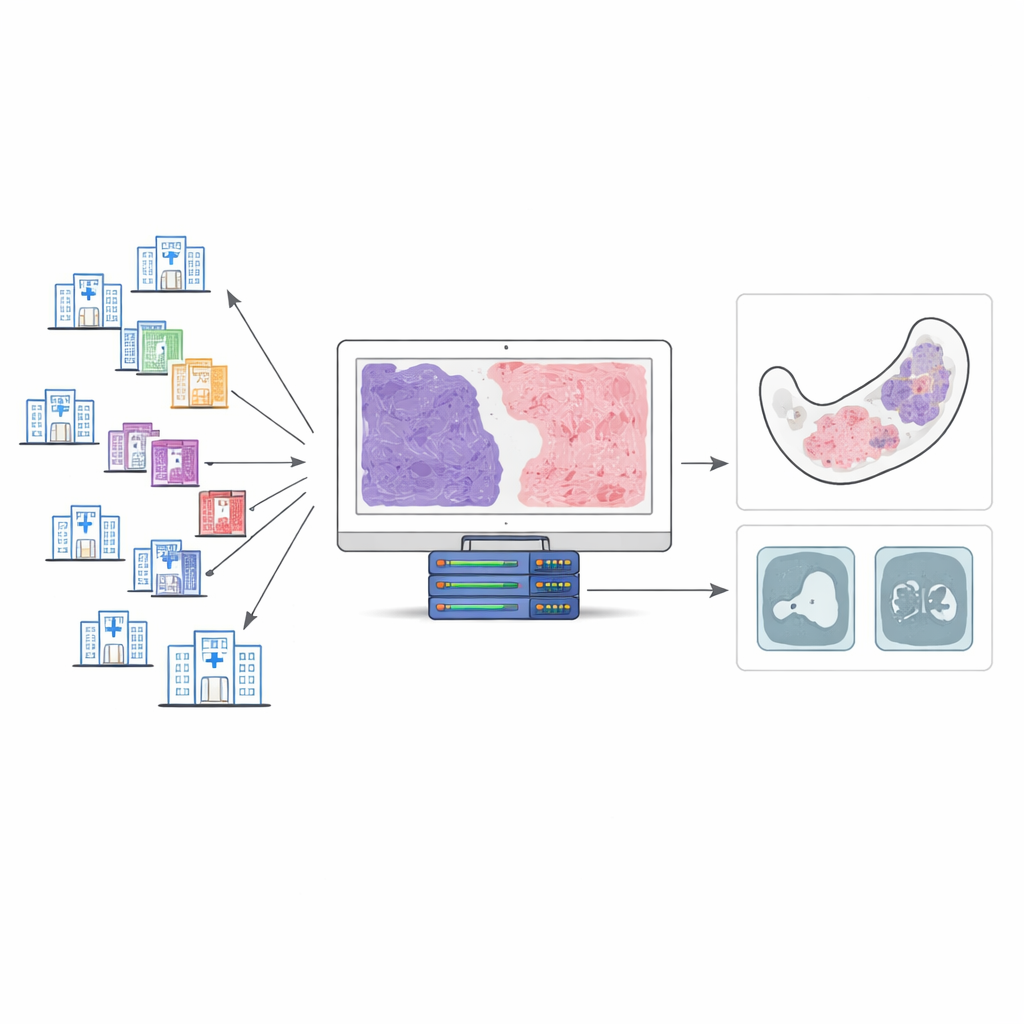
גידולי לסת נדירים שנראים מטעוּנים דמיון
מיוקומה אודונטוגנית ומיוקופיברומה אודונטוגנית מתפתחות מהרקמות המעורבות ביצירת השן. שתיהן גידולים רכים, ג'לטיניים, הממוקמים בתוך עצם הלסת. תחת המיקרוסקופ הן מכילות תערובת של אזורים רפויים, מיואידיים ורצועות צפופות יותר של רקמה סיבית. באופן מסורתי, פתולוגים ניסו להבחין ביניהן על‑ידי הערכת המידה שבה הגידול סיבי לעומת מיואידי. אך גידולים אלה נדירים, ואין כללים מוסכמים כלל‑עולמיים כמה רקמה סיבית מספיקה כדי לשנות את האבחנה מתוויה אחד לאחר. כתוצאה מכך, בתי חולים שונים עשויים לתת שמות שונים לנגעים מאוד דומים, גם כאשר למטופלים יש תסמינים ותוצאות סריקה דומות.
הפיכת Preparations של מיקרוסקופ למספרים
צוות המחקר אסף 143 דגימות רקמה ממטופלים שטופלו ב‑34 בתי חולים על פני שני עשורים, ובסופו של דבר התרכז ב‑100 מקרים שעומדים בקריטריוני איכות קשיחים. כל הדגימות הוכתמו בצביעה מיוחדת (Masson’s trichrome) שמצבעה את הרקמה הסיבית בצורה נבדלת מהרקמה הסובבת. שני פתולוגים אורליים מומחים בדקו כל מקרה בקפידה והעריכו את אחוז הרקמה הסיבית בצעדים של 10%. הערכות המומחים הללו שימשו כהתייחסות לאימון מערכת בינה מלאכותית לבצע את אותה המשימה באופן אוטומטי, אך באופן כמותי וממושמע.
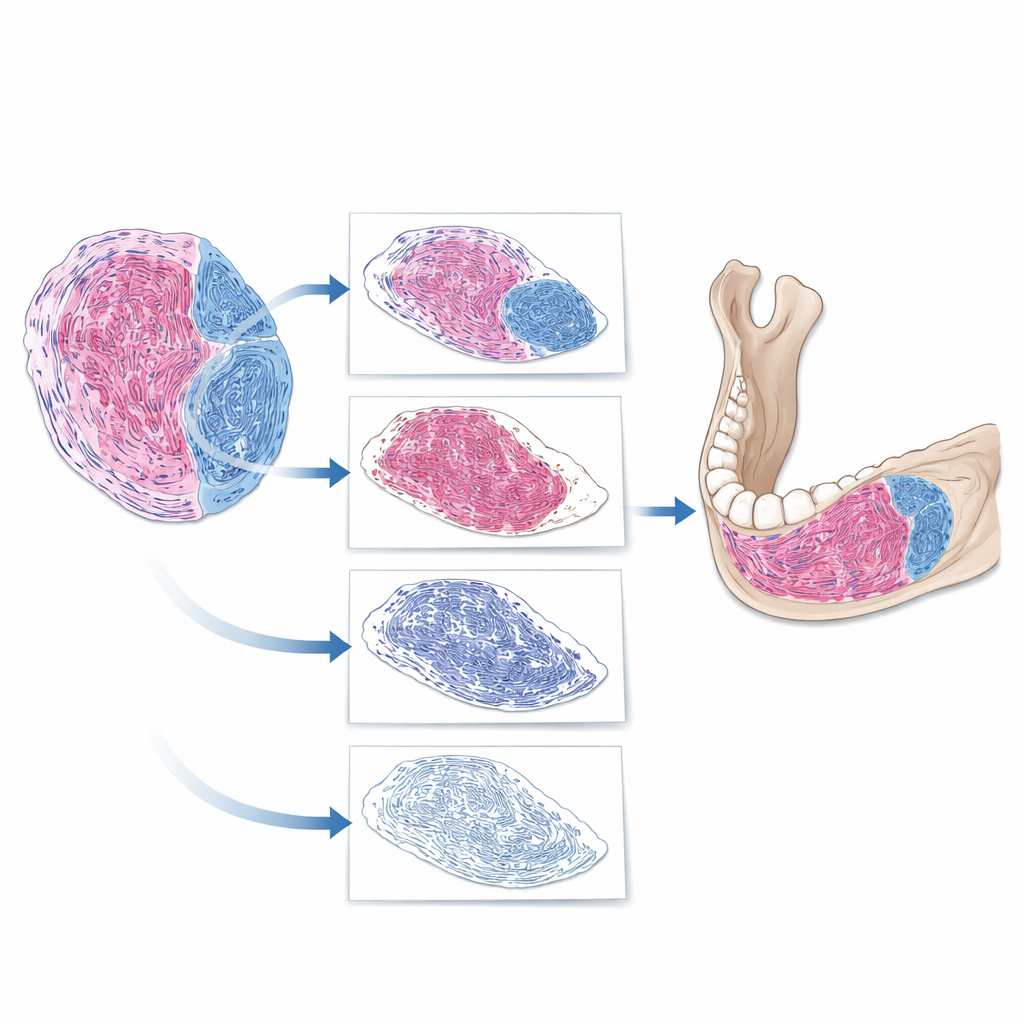
כיצד ה‑AI "קורא" פרט של גידול
הצוות בנה צינור עיבוד דיגיטלי שלב‑אחר‑שלב כדי לנתח תמונות של שלם־הפרוסה. ראשית, התוכנה הפרידה בין רקמה אמיתית לרקע הריק על השקף. לאחר מכן היא בודדה את הגידול ממבנים סמוכים כגון עצם ושיניים. לבסוף, בתוך הגידול, הוסרו גרעיני התאים והמערכת התמקדה בחומר הנותר, וזיהתה אזורים שלקחו את הצביעה הסיבית. מהנתונים האלה חישב ה‑AI שיעור של רקמה סיבית: שטח הרקמה הסיבית חלקי שטח הגידול הכולל. כאשר החוקרים השוו את הערכים שנוצרו על‑ידי ה‑AI עם דירוגי המומחים שלהם, ההסכמה הייתה חזקה, עם פיזור של כ‑10 נקודות אחוז בלבד ברוב המקרים הבודדים. זאת רמזה שה‑AI יכול לשקף באופן אמין את שיקול הדעת של מומחים, תוך ביטויו במידות מדויקות במקום רושם גס.
מה מאפיין הרכב סיבתי מגלה על המראה של הגידול
מזוּדֶה במדידות אלה, החוקרים בחנו כיצד תוכן סיבי קשור לתכונות קליניות ולהדמיות. הם מצאו שמידת הרקמה הסיבית השתנתה במידה רבה בין המוסדות, משקפת הבדלים באופן בו פתולוגים סווגו במקור את הגידולים. כאשר בחנו את מאפייני ההדמיה, דפוס אחד בלט: גידולים שהופיעו כחוליה יחידה בסריקות (נגעים יונילוקולרים) נטו להכיל שיעור גבוה יותר של רקמה סיבית מאשר אלה עם מספר חללים קטנים (נגעים מולטי‑לוקולרים). הדבר תואם את הרעיון שרקמה צפופה וסיבית יותר עשויה ליצור מסה מוצקה בעלת חלל יחיד, בעוד שרקמה רפויה ועשירה בנוזלים עשויה להתפרק למספר חללים.
בהקשר של אבחון וטיפול עתידיים
המחקר אינו נועד לשנות שמות של מחלות או להחליף פתולוגים במכונות. במקום זאת, הוא מראה כי פתולוגיה כמותית מבוססת‑AI יכולה לספק סרגל מדידה משותף לגידולי לסת נדירים ברחבי בתי חולים רבים. על‑ידי המרת המרקמים העדינים של רקמת הגידול למספרים שחוזרים על עצמם, גישה זו חושפת עד כמה אבחנות יומיומיות תלויות בשיפוט סובייקטיבי ומציעה דרך להפחית את השונות הזו. עבור המטופלים, פירוש עקבי יותר של נגעים אלה יכול לתמוך בהחלטות טיפול ברורות יותר ובהשוואת תוצאות בין מרכזים. ככל ששיטות דומות יורחבו לגידולים נדירים אחרים, מיקרוסקופיה בסיוע AI עשויה לשנות בשקט את האופן שבו פתולוגים רואים מחלה — ולהפוך את הערכותיהם לניתנות להשוואה, ולבסוף לשימושיות רבה יותר, בכל מקום שבו המטופל מטופל.
ציטוט: Harazono, Y., Fukawa, Y., Iwasaki, T. et al. Multicenter clinicopathological study of odontogenic myxoma spectrum lesions using quantitative pathology. Sci Rep 16, 11221 (2026). https://doi.org/10.1038/s41598-026-42019-8
מילות מפתח: מיוקומה שינים (odontogenic myxoma), גידולי לסת, פתולוגיה דיגיטלית, בינה מלאכותית, שיעור רקמה סיבית