Clear Sky Science · he
ניתוח זרחונים חוץ-תאיים ממקור תאי אפיתל ברונכיאלי באמצעות ציטומטריית זרימה קונבנציונלית, הדמיתית וננומטרית
מדוע בועות זעירות בריאות חשובות
הריאות שלנו מרופדות בתאים שמתקשרים באופן מתמיד עם מערכת החיסון, במיוחד כשאנחנו שואפים אבק, זיהום או חיידקים. חלק גדול מה"שיחה" הזאת מתבצע דרך בועיות זעירות הנקראות וזיקולות חוץ-תאיות — חבילות של שומנים וחלבונים שמשתחררות מהתאים. הווזיקולות הללו יכולות להחמיר או להרגיע מחלות ריאה, ואולי יום אחד ישמשו כאיתותי אזהרה מוקדמים למצבים כמו אסטמה, מחלת ריאות חסימתית כרונית (COPD) ופיברוזיס. המחקר הזה בוחן את הדרכים הטובות ביותר למדוד חלקיקים חמקמקים אלה באמצעות סוגים שונים של מכשירי לייזר מתקדמים, מתוך מטרה להפוך מדידות כאלה לפרקטיות למחקר ובדיקות קליניות עתידיות.
הודעות בלתי נראות מתאי דרכי הנשימה
וזיקולות חוץ-תאיות (EVs) הן חבילות זעירות עטופות ממברנה המשוחררות על ידי כמעט כל התאים לנוזלים כמו דם, שתן ושכבת הנוזל הדקה שמכסה את דרכי הנשימה. הווזיקולות המגיעות מתאים אפיתל ברונכיאלי אנושיים — התאים שמרפדים את צינורות הנשימה — כבר נקשרו למספר תהליכים בריאה: הן יכולות להשפיע על התפתחות אלרגיות, לסייע במאבק בזיהומים ריאתיים, לעצב את המבנה של דרכי הנשימה ב-COPD ואפילו להגביל הצטלקות ברקמת הריאה. מאחר שהן נושאות חלקי חלבונים, שומנים וחומר גנטי מהתא המקור, הווזיקולות עשויות לשמש כ"טביעות אצבע" של בריאות או מחלה בריאה, ואולי לשמש בעתיד גם כטיפולים. האתגר הוא שהן קטנות מאוד, משתנות במידה רבה ונמצאות בריכוזים נמוכים, מה שהופך אותן לקשות לזיהוי ולמניין מדויק.
מעבר לבדיקות איטיות וחלקיות
מסורתית, מדענים הסתמכו על מספר שיטות נפרדות לחקר EVs. אולטראצנטריפוגציה או כרומטוגרפיה המבוססת על גודל משמשות לבידוד; ניתוח מעקב גרגירים (nanoparticle tracking analysis) מודד תנועתן כדי לאמוד גודל ומספר; ומיקרוסקופ אלקטרונים מספק תמונות מפורטות. למרות העוצמה שלהן, גישות אלו איטיות, דורשות עבודה רבה ואינן אידיאליות לשימוש שגרתי או קליני. באופן מהותי, הן לקויות בזיהוי אילו חלבונים ספציפיים נושאת כל וזיקולה. ציטומטריית זרימה — טכנולוגיה נפוצה לניתוח דם ותאי מערכת החיסון — מציעה אלטרנטיבה יעילה יותר. היא משדרת חלקיקים אחד-אחד מול קרני לייזר, ומודדת פיזור אור (שקשור לגודל) ופלואורסצנציה (מידע מטבענים או נוגדנים). תכנונים חדשים של מכשירים מבטיחים לדחוק את יכולות ציטומטריית הזרימה לגודל הווזיקולות הקטנות ביותר, מה שמעלות את האפשרות שמכשיר אחד יוכל למדוד גודל, לספור ולאפיין EVs בהרצה אחת.
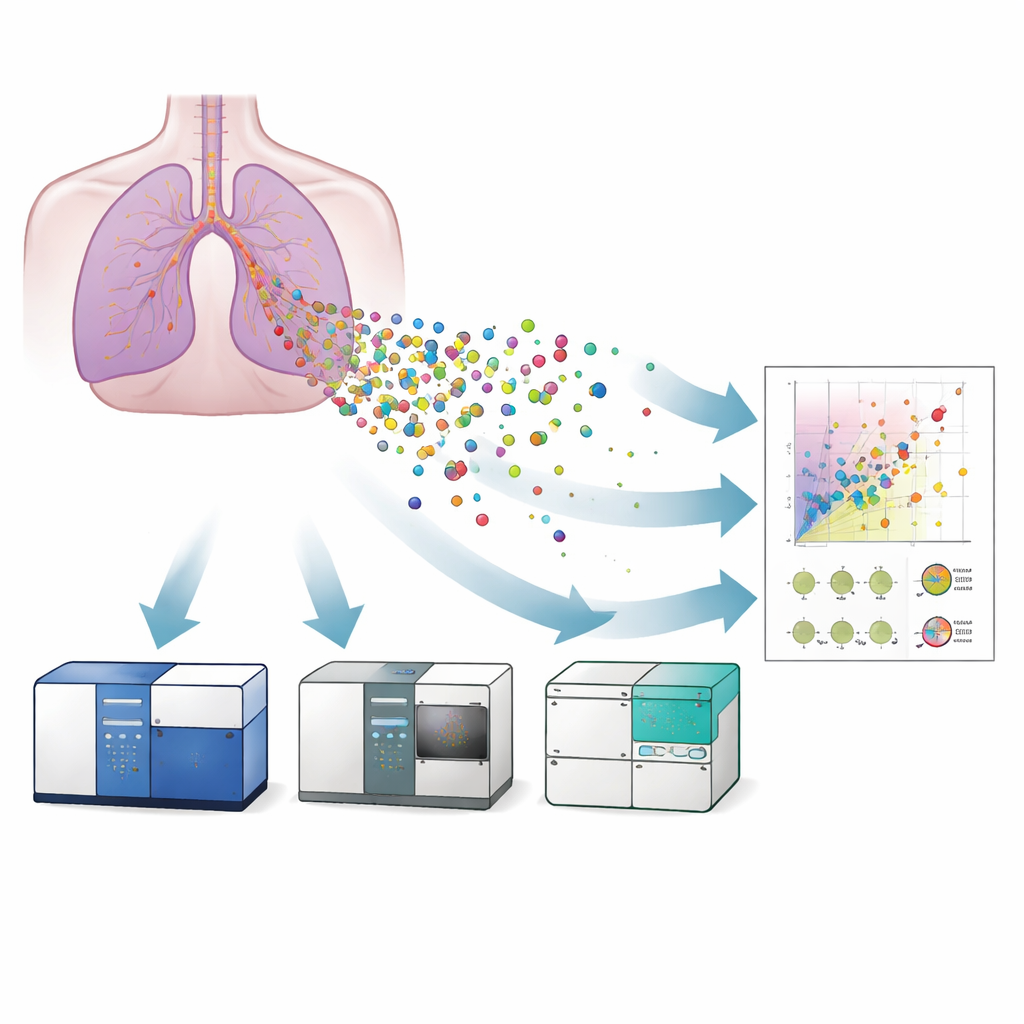
שלושה מכשירים, מטרה אחת
החוקרים השוו שלוש קטגוריות של ציטומטריית זרימה לחקר EVs שהשתחררו מדגם מעבדתי של אפיתל ברונכיאלי אנושי: ציטומטר זרימה קונבנציונלי, ציטומטר זרימה הדמיתי וציטומטר זרימה ננומטרי. תחילה אישרו את נוכחותן והמראה הטיפוסי של הווזיקולות באמצעות מיקרוסקופ אלקטרונים ומיקרוסקופ על-רזולוציוני, שהראו גם שהווזיקולות נשאו חלבוני שטח ידועים כטטרספרנינים (CD9, CD63, CD81) — סמנים סטנדרטיים לזיהוי EVs. לאחר מכן השתמשו בחרוזי ייחוס ותקני ליפוזומים מכוילים כדי לתרגם את אותות האור של כל מכשיר לגודל משוער של הווזיקולות. הציטומטר הננומטרי יכול היה לזהות וזיקולות קטנות עד כ-40 ננומטר, המכשיר ההדמיתי עד כ-55 ננומטר, בעוד שהמכונה הקונבנציונלית התקשתה מתחת לכ-120 ננומטר. משמעות הדבר היא שרק המערכות הרגישות יותר הצליחו ללכוד במלואן את הווזיקולות הקטנות ביותר, שעשויות להיות הרלוונטיות מבחינה רפואית.
תיוג וספירת הווזיקולות
כדי לוודא שהם מודדים וזיקולות שלמות וביולוגית פעילות ולא שבבים, הצוות השתמש בצבוע בשם קלצאין-AM. צבוע זה זוהר רק ברגע שהוא חוצה ממברנה שלמה ומעובד על ידי אנזימים בתוך הווזיקולה. כיולו של ריכוז הצבע נעשה בקפידה כדי לסמן את הווזיקולות בעוצמה תוך הפחתת רעש רקע, והושגה תשובה ברורה וקווית על פני דילולים של דגימות. קלצאין שוּלב לאחר מכן עם נוגדנים פלואורסצנטיים שנצמדים לטטרספרנינים על משטח הווזיקולה, מה שאיפשר למכשירים להבחין בווזיקולות שנושאות קומבינציות שונות של סמנים אלה. הקבוצה גם מדדה עד כמה כל מכשיר רגיש לתגי פלואורסצנציה אלה — כמה מולקולות נוגדן צריכות להיות נוכחות על וזיקולה כדי שהיא תתגלָה באמינות. באופן כללי, ציטומטריית זרימה הדמיתית הציעה ספי גילוי נמוכים יותר מאשר הציטומטר הקונבנציונלי, מה שהופך אותה מתאימה יותר לחלקיקים שיש עליהם מעט מולקולות סמן.
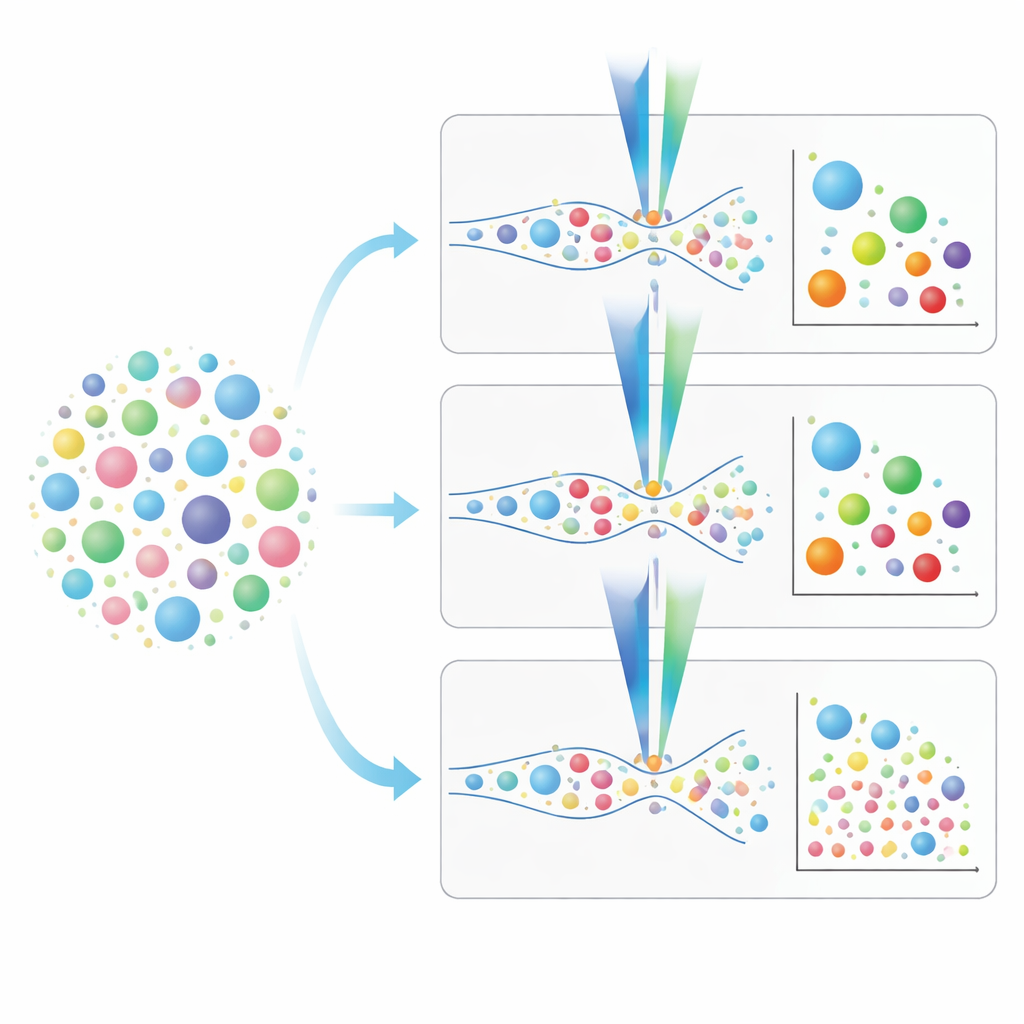
בחירת הכלי המתאים ללימודי וזיקולות ריאה
מהשוואה ישירה זו מתגבש תמונה פרקטית. ציטומטרי זרימה קונבנציונליים מהירים יותר ויכולים לנתח דגימות ללא בידוד מוקדם, אך הם מפספסים רבות מהווזיקולות הקטנות ביותר שעלולות לשאת איתותי מחלה חשובים. ציטומטרים הדמיטיים וננומטריים, אם כי איטיים יותר ובמקרה של המכשיר הננומטרי תלויים יותר בניקוי דגימה מוקדם, יכולים לראות עד גדלים קטנים משמעותית ולתמוך בהדפסת אצבע עשירה יותר של סמני משטח הווזיקולות. המחברים מציגים אסטרטגיות צביעה וכיול שלב אחר שלב, מדגישים את חשיבות הידיעה של גבול הגילוי של כל תג פלואורסצנטי, ומראים כיצד להימנע מאותות מטעות מצבעים שמסמנים גם שברים או חלקיקים שאינם וזיקולות. במילים פשוטות, הם מספקים מפת דרכים לחוקרים להחליט איזה מכשיר ופרוטוקול מתאימים ביותר לשאלות שלהם על EVs בריאה, ובכך מקדמים את האפשרות להשתמש בתקשורת המיקרוסקופית הזו ככלי מעשי להבנה, אבחון ולבסוף טיפול במחלות נשימה.
ציטוט: Hopkins, G., Browne, W., Tucis, D. et al. Bronchial epithelial cell-derived extracellular vesicle analysis using conventional, imaging, and nanoscale flow cytometry technologies. Sci Rep 16, 11162 (2026). https://doi.org/10.1038/s41598-026-41848-x
מילות מפתח: וזיקולות חוץ-תאיות, אפיתל הריאה, ציטומטריית זרימה, מחלות נשימה, ניתוח סמני ביולוגי