Clear Sky Science · he
סיווג חתכי קפואים בכל סוגי הסרטן באמצעות Vision Transformer עם תערובת מומחים רכה תחת פיקוח חלש
מדוע זה חשוב בחדר ניתוח
כשמנתחים מוציאים גוש חשוד, לעתים קרובות נשארים להם רק דקות כדי לקבוע האם כל הגידול הוסר. פתולוגים ממהרים לבחון פרוסת רקמה שהוקפאה במהירות ולמסור תשובה בעוד המטופל עדיין על שולחן הניתוחים. תהליך אינטנסיבי זה עלול להיפגע משקופיות מטושטשות, גידולים עדינים ומגבלות זמן פשוטות. המחקר המתואר כאן בוחן כיצד מערכת בינה מלאכותית (AI) יכולה לסייע לפתולוגים להבחין במהירות ובאמינות בין רקמה תמימה למסוכנת ברקמות מרובות איברים, באמצעות ציוד שמצוי בסביבת בתי חולים יום־יומית.
מבחן מהיר עם אתגרים מובנים
אנליזת חתכים קפואים היא כלי שגרתי בניתוחים מודרניים: חתיכה דקה של רקמה מוקפאת, נחתכת, מוכתמת ונבדקת במיקרוסקופ כדי לשפוט אם היא שפירה או ממאירה והאם שולי הניתוח נקיים. בשונה משקופיות קבועות במעבדה, חתכים קפואים סובלים לעתים מסדקים, קיפולים וצבעון לא אחיד. פתולוגים שונים עלולים לחלוק על מקרים גבוליים, והשעון תמיד מתקתק. בעיות אלה משמעותיות במיוחד בבתי חולים קטנים או עמוסים, שבהם מספר קטן של מומחים צריך לכסות סוגי סרטן רבים. המחברים טוענים שעוזר ממוחשב חסון יכול להפוך החלטות על חתכים קפואים ליותר עקביות, מהירות ונגישות.
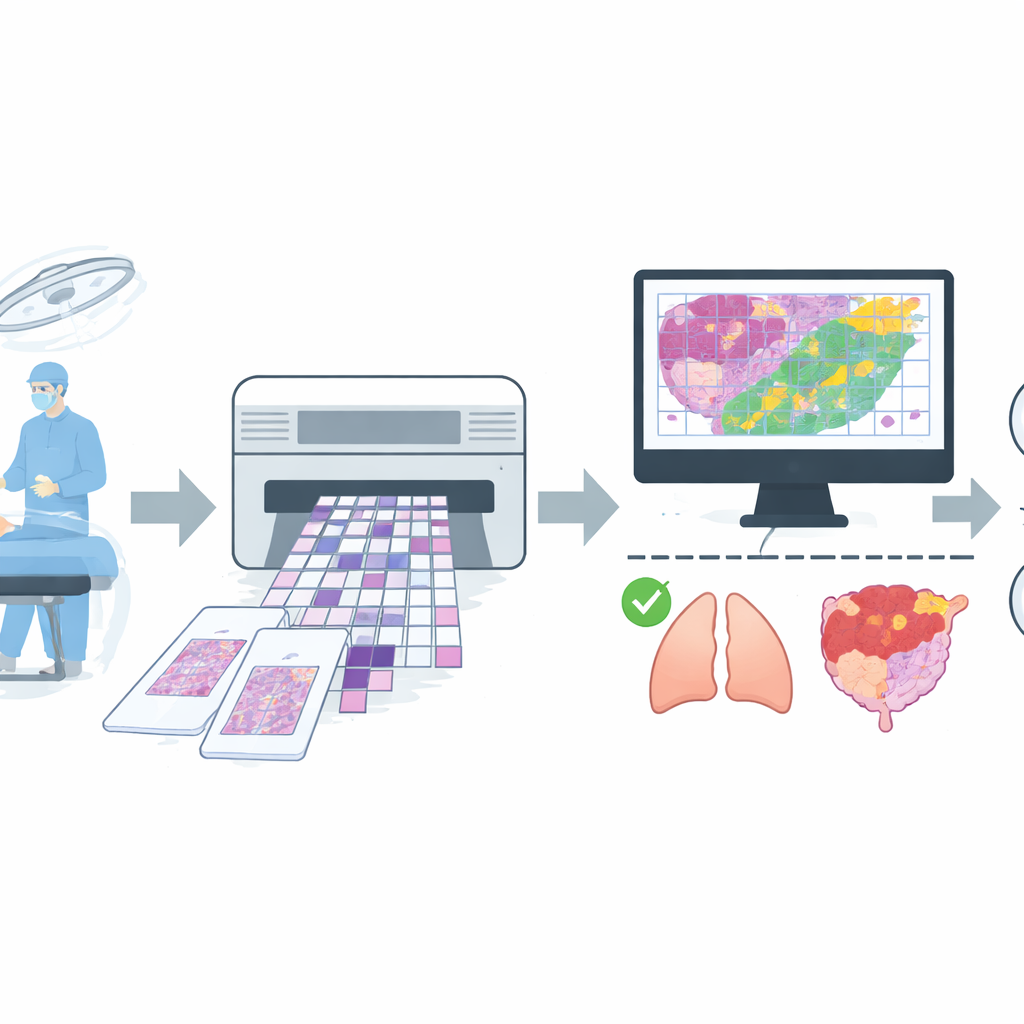
בניית מאגר תמונות רחב-טווח מהעולם האמיתי
כדי לאמן עוזר כזה, הצוות אסף אוסף גדול של תמונות דיגיטליות מניתוחים שגרתיים בבית חולים מרכזי. הם ריכזו 4,754 שקופיות שלמות של חתכים קפואים מיותר מ‑2,600 מטופלים, ואז יישמו כללי איכות מחמירים להסרת שקופיות עם ארטיפקטים חמורים או אבחנות לא ודאיות. מאגר הנתונים הסופי הכיל 4,667 שקופיות, שכל אחת מתויגה בפשטות כשפירה או ממאירה על סמך הסכמה בין קריאת החתך הקפוא המהירה ודוח החתך הקבוע המאוחר יותר. השקופיות כיסו אתרים שכיחים כגון ריאה, שד, בלוטת התריס, קשריות לימפה ואיברי רבייה נשיים, בנוסף לקבוצה מעורבת של מיקומים פחות תכופים כמו קיבה, כבד ועור. הנתונים חולקו לקבוצות נפרדות לאימון, לכיול עדין ובדיקה סופית, תוך הקפדה שהתמונות מאותו מטופל לא יופיעו ביותר מקבוצה אחת.
איך ה‑AI לומד מרמזים חלשים
החוקרים בנו את המודל שלהם על סוג של רשת עצבית הנקראת Vision Transformer, שמצטיינת בזיהוי דפוסים בתמונות גדולות. כל תמונת רקמה ענקית הופרדה אוטומטית לריבוי אריחים ותתי־קטעי תמונה כדי שניתן יהיה לעבד אותה על חומרת גרפיקה סטנדרטית. חידוש מרכזי היה החלפת חלק מהרשת ב"תערובת מומחים רכה", קבוצת סניפים מומחים קטנים שכל אחד מתמקד בדפוסים ויזואליים שונים. במקום להדליק ולכבות מומחה מסוים, המערכת מערבבת באופן רך את תרומותיהם, מה שמייצב את האימון ומשתמש טוב יותר בכמות מוגבלת של נתונים. מאחר שהפתולוגים לא שרטטו קווי מתאר של הגידולים, המודל נדרש ללמוד מפיקוח חלש: הוא ידע רק האם שקופית שלמה היא שפירה או ממאירה. אסטרטגיית למידה מריבוי דוגמאות (multiple‑instance learning) קידמה את חלקי התמונה החשודים ביותר בתוך שקופית ממאירה לשמש כדוגמאות חיוביות, מה שאפשר לרשת לכוונן בהדרגה לאזורים המידע־עשירים ביותר.
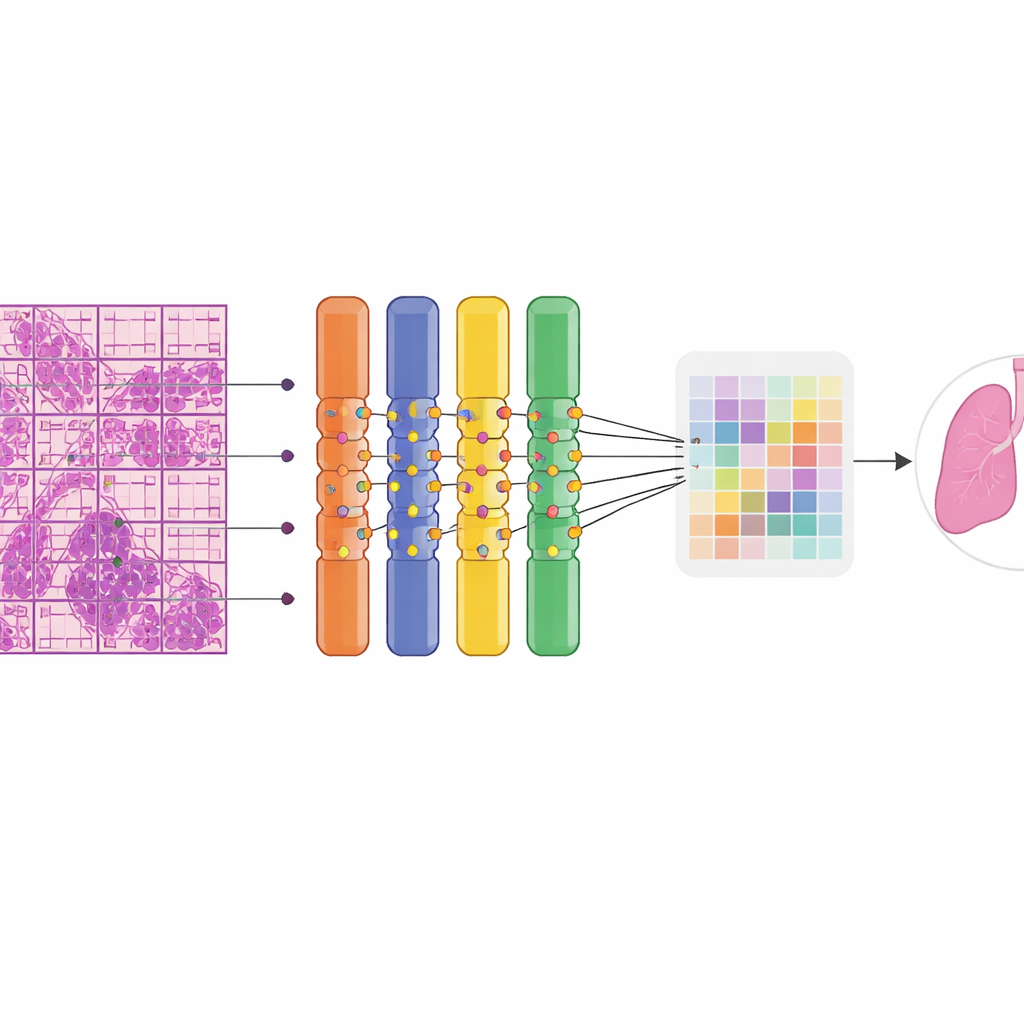
כמה טוב המערכת עובדת בפועל
בבדיקה על 669 שקופיות שלא נראו בעבר, ה‑AI הבחין בין רקמה שפירה לממאירה בדיוק גבוה. הוא סיווג נכון כ‑90% מהמקרים בסך הכל והראה יכולת מצוינת להפריד בין הקבוצות על פני ספים של הסתברות. הרגישות, הסיכוי לזהות שקופית ממאירה באמת, הייתה בסביבות ארבע מתוך חמש, בעוד הספציפיות, הסיכוי לקרוא באופן מרגיע שקופית שפירה כשפירה, הייתה אף גבוהה יותר. חשוב שהביצועים נשארו חזקים בין האיברים: המערכת זיהתה באופן מושלם את כל המקרים הממאירים של ריאה ושד במערך הבדיקה וביצעה טוב גם בקבוצות נדירות יותר כגון גידולי חיבור איברי נשים וקבוצת "אחר" מעורבת. מפות חום צבעוניות שכיסו את השקופיות חשפו שהקשב של המודל הרוכז על אזורים שפתולוגים מומחים זיהו כגידול, כולל מוקדים גרורתיים בקשריות לימפה, בעוד שהוא התעלם ברובו ממבנים נורמליים. המערכת פעלה ביעילות, צרכה פחות מ‑5 ג׳יגה־בייט זיכרון, מה שהופך אותה מתאימה לשימוש בכרטיסי גרפיקה נפוצים במקום בציוד יקר של אשכולות מחשוב.
מגבלות, מקרים שגויים וחלל לשיפור
המחברים בחנו גם היכן ה‑AI כשל. תוצאות שליליות שגויות כללו לעתים קרובות תאים סרטניים דלילים במיוחד, אזורים סרוקים מטושטשים או דלקת כבדה שהסתירה מאגרים ממאירים. תוצאות חיוביות שגויות נטו להופיע במצבים שפירים שמחקים סרטן תחת המיקרוסקופ, כגון הצמחות תגובתיות או רקמה קפואה מעוותת. מכיוון שהזרימה השוטפת של ניתוחים בדרך כלל אינה כוללת מתארים מפורטים של אזורי הגידול, הצוות לא יכל לכמת במדויק עד כמה מפות החום תואמות לסימוני המומחים, והתבסס במקום זאת על סקירה איכותנית. סוגי איברים מסוימים, כמו לשון או גידולים רכים מסוימים, נשארו תת‑מוצגים, מה שמרמז כי יידרשו מאגרים גדולים ורב‑מרכזיים כדי להרחיב את היקף המערכת.
מה זה יכול bedeutet עבור חולים ובתי חולים
בסך הכל, המחקר מראה שמערכת AI מתוכננת בקפידה יכולה לסייע במדויק ובאופן שניתן לפרש במשימה מרכזית של פתולוגיה כירורגית: להחליט, בזמן אמת, האם רקמה היא שפירה או ממאירה במגוון סוגי איברים. על ידי עבודה רק עם תוויות ברמת השקופית, ריצה על חומרה זמינה באופן נרחב והדגשת אזורים חשודים לבחינה אנושית, המודל מציע מסלול מעשי לקבלת החלטות חתכים קפואים עקבית יותר. עבור חולים זה יכול להתבטא בניתוחים בעלי מידע טוב יותר בפעם אחת; עבור בתי חולים, במיוחד אלה עם כוח מומחים מוגבל, זה מצביע על עתיד שבו כלים דיגיטליים מתקדמים מסייעים לספק טיפול סרטן איכותי יותר ושוויוני יותר.
ציטוט: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
מילות מפתח: חתך קפוא, פתולוגיה דיגיטלית, אבחון סרטן, Vision Transformer, למידה בפיקוח חלש