Clear Sky Science · he
גילוי הטריאזול-הידרוקסי כמעכב פוטנציאלי של גליאוקסלאז‑I באמצעות טכניקות תכנון תרופות במחשב
מדוע עצירת מנקה זעיר בתא עשויה להילחם בסרטן
תאי סרטן גדלים לעתים כה מהר עד שהם טובעים בפסולת שהם מייצרים. אחת מזימות ההישרדות שלהם היא צוות ניקוי פנימי שמנטרל תוצרי לוואי מזיקים משריפת סוכר. המחקר הזה בוחן כיצד לכבות חבר מרכזי בצוות הזה, האנזים גליאוקסלאז‑I, באמצעות מחשבים שמסננים עשרות אלפי מולקולות וניסויים שבודקים את המועמדים הטובים ביותר. המטרה היא למצוא נקודות התחלה חדשות לתרופות שעשויות יום אחד לאפשר לרופאים להרוס באופן סלקטיבי תאי סרטן מבפנים.
מערכת פסולת נסתרת בתוך התאים שלנו
כל תא מפרק באופן קבוע סוכר כדי לייצר אנרגיה, ותהליך זה מייצר חומר פסולת ריאקטיבי שנקרא מתילגליוקסל. בכמויות רגילות, הגוף שלנו ממיר מתילגליוקסל לחומצת חלב בלתי מזיקה דרך מערכת הגליאוקסלאז, מסלול דו‑שלבי התלוי במולקולת העזר גלוטתיון. גליאוקסלאז‑I הוא הצעד הראשון והחיוני ביותר בשרשרת זו. תאי סרטן, השורפים סוכר בקצב מואץ, תלויים במידה רבה בגליאוקסלאז‑I כדי למנוע הצטברות מתילגליוקסל לרמות רעילות. אם אנזים זה נחסם, מתילגליוקסל מצטבר ועלול לדחוף תאים פגועים לעבר מוות מתוכנת. זה הופך את גליאוקסלאז‑I למטרה אטרקטיבית לתרופות אנטי‑סרטן שפוגעות בחולשה בסיסית של מטבוליזם הגידול.
חיפוש בחלל הכימי בעזרת סיליקון וסטטיסטיקה
במקום לבדוק חומרים אקראיים במעבדה, החוקרים השתמשו בתכנון תרופות בסיוע מחשב כדי לעבור על אוסף מסחרי רחב של יותר מ‑50,000 מולקולות קטנות. תוכנה מיוחדת ניקתה ותקננה כל מולקולה, ואז חזתה את צורתה התלת‑ממדית והתנהגותה בסביבה חומצית הדומה לגוף. שלב סקר וירטואלי מהיר דירג עד כמה כל מועמד עשוי להתאים לאתר הפעיל של גליאוקסלאז‑I. הצוות יישם אחר כך כללים פשוטים לגבי גודל, מסיסות ותכונות דמויות‑תרופה כדי להוציא מן הרשימה מולקולות שסביר שלא יעבדו בגוף. תוכנית דוקינג מפורטת יותר בדקה כיצד המולקולות המבטיחות ביותר יכולות להתמצב בתוך האנזים, במיוחד כיצד הן עשויות להגיע לאטום אבץ ולהיצמד אליו — האטום שנמצא בלב הכימיה של גליאוקסלאז‑I.
דרך חדשה לאחיזת ליבת המתכת של האנזים
מאמצים קודמים לחסום את גליאוקסלאז‑I התמקדו בקבוצות כימיות מוכרות, כגון חומצות קרבוקסיליות וחומצות הידרוקסמיות, שמצטיינות בקשירת מתכות אך לעתים סובלות מחוסר יציבות או תופעות לוואי לא רצויות. המחקר הנוכחי חשף במקום זאת יחידת "תפיסת מתכת" שונה: טבעת הטריאזול‑הידרוקסי. מתוך שש‑עשרה מולקולות בדירוג גבוה שנבחרו לרכישה ולניסוי במעבדה, אחת שנושאת טבעת זו — מקודדת SPB07393SC — בלטה. בדוקינג הווירטואלי, קבוצת ההידרוקסי‑טריאזול שלה השתרעה לעבר אטום האבץ, בעוד שתי הטבעות הארומטיות שלה התקעו לכיסים שומניים סמוכים באנזים. סימולציות מחשב של המורכב על פני עשרות ננו‑שניות הראו שהמולקולה נשארת קשורה באופן הדוק, עם מרחקים יציבים, צורת חלבון קומפקטית ורשת קבועה של קשרי מימן.
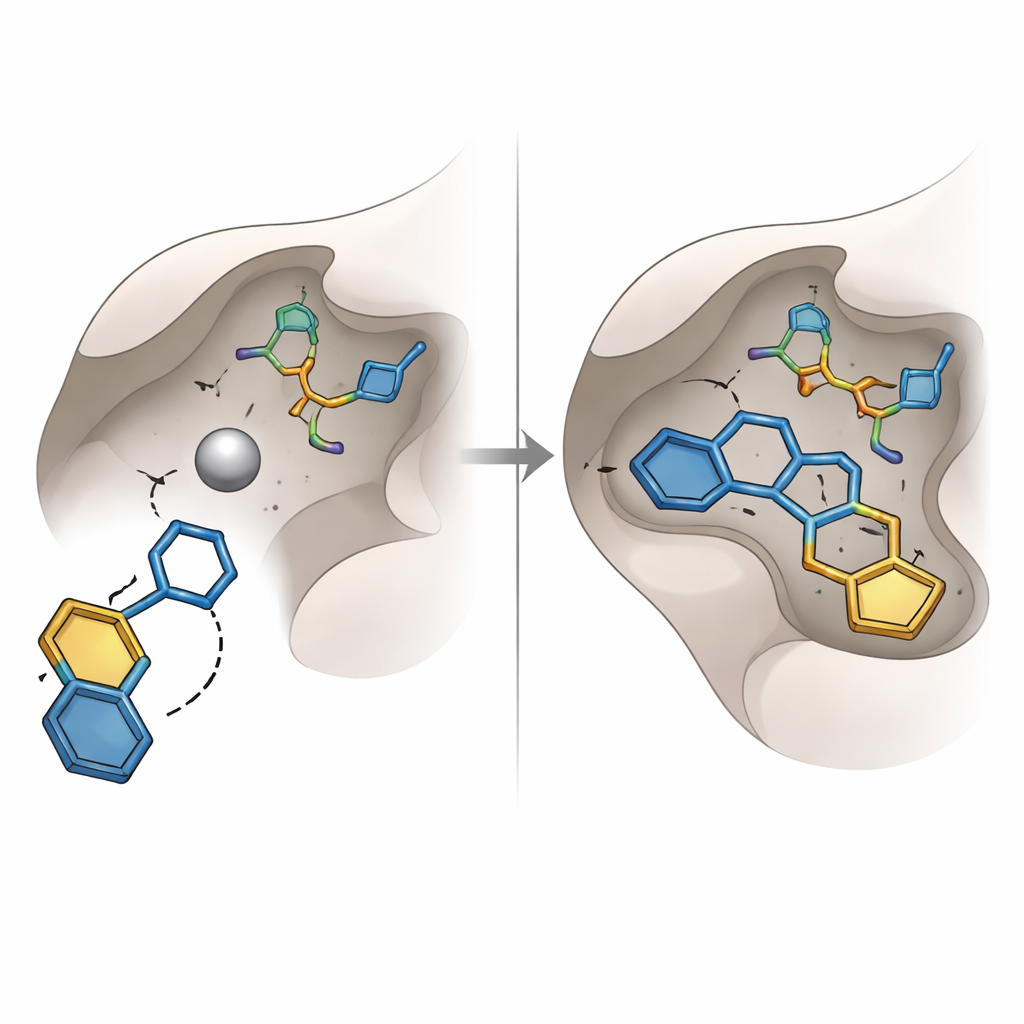
העמדת התחזיות במבחן
כדי לבדוק האם המודלים הממוחשבים מתורגמים להשפעות במציאות, הצוות מדד כמה טוב המולקולות הנבחרות האטו את פעילות גליאוקסלאז‑I האנושי המטוהר במבחן מבוסס פלטה. חמישה‑עשר מתוך שש‑עשרה המועמדים הראו רק עיכוב חלש או זניח בתנאים שנבדקו, דבר המדגיש את הסכנות שבמהימנות יתר על דוקינג סטטי בלבד. בניגוד לכך, SPB07393SC עיכב את האנזים בעוצמה משמעותית, עם פוטנטיות באמצע טווח המיקרומולרית שהופכת אותו ל"טריג" מוצק בתחילת הדרך ולא לתרופה גמורה. כלי תוכנה נוספים חזו שלמולקולה זו אמורה להיות מסיסות סבירה, ספיגה טובה, היכולת להגיע למוח אם יש צורך, וסיכון נמוך לגרימת רעילות מסוימת הקשורה לגנים או לכבד, אף על פי שניבויי בטיחות אלה עדיין דורשים אימות ניסויי.
מובן הדבר עבור תרופות סרטן עתידיות
העבודה מציגה את ההידרוקסי‑טריאזול כדרך חדשה לעגן מועמדי תרופות לאטום האבץ בליבת גליאוקסלאז‑I, ומרחיבה את התפריט של הטריקים הכימיים העומדים לרשות מתכנתי תרופות. בעוד SPB07393SC עצמו הוא רק נקודת התחלה, שילוב הכוח לחסום אנזים, ההתנהגות הצפויה בדמויות‑תרופה והקשירה היציבה בסימולציות מבוססות תנועה מצביעים עליו כיסוד מבטיח לטיוב נוסף. באופן רחב יותר, המחקר ממחיש גם את החוזקות וגם את המגבלות של סריקה מונחית מחשב: היא יכולה לצמצם במהירות ספריות כימיות עצומות למעט מתמודדים מציאותיים, אך ניסויים מעבדתיים קפדניים נדרשים כדי לגלות אילו מולקולות באמת מנטרלות את האנזים שהתאים הסרטניים סומכים עליו כדי לנהל את פסולת הרעילה שלהם.
ציטוט: Al-Qazzan, M., Al-Balas, Q., Alnajjar, B. et al. Discovery of hydroxytriazole as a potential glyoxalase-I inhibitor utilizing computer-aided drug design techniques. Sci Rep 16, 9945 (2026). https://doi.org/10.1038/s41598-026-40497-4
מילות מפתח: גליאוקסלאז I, מטבוליזם של סרטן, תכנון תרופות בסיוע מחשב, מעכבים הקושרים אבץ, דוקינג מולקולרי