Clear Sky Science · he
בחירת דוגמות אדפטיבית לגילוי מיטוזות מבוסס פרוטוטיפים שניתן להסביר בפתולוגיה דיגיטלית
מדוע זה חשוב לטיפול בסרטן
כאשר פתולוגים בוחנים דגימות סרטן תחת המיקרוסקופ, ספירת התאים הגידוליים שמחולקים באופן פעיל מסייעת להעריך עד כמה הסרטן אגרסיבי ואילו טיפולים כדאי לבחור. כיום בינה מלאכותית יכולה לזהות במהירות תאים מחלקים על גבי תמונות דיגיטליות, אך קבלת ההחלטות שלה לעתים קרובות נותרת תעלומה אפילו עבור מומחים. המאמר הזה מציג שיטה בשם בחירת דוגמות אדפטיבית (Adaptive Example Selection, AES) שמאפשרת למערכת ה-AI "להראות את עבודתה" על ידי הצבעה על מקרים אמיתיים מהעבר שתומכים או סותרים כל החלטה, ובכך להפוך את גילוי המיטוזות האוטומטי לשקוף ובעל אמינות קלינית רבה יותר.
האתגר בזיהוי תאים מחלקים
תאי גידול בחלוקה, המכונים דמויות מיטוטיות, זעירים, נדירים ובעלי מראה ויזואלי מגוון. בצביעה הסטנדרטית הורודה-סגולה הם עלולים להידמות מאוד למבנים תמימים כגון תאים גוססים או סוגי תאים חיסוניים מסוימים. מומחים אנושיים צריכים לסרוק תמונות דיגיטליות עצומות כדי למצוא אותם — תהליך איטי, מעייף ורגיש לאי-הסכמה. מערכות למידה עמוקה מודרניות יכולות לשוות או להעלות על ביצועי מומחים במשימה זו, אך הן מתנהגות כמו קופסאות שחורות: הן מפיקות ציון לכל תא חשוד ללא הסבר ברור. ברפואה, שבה החלטות טיפוליות יכולות לשנות חיים, חוסר הבהירות הזה מהווה מחסום משמעותי לשילוב ה-AI בשגרה הקלינית.
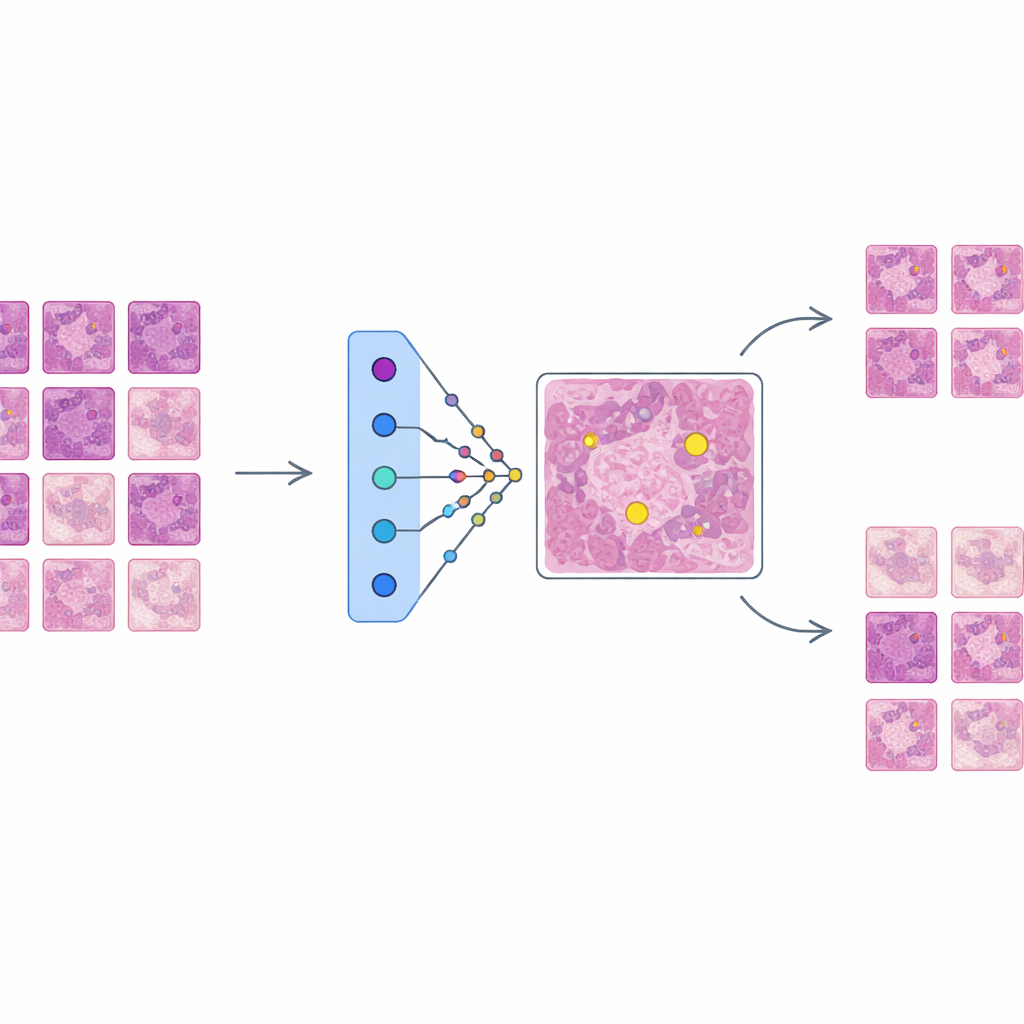
בניית גלאי חזק אך לא שקוף
החוקרים מאמנים תחילה רשת לזיהוי עצמים מהשורה הראשונה, המבוססת על ארכיטקטורת Faster R-CNN, כדי לאתר דמויות מיטוטיות בערכת נתונים רחבה ומגוונת בשם MIDOG++. תמונות אלה נאספו גם ממטופלים אנושיים וגם מכלבים, מכסות כמה סוגי סרטן ומעבדות שונות, וכוללות יותר מאחת־עשרה אלף דמויות מיטוטיות מתוייגות בקפידה. כדי לשמר פרטים עדינים, השקופים נחתכים לפאצ'ים קטנים ומוגברים באופן נרחב כדי לדמות וריאציות אמיתיות בצביעה ובדימות. הגלאי שהתקבל משיג ביצועים טובים בחלוקה לפי סוגי גידול, עם מקדמי F1 של עד 0.84, מה שמאשר שהוא מדויק אך מורכב — בדיוק סוג המערכת שדורשת הסבר טוב יותר לפני שמטפלים יבנו עליה אמון קליני.
ללמד את ה-AI להסביר את עצמו באמצעות דוגמאות
AES פועלת כשכבת פרשנות מעל הגלאי המאומן מבלי לשנות את אופן פעולתו. עבור כל אזור מועמד שהגלאי מסמן כאפשרי מיטוט, AES מחפשת בספריית פאצ'ים של רקמה אמיתית שנלקחו מנתוני האימון. מתוך ספרייה זו היא בוחרת קבוצת "דוגמות תומכות" קטנה שדומות למיטוזות אמתיות וקבוצת "דוגמות סותרות" שנראות יותר כמו תאים שאינם מיטוטיים. מאחורי הקלעים AES מטפלת בציוני הבטחון של הגלאי כנוף חלק ומשתמשת בכלי מתמטי בשם פונקציות בסיס רדיאליות כדי לקרב כיצד הביטחון הזה משתנה בסביבה של כל מקרה. נשמרים רק פרוטוטיפים שמשפיעים באופן משמעותי על הביטחון המקומי, לכן ההסבר עבור החלטה בודדת כולל בדרך כלל כעשרה דוגמאות שנבחרו בקפידה ולא מאות חפיפות חסרות רלוונטיות.
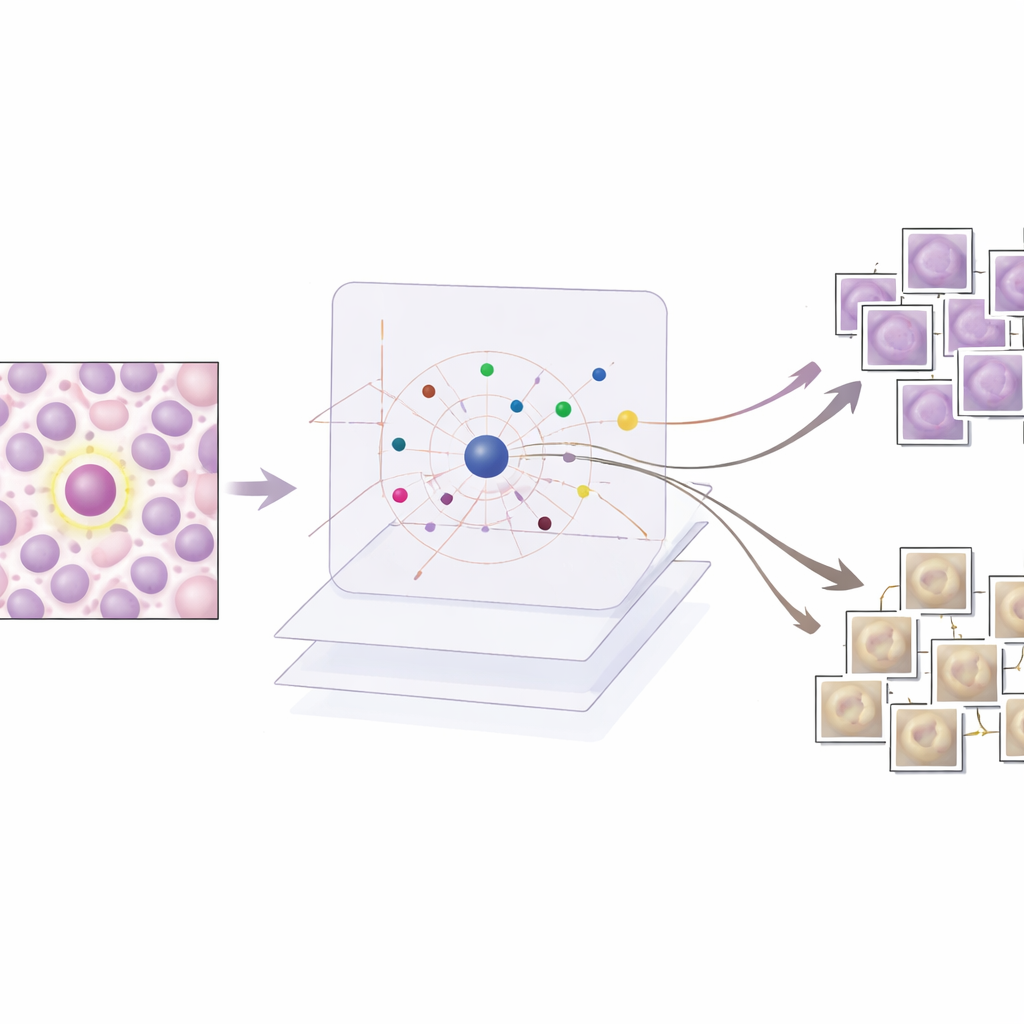
מה שהדוגמאות חושפות על החלטות ה-AI
החוקרים מעריכים את AES הן במספרים והן בסיפורים. בכמותית, הם מראים שמילון קומפקטי של כ־190 תמונות פרוטוטיפ יכול לחקות במדויק מאוד את ציוני הביטחון של הגלאי, בעוד ששומר על מספר הדוגמאות המוצגות לכל מקרה נמוך מספיק כדי שאדם יוכל לסקור אותן. באיכותי, הם בוחנים שלוש תרחישים נפוצים. כאשר הגלאי נכון באופן ברור, AES מחזירה רק פרוטוטיפים מיטוטיים שתומכים בחוזקה בהחלטה — דבר שמרגיע קלינאים. עבור אזעקות שווא, השיטה מציגה דוגמות מיטוטיות דמויות-חיצון שמסבירות מדוע הגלאי הוטעה על ידי מרקם או דפוס כרומטין דומים, לעיתים לצד פרוטוטיפים לא-מיטוטיים חלשים שמרמזים על חוסר ודאות. עבור מיטוזות שפספסו, AES נוטה להחזיר בעיקר פרוטוטיפים לא-מיטוטיים או דוגמאות אמביוולנטיות, ומציינת נקודות עיוורון בנתוני האימון ומרמזת היכן נדרשות דוגמאות חדשות או מתוייגות היטב יותר.
מקופסה שחורה לכלי שיתופי
בהנחת כל תחזית על כמה פאצ'ים של רקמה אמיתית ומתויגת, AES גורמת לגלאי מורכב של AI להתנהג יותר כמו קולגה אנושית שמצדיקה החלטות על ידי שליפת מקרים עבר. המערכת לא רק מדווחת האם סביר שתא נמצא במחלקה, אלא גם מראה מדוע וכמה בטוחה היא בכך, דרך התמהיל והשפעת פרוטוטיפים תומכים וסותרים. עיצוב זה מאפשר לפתולוגים לאשר תחזיות חזקות במהירות, למקד תשומת לב לאזורים גבוליים או מבלבלים, ולאתר דפוסי שגיאה מערכתיים שיכולים לכוון לאימון נוסף. אף על פי שפותח עבור גילוי מיטוזות, הגישה יכולה להתרחב למשימות נוספות בפתולוגיה דיגיטלית, ועוזרת להזיז את ה-AI מאוטומציה אפלה לעבר עוזר מובן-מקרה, שניתן להטיל עליו שאלות, לבטוח בו ולשכלל אותו.
ציטוט: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
מילות מפתח: בינה מלאכותית שניתנת להסבר, פתולוגיה דיגיטלית, גילוי מיטוזות, מודלים מבוססי פרוטוטיפים, אבחון סרטן