Clear Sky Science · he
מסגרת חכמה בתחום הבריאות לאבחון קרצינומה הפטוצלולרית המבוססת על לומדים מאוגדים מנתונים רפואיים בשילוב בינה מלאכותית להסבר
מדוע בדיקות חכמות יותר לסרטן הכבד חשובות
סרטן הכבד, ובפרט סוג שכיח הנקרא קרצינומה הפטוצלולרית, גדל לעיתים בשקט עד שקשה לטפל בו. רופאים כבר אוספים היקף גדול של תוצאות בדיקות שגרתיות מהמטופלים, אך להמיר את כל המספרים הללו לאות אזהרה מוקדמת קשה. המחקר הזה בוחן כיצד תוכנות מתקדמות יכולות לסנן נתונים רפואיים יומיומיים כדי לזהות אילו מטופלים נמצאים בסיכון גבוה, תוך מתן הסברים שניתן לסמוך עליהם על ידי אנשי הרפואה.
להפוך בדיקות שגרתיות לאזהרות מוקדמות
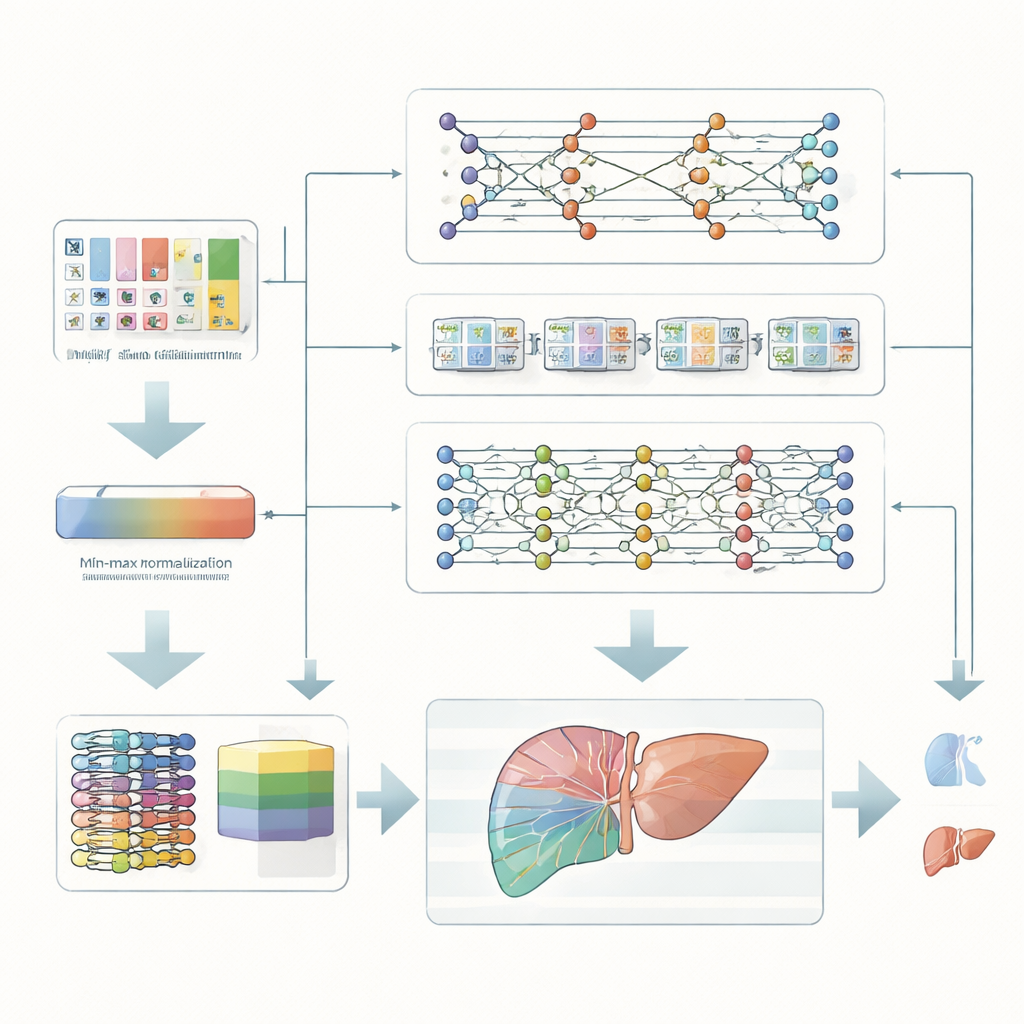
החוקרים מתמקדים במטופלים עם בעיות כבד כרוניות, הנמצאים בסיכון גבוה יותר לפתח סרטן כבד חמור. במקום להסתמך על סריקות יקרות או בדיקות גנטיות מורכבות, הם משתמשים במדידות קליניות סטנדרטיות — כגון כימיה של דם, אנזימי כבד ומידע בסיסי על מצב הבריאות. מדידות אלה ממוקנות תחילה בקפידה כך שכל המאפיינים נופלים לתחום מספרי אחיד. שלב ניקוי פשוט אך חשוב זה עוזר למודלים החישוביים ללמוד דפוסים באופן אמין יותר ומונע מערך יוצא דופן אחד להשתלט על החיזויים.
"דעות שניות" דיגיטליות רבות העובדות יחד
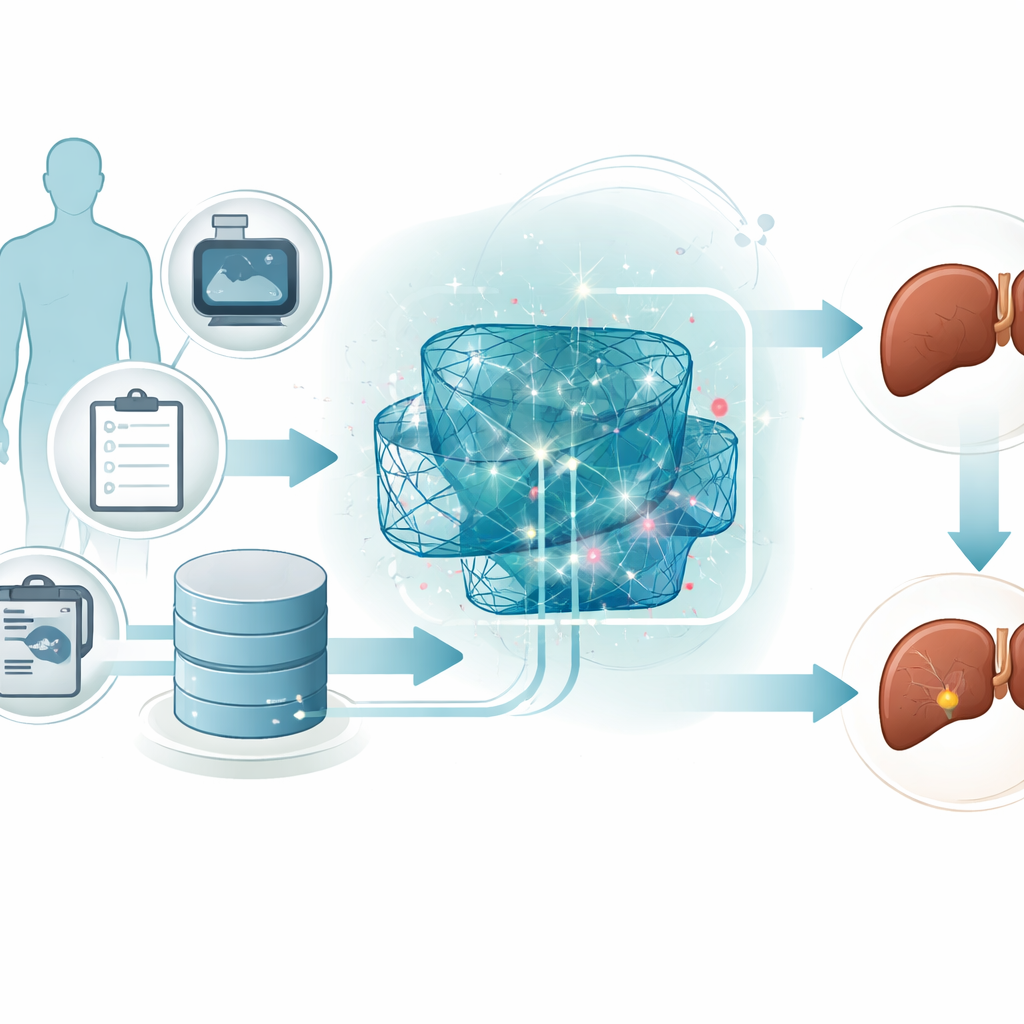
במקום להסתמך על אלגוריתם יחיד, הצוות בונה אנסמבל, או צוות, של שלושה מודלים שונים של למידה עמוקה. מודל אחד מכווץ את הנתונים כדי לחשוף את השילובים המידע־עשירים ביותר של תכונות. מודל שני נועד לזהות דפוסים שמתפתחים כסדרות, ותופס כיצד מספר מדידות יחד עשויות לרמוז על סיכון. מודל שלישי מצטבר ממספר שכבות פשוטות כדי לתפוס יחסים מורכבים ולא־קווים הנסתרות בנתונים. כל מודל נותן את שיקול דעתו בנוגע לשייכות מטופל לקבוצת סיכון גבוה או נמוך, וממזג עליון שוקל ומאחד את הדעות האלה להחלטה סופית אחת.
לפתוח את הקופסה השחורה בפני הרופא
בעוצמתן, מערכות למידה עמוקה סובלות לעיתים מביקורת על התנהגותן כ"קופסאות שחורות" מסתוריות. כדי להתמודד עם זאת, המחברים מוסיפים שכבת בינה מלאכותית מסבירה המבוססת על שיטה הידועה כ‑SHAP. טכניקה זו מעריכה כמה כל מאפיין קלטי דוחף את התחזית האישית לעבר תוצאה בטוחה יותר או מסוכנת יותר. לדוגמה, רמות מסוימות של אנזימי כבד, סימני תפקוד כבד וסימנים להסתיידות מחוץ לכבד בולטים כהשפעות משמעותיות. רופאים יכולים לראות לא רק שהמערכת מסמנת מטופל כסיכון גבוה, אלא גם אילו מדידות ספציפיות הניעו את ההחלטה ובאיזה כיוון, וכך ליצור שותפות שקופה יותר בין הקלינאי למכונה.
עד כמה הגישה עובדת?
הצוות בודק את המסגרת שלו על מערך נתונים ציבורי של 165 מטופלים שעוקבו לפחות שנה, כאשר כל אחד מסומן כשרד או לא שרד. למרות הגודל הצנוע של מאגר הנתונים, המודל המשולב לומד להפריד בין מטופלים בסיכון גבוה לנמוך בדיוק מרשים: הוא מסווג נכון בערך 98 מתוך 100 מקרים בשלבי האימון הסופיים. בהשוואה למגוון שיטות קיימות — כולל מודלים סטטיסטיים קלאסיים וכמה רשתות עצביות מודרניות — הגישה הזו לא רק משווה או עולה על דיוקה, דיוקה ואיזון בין השמטות לאותות שווא, אלא גם עושה זאת בזמן חישוב יחסית נמוך. מחקר אבלאציה, שבו מנסים כל אחד משלושת המודלים הרכיבים לבדו, מראה שכל אחד תורם ערך, אך השילוב ביניהם נותן את הביצועים הטובים ביותר.
מה זה עשוי להשפיע על טיפול המטופל
לפרקטיקה הרפואית היומיומית, עבודה זו מצביעה על כלי החלטה שהם גם חדיוּת וגם מובנים. מערכת שנבנית על קווים כאלה יכולה לעזור לסמן מטופלי כבד שמתקדמים באיטיות לאזור מסוכן הרבה לפני הופעת סימפטומים, באמצעות נתונים שכבר נאספים במספר רב של מרפאות. במקביל, ההסברים שלה — המדגישים אילו תוצאות בדיקה וסימנים קליניים הם המשמעותיים ביותר עבור אדם נתון — יכולים לתמוך ברופאים תוך עדכון תכניות טיפול ושיחה על סיכונים עם המטופלים. אף על פי שהמחקר עדיין סומך על מאגר נתונים יחיד ויחסית קטן ומוותר על נתוני הדמיה וגנטיקה, הוא מציע מפת דרכים למודלים חכמים ושקופים יותר לסיכון לסרטן שיכולים, עם נתונים גדולים ומגוונים יותר, להפוך יום אחד לבעלי ברית שגרתיים במאבק בסרטן הכבד.
ציטוט: Alqaralleh, B.A.Y., Alksasbeh, M.Z., Kulakli, A. et al. An intelligent healthcare framework for hepatocellular carcinoma diagnosis based on aggregated learners from biomedical data utilising explainable artificial intelligence. Sci Rep 16, 9357 (2026). https://doi.org/10.1038/s41598-026-39871-z
מילות מפתח: סרטן הכבד, בינה מלאכותית רפואית, איבחון מוקדם, בינה מלאכותית מסבירה, תמיכה בקבלת החלטות קלינית