Clear Sky Science · he
למידת מכונה ניתנת לפירוש שמסבירה את עיכוב האנזים קרבוניק אנדרז באמצעות חיזוי קונפורמלי והסברים נגד-פסיכולוגיים
מדוע תרופות סרטן חכמות יותר חשובות
תרופות נגד סרטן נוטות להתנהג ככלים גסים: בעוד שהן תוקפות תאי גידול, הן עלולות לפגוע גם ברקמות בריאות ולגרום לתופעות לוואי חמורות. גישה מבטיחה לחדד את המטרה היא לחסום וריאנטים ספציפיים של האנזים קרבוניק אנדרז, המסייעים לגידולים לשרוד בסביבות דלות חמצן. עם זאת, כמה ווריאנטים של אנזים זה דומים כמעט זה לזה, מה שמקשה לעצב תרופות שפוגעות ב"הרעים" שבגידול מבלי להפריע ל"טובים" הנמצאים בכל הגוף. המחקר הזה מראה כיצד למידת מכונה ניתנת לפירוש יכולה לסייע לחוקרים לנווט באתגר הזה ולעצב מועמדים לתרופות סלקטיביות ובטוחות יותר.
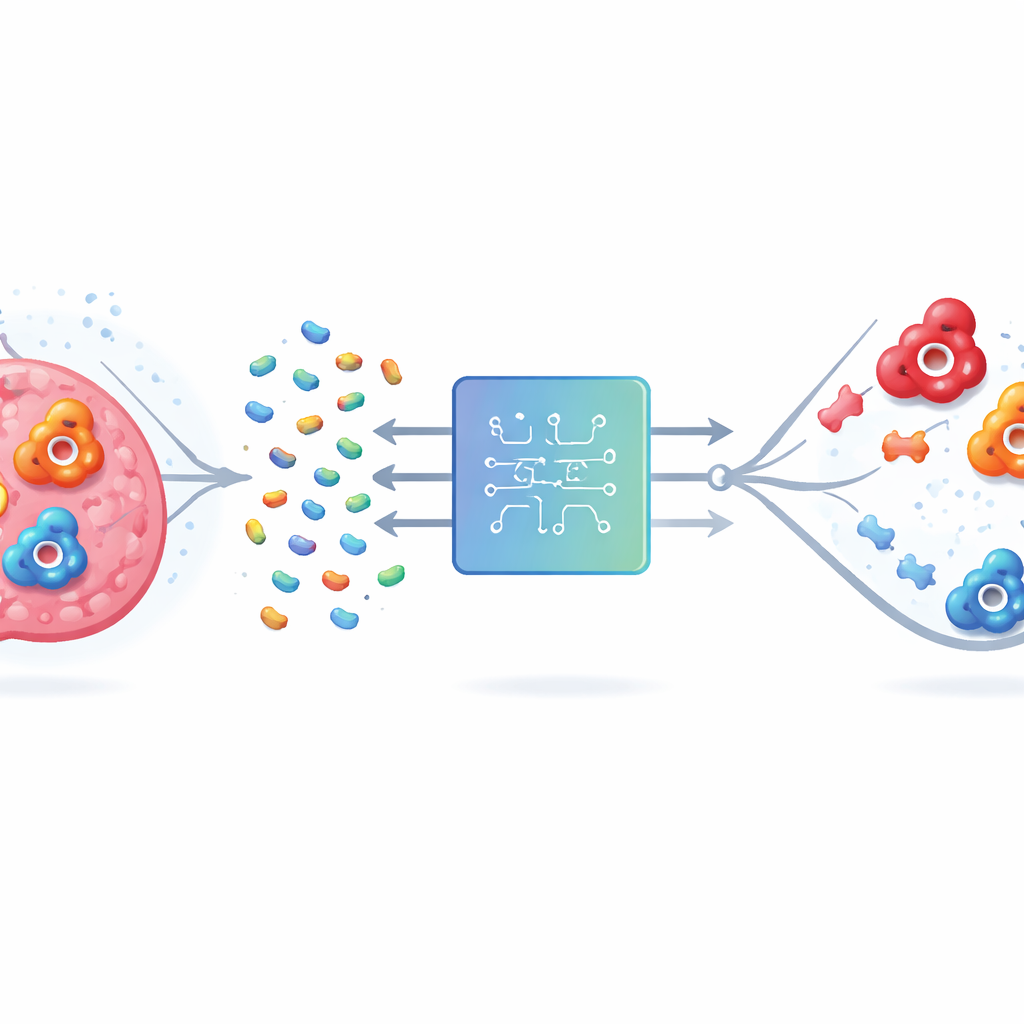
הבעיה של פגיעה במטרה הלא נכונה
הקרבוניק אנדרז האנושי (hCA) קיים בצורות רבות, או איזו-פורמים. שניים מהם, IX ו-XII, מקושרים להישרדות תאי סרטן בגידולים רעובי חמצן, ולכן חסימתם עלולה להאט את המחלה ולשפר טיפול. אבל איזו-פורם II נפוץ ברקמות בריאות ואתר הפעילות שלו דומה מאוד ל-IX ול-XII. תרופות הקושרות את שלושתם עלולות לגרום לבעיות לא רצויות כמו חמצת מטבולית והפרעות בראייה. שיטות מעבדה ומחשב מסורתיות מתקשות מכיוון שאנזימים הם מולקולות גדולות ומורכבות, ומספר האפשרויות של תרכובות דמויות-תרופה הוא עצום. בדיקה ממצה של כולן, בין במעבדה ובין במחשב, פשוט אינה אפשרית.
בניית בסיס נתונים נקי ואמין
המחברים פתרו זאת באמצעות הרכבת מאגר נתונים מטוהר בקפידה של אלפי מולקולות שנבדקו כנגד hCA II, IX ו-XII מתוך מאגר ChEMBL. הם סטנדרטיזו מבני כימicals, הסירו מדידות חשודות והתמקדו בחומרים החולקים קבוצת קשירה לאבץ אופיינית למחלקה זו של מעכבים. באמצעות ספים מחמירים תוייגו מולקולות כפעילות באופן ברור או כלא פעילות באופן ברור והועברו מקרים שוליים שעלולים לבלבל את המודלים. מאחר שהיה הרבה יותר מולקולות לא פעילות מאשר פעילות, הם איזנו את הנתונים כדי שלמנingi של הלמידה לא יהיה קל להעדיף את המחלקה הרובית. הם גם השתמשו בשיטת "מבוססת שלד" לחלוקה של הנתונים כך שמערכי האימון והמבחן יכללו מסגרות מולקולריות ליבה שונות, מה שנתן תמונה מציאותית יותר של יכולת המודלים להתמודד עם תרכובות חדשות באמת.
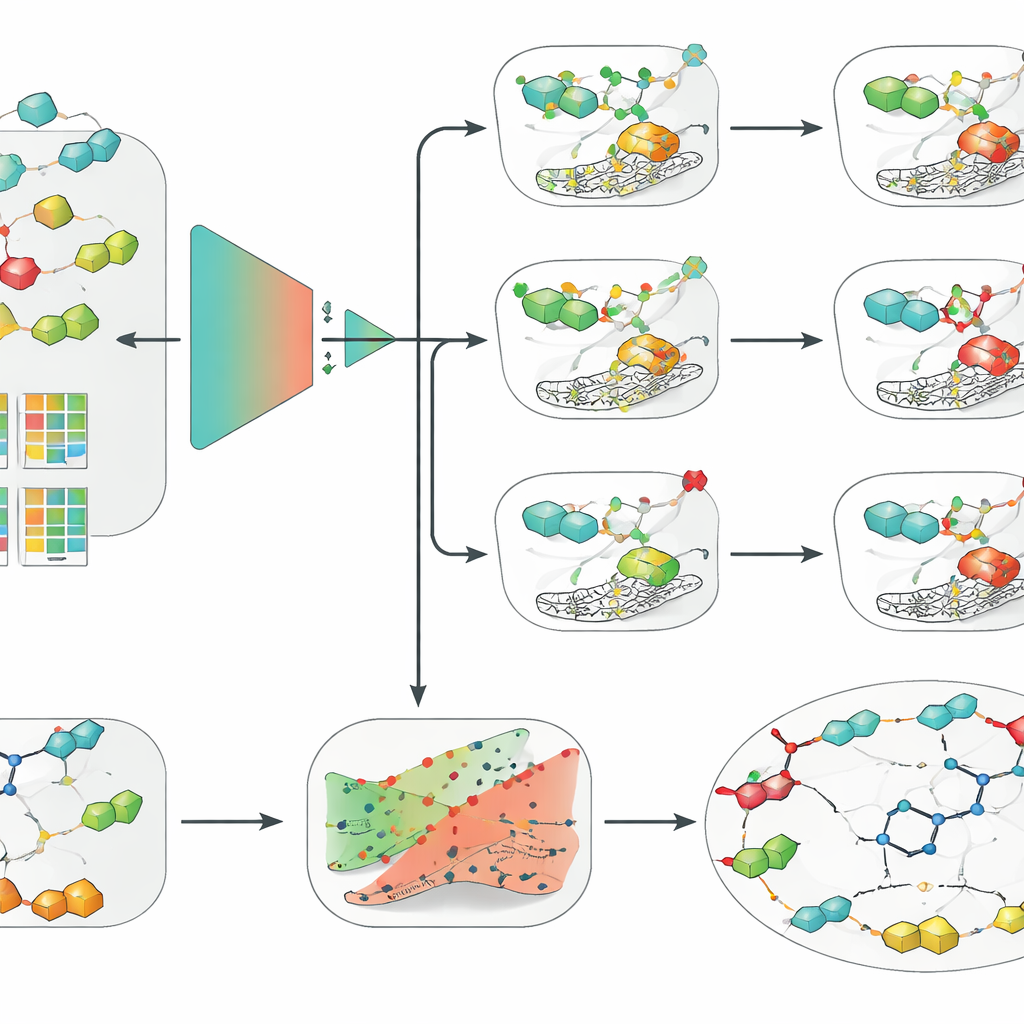
מודלים פשוטים מנצחים למידה עמוקה כאשר הנתונים מוגבלים
עם מאגר הנתונים הממוין הזה, הצוות השווה מגוון רחב של גישות, משיטות למידת מכונה קלאסיות כמו רגרסיה לוגיסטית, יערות אקראיים ומכונות תומך-וקטור (SVM) ועד רשתות נוירונים עמוקות מודרניות, כולל מודלים גרפיים הפועלים ישירות על מבני מולקולות. הם שילבו זאת עם מספר דרכים לקידוד מולקולות, כגון תיאורים מותאבים ידנית, טביעות אצבע מבוססות-מפתח והטמעות נלמדות ממודל שפת כימיה. בשש מדינות האיזו-פורמים ותחת ההערכה המחמירה המבוססת-שלד, שילוב אחד בלט בעקביות: SVM שהוזן בטביעות אצבע של חיבוריות מורחבת, שיטה מובנית לתיאור סביבות כימיות מקומיות בתוך מולקולה. בהפתעה, תצורה פשוטה יחסית זו עלתה על מודלים גרפיים ולמידה עמוקה אופנתיים יותר, מה שמדגיש שאיכות הנתונים, אימות זהיר ותיאורי מולקולות טובים יכולים להיות חשובים יותר מהמורכבות האלגוריתמית כאשר מערכי הנתונים הם בגודל מתון.
הוספת ביטחון מהימן והסברים ידידותיים לאדם
החוקרים עטפו את מודל ה-SVM הטוב ביותר שלהם בשתי שכבות נוספות שנועדו להפוך את תחזיותיו לשימושיות יותר בגילוי תרופות אמיתי. ראשית, הם יישמו מסגרת שנקראת חיזוי קונפורמלי, שאינה מספקת תשובה חד-משמעית אלא אזור של תוצאות סבירות יחד עם שיעור שגיאה מובטח. זה מאפשר למדענים לכוונן עד כמה ברירה זהירה שהם רוצים שהמודל יהיה ולזהות מקרים שבהם המודל באמת לא בטוח. שנית, הם השתמשו בהסברים נגד-מקריים כדי להפוך את ההסקה של המודל לאינטואיטיבית יותר. עבור מולקולה נתונה, הם ייצרו אנלוגים קרובים שמחליפים את התחזית מפעילה ללא פעילה, או להיפך. בחינת זוגות אלה עבור המועמד הקליני SLC-0111, החוסם בררני את IX ו-XII אך לא את II, גילתה מחדש באופן עצמאי תובנה חשובה בכימיה רפואית: שינויים קטנים ב"זנב" של המולקולה משנים באופן חזק את האיזו-פורם המועדף לקשירה.
מאלגוריתמים לכלים מעשיים לעיצוב תרופות
כדי להפוך את הגישה לנגישה, המחברים ארזו את שלוש מודלי ה-SVM, שכבת אי-הוודאות ומנוע ההסברים נגד-מקריים לכלי גרפי שנקרא CAInsight. משתמש יכול להזין ייצוג טקסטואלי של מולקולה ובקליק אחד לקבל תחזית פעילות כנגד hCA II, IX ו-XII, הערכה עד כמה תחזית זו אמינה והצעות לשינויים מבניים שעשויים להגדיל או להפחית פעילות. בעוד שהמודלים מתמקדים בסיווג מולקולות כפעילות או לא פעילות במקום לחזות עוצמה או סלקטיביות מדויקת בשלב אחד, הם כבר משחזרים התנהגות ידועה של מועמדי תרופות אמיתיים ומבדילים שינויים מבניים עדינים. המחברים מציינים כי מאגרים גדולים ואחידים יותר, בנוסף לניתוח מעמיק של האופן שבו נבחרים ספי פעילות, יכולים לשפר עוד יותר את הביצועים.
מה משמעות הדבר עבור תרופות סרטן עתידיות
בהגדרה פשוטה, עבודה זו מראה שמודלים של למידת מכונה שנבנו בקפידה ומוסברים היטב יכולים לסייע בכימאים לעצב תרופות סרטן המבדילות טוב יותר בין מטרות אנזים דומות. באמצעות שילוב סטטיסטיקה חזקה, הערכות אי-וודאות ודוגמאות אינטואיטיביות של "מה אם", המסגרת לא רק חוזה אילו מולקולות סבירות לעבוד אלא גם מציעה מדוע. סוג זה של בינה מלאכותית שקופה יכול לזרז סריקה וירטואלית, לתמוך בעיצוב גנרטיבי של תרכובות חדשות ולהפחית את המאמץ של ניסוי וטעייה במעבדה, ובסופו של דבר לסייע בגילוי טיפולים סלקטיביים ובטוחים יותר לחולים.
ציטוט: Ghamsary, M.S., Rayka, M. & Naghavi, S.S. Interpretable machine learning rationalizes carbonic anhydrase inhibition via conformal and counterfactual prediction. Sci Rep 16, 8419 (2026). https://doi.org/10.1038/s41598-026-39771-2
מילות מפתח: מעכבי קרבוניק אנדרז, למידת מכונה ניתנת לפירוש, סלקטיביות תרופתית, חיזוי קונפורמלי, הסברים נגד-מקריים