Clear Sky Science · he
השפעת חימצון של RNA מסוג G-quadruplex על הדינמיקה הקונפורמציונית שלו והאינטראקציה עם החלבון TDP-43 הקשור ל-ALS
מדוע זה חשוב לבריאות העצבית
השחמת עצבים מוטורית-צידית (ALS) היא מחלה קטלנית שבה תאי העצב השולטים בתנועה מתים בהדרגה, אך שורשיה של הפגיעה הסלקטיבית הזו נשארים מסתוריים. המחקר שואל שאלה פשוטה אך מהותית: ככל שאנו מזדקנים והתאים שלנו חשופים לנזק כימי בסגנון "חלודה", האם בלאי זה על ה-RNA — ההעתק הפעיל של הגנים — מופרע מסרים חיוניים השומרים על חיי תאי העצב המוטוריים? באמצעות התמקדות בצורת RNA מקופלת מיוחדת ובחלבון מרכזי הקשור ל-ALS בשם TDP-43, העבודה חושפת כיצד צלקות כימיות זעירות עלולות לתרום לתנאים שמקדמים מחלה. 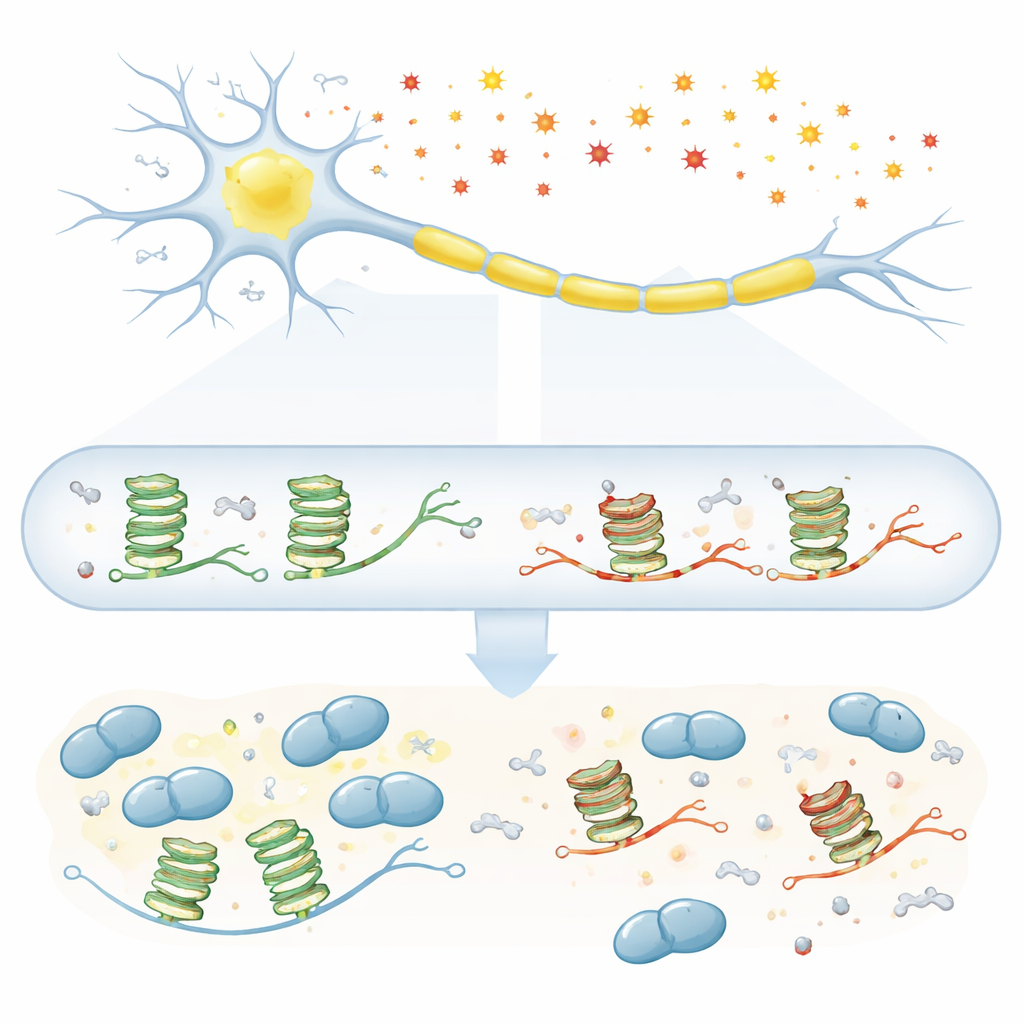
קשרון RNA שביר בלב תאי העצב המוטוריים
תאי עצב מוטוריים נשענים על הובלה מרחוק של מסרי RNA לאורך האקסון כדי שפרוטאינים ייוצרו באתר, סמוך למפגשים עם השריר. רבות מההודעות האלה נושאות "קשר" מבני מיוחד שנקרא G-quadruplex, שנבנה מתיבות של הבסיס גואנין. חלבונים כמו TDP-43 מזהים קשר זה ומצמידים את ה-RNA לגרנולות תחבורה שנעות לאורך האקסון. הבעיה היא שגואנין הוא גם הבסיס שהכי קל לחמצון כאשר התאים נחשפים למולקולות חמצון תגובתיות, שהצטברותן עולה עם ההזדקנות. רמזים קודמים הצביעו על כך ש-G-quadruplexes ו-TDP-43 הם מרכזיים ב-ALS, אך לא היה ברור בדיוק כיצד חימצון של קשרים אלה עלול להפריע לשותפותם.
צפייה בלחץ חמצוני המעוות צורות RNA
החוקרים חשפו תחילה תאי נוירובלסטומה אנושיים לפרוקסיד מימן, סוכן חמצון שכיח, ולאחר מכן בדקו את מצב המבנים של G-quadruplex. האותות ממחט הרגישה ל-G-quadruplex ירדו כאשר הלחץ החמצוני עלה, מה שמעיד על כך שקשרים קומפקטיים אלה מאבדים את צורתם הרגילה. כדי לקשור את התצפיות לכימיה, הצוות בנה RNA סינתטי המהווה G-quadruplex והוסיף בכוונה כמויות שונות של 8-oxoguanine, צורה מחומצנת מוכרת של גואנין הנמצאת בתאי עצב מזדקנים וברקמות ALS. באמצעות מערך כלים ביופיזיקליים הם הראו שגם רמות מתונות של השינוי הזה מרפדות את הערימה המסודרת של ה-G-quadruplex, אם כי התוצאה המדויקת תלויה ברצף ה-RNA שמסביב. 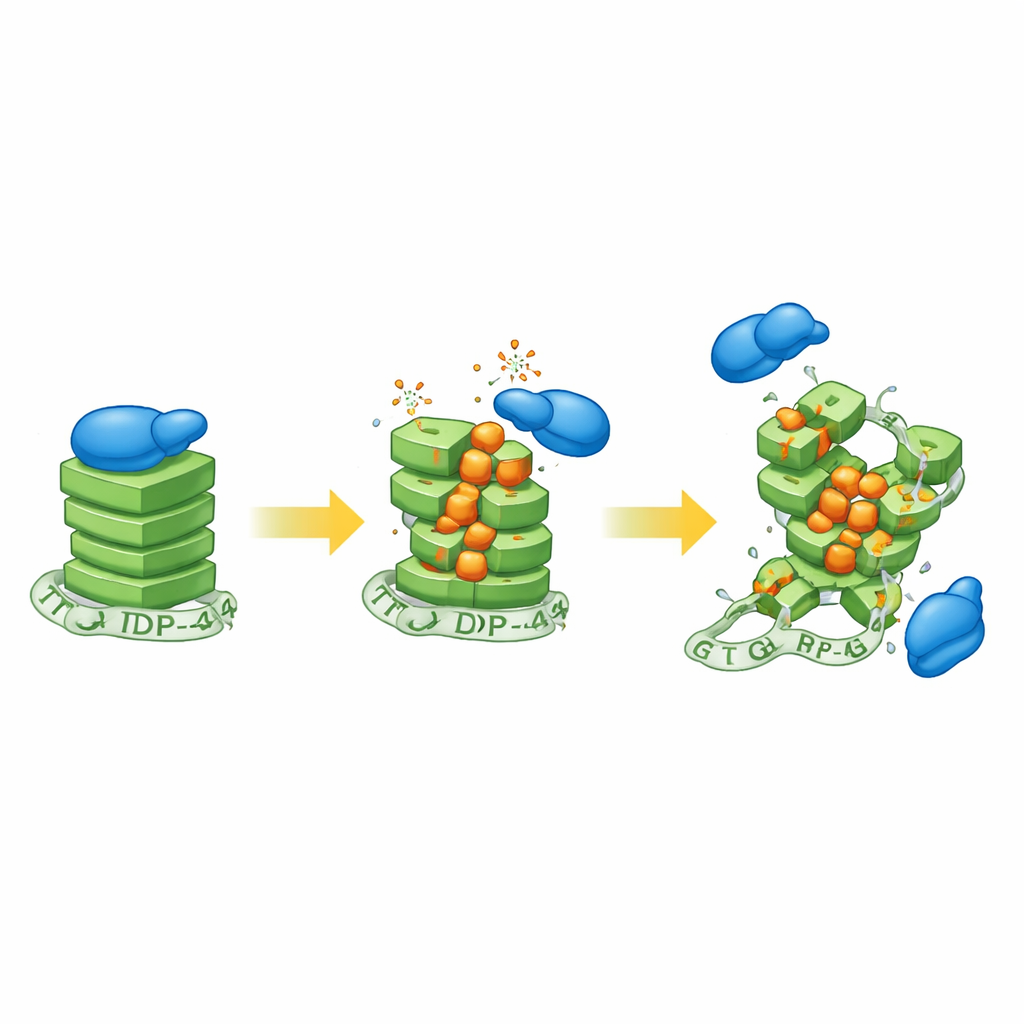
תקלות חדשות: בסיסים לא תואמים וגדילי RNA שמתווכים באופן שגוי
ניתוח מעמיק חשף שני סוגים מובחנים של בעיות מבניות. באחד ה-G-quadruplex ששאב את מקורו מההודעה של PSD-95, גואנינים מחומצנים נטו להתאים באופן לא ראוי לאדנינים קרובים, וליצור "אי-התאמות" שעוותו בעדינות את הקיפול. אי-התאמות אלה הופיעו בעיקר ברמות חמצון בינוניות, כאשר ה-RNA עדיין יכול היה להרכיב באופן חולף G-quadruplex שהביא שותפים שגויים במגע. ב-G-quadruplex אחר מההודעה של CaMKIIα, חמצון כבד הוציא מכלל שיווי משקל את הקשר התוך-מולקולרי הרגיל עד כדי כך שגואנינים שלמים שנותרו חיפשו שותפים בגדילים אחרים של RNA, וקידמו G-quadruplexes בין-מולקולריים חריגים. מבנים שמולחמים כאלה עלולים לסבך RNAs שונים זה עם זה ולהפריע לתנועה התקינה של RNA בתוך תאים עצביים.
כשה-RNA הפגוע מאבד את שותף החלבון שלו
המחקר בדק אז כיצד קשרים מעוותים אלה מתנהגים מול TDP-43. באמצעות ניסויי קשירה מבוססי ג'ל, הראו החוקרים כי TDP-43 מעדיף מאוד G-quadruplexes שלמים ובמקביל, ובמידה הולכת ופוחתת אינו נקשר כאשר מוכנסים יותר בסיסים מחומצנים. המבנה של CaMKIIα, שכבר היה דחוס בצפיפות, התגלה כרגיש במיוחד: חמצון קל כמעט ביטל את קשירת TDP-43. חלבון שני, FUS — שגם הוא מזוהה עם ALS — הראה ירידה דומה אך מעט פחות חמורה באפיניות, מה שמעיד שחימצון מחליש באופן רחב את אחיזת החלבונים הקושרים G-quadruplex. באופן מחקרני, כאשר עירבבו TDP-43 עם RNA מחומצן קלות, הנתונים הצביעו שהחלבון נקשר לצורת ביניים בלתי יציבה של ה-G-quadruplex במקום קשר מקופל מלא, רמז למאבק דינמי בין ייצוב להתפרקות.
פגיעות נוספת בחלבוני TDP-43 מוטנטיים הקשורים ל-ALS
העבודה בחנה בנוסף עשר וריאנטים של TDP-43 שמצאו בחולי ALS, רובם נושאים שינויים בזנב גמיש ועשיר גליצין המכוון זיהוי RNA. כל המוטנטים הללו כבר נקשרו ל-G-quadruplexes רגילים בחוזקה פחותה מאשר חלבון הבר-זמן (wild-type). כאשר הוכנסו G-quadruplex RNAs מחומצנים כמתחרים, המוטנטים היו אפילו פחות מסוגלים ממנה לחזות ולשאת מבנים פגועים. כמה וריאנטים הממוקמים באזורים מועדים לאי-סדר הושפעו במיוחד. הדבר מרמז על מכה כפולה באנשים מזדקנים הסוחבים מוטציות כאלה: לא רק ש-TDP-43 שלהם פחות יעיל באינטרינזי, אלא שחמצון RNA הנובע מהגיל מחליש עוד יותר את יכולתו להוביל מסרים חשובים לאורך אקסוני תאי העצב המוטוריים.
מה משמעות הדבר להבנת ALS
פשוטה: המחקר מראה שנזק כימי מונע-גיל מחדש מעצב את קשרי ה-RNA העדינים המכוונים הובלת מסרים בתאי עצב מוטוריים, וקשרים מעוותים אלה כבר אינם משתפים פעולה היטב עם TDP-43 או חלבונים קשורים. התוצאה היא סבירות גבוהה יותר להטמנת או לעצירת מטעני RNA, בדיוק באותם אקסונים ארוכים ופגיעים השומרים על השליטה בשרירים. עבור אנשים שירשו גם מוטציות ב-TDP-43, החלשות זו של אינטראקציות RNA–חלבון שנגרמת על ידי חמצון עלולה לדחוף תאים עצביים שנמצאים כבר בלחץ קרוב יותר לאי-כושר. על ידי הארה של שרשרת אירועים עדינה אך עוצמתית זו — מלחץ חמצוני למבנה RNA משתנה ועד הפרעה בהובלה — העבודה מדגישה חימצון של RNA מסוג G-quadruplex כקשר מולקולרי מבטיח בין הזדקנות ל-ALS, וכמטרה פוטנציאלית לאסטרטגיות עתידיות להגנה.
ציטוט: Ishiguro, A. Impact of G-quadruplex RNA oxidation on its conformational dynamics and interaction with ALS-associated TDP-43. Sci Rep 16, 8802 (2026). https://doi.org/10.1038/s41598-026-39767-y
מילות מפתח: שחמת עצבים מוטורית-צידית (ALS), חימצון RNA, G-quadruplex, TDP-43, ניוון תאי עצב מוטוריים