Clear Sky Science · he
חשיפה לקדמיום מעוררת פיברוזיס כלייתי על ידי עיכוב מסלול האיתות hsa_circ_0075684/miR-363-3p/KLF4
מדוע איום מתכתי חבוי חשוב
קדמיום הוא מתכת רעילה שחודרת לחיינו באופן שקט דרך מזון, עשן סיגריות וזיהום תעשייתי. ברגע שהיא נכנסת לגוף היא שורדת עשורים, עם נטייה בולטת להצטבר בכליות. במחקר זה בודקים כיצד חשיפה כרונית לקדמיום פוצעת את רקמת הכליה ומאתרים מעגל מולקולרי קטן שיכול לאותת על הנזק מוקדם — מה שמעניק תקווה למניעה של מחלת כליות כרונית במקום טיפול בשלב מאוחר בלבד.
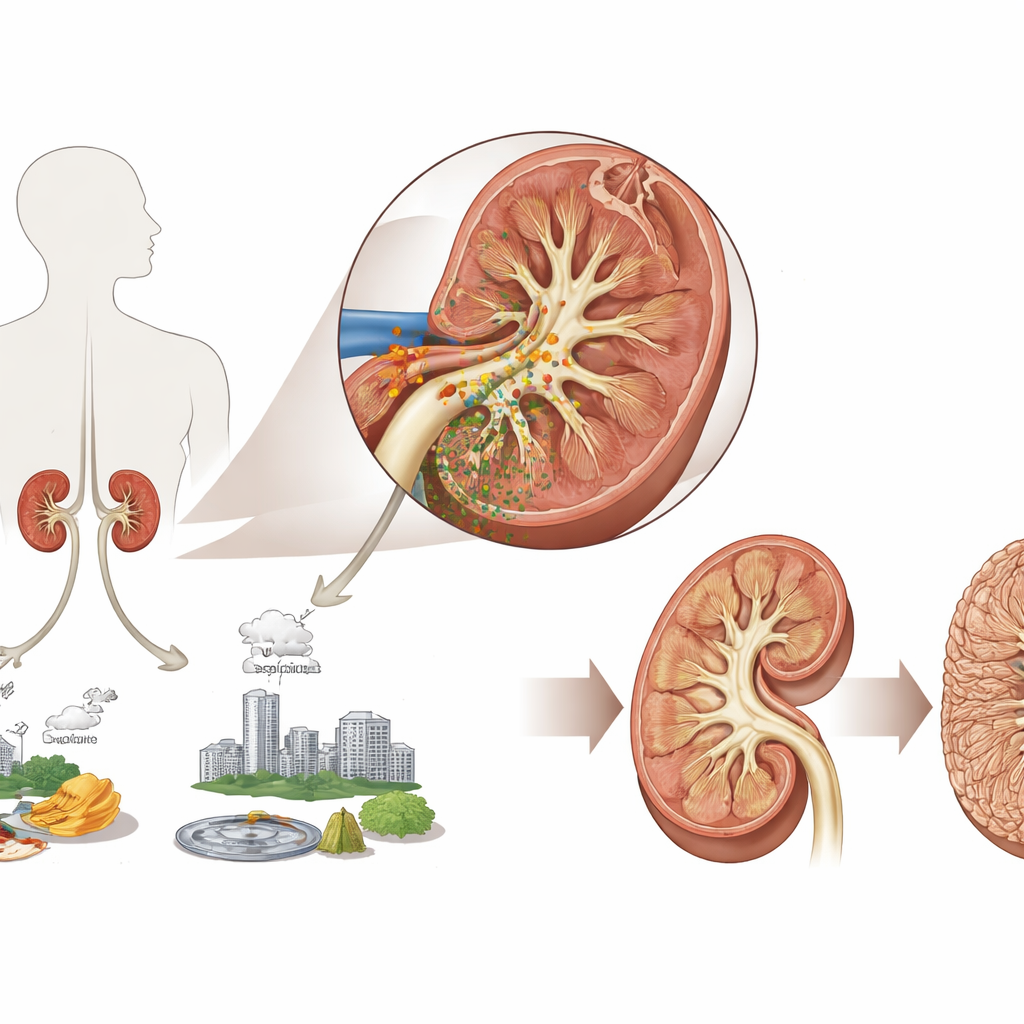
הנזק האיטי לכליה
הכליות פועלות כמסננות הגוף, מסלקות פסולת מהדם. קדמיום, עם זאת, נצבר במערכת הסינון הזו במשך שנים רבות ומתקשר במידה רבה למחלת כליות כרונית. המחברים מציינים שמקרי מחלת כליות כרונית עולים בעולם, ואין דרך יעילה להסיר קדמיום לאחר שהוא מתמקם בכליות. במקום להתמקד בניקוי, הם טוענים שיש צורך בדרכים לאבחן ולהפריע לנזק מוקדם — במיוחד לתהליך המכונה פיברוזיס, שבו רקמה בריאה מוחלפת בהדרגה ברקמת צלקת קשה שמפחיתה את תפקוד הכליה.
הודעות RNA זעירות ומסלול מגן
החוקרים התרכזו במולקולה רגולטורית קטנה בשם miR-363-3p, חלק ממשפחת רסיסי RNA קצרים שמכווננים את פעילות הגנים. עבודתם הקודמת הראתה כי RNA זה עלה ברמה בעובדי מפעל עם הרעלת קדמיום ממושכת. באמצעות מאגרי גנים ציבוריים רחבים חיפשו צוות החוקרים מעגל בקרה סביב miR-363-3p ברקמת כליה שנחשפה לקדמיום. הם זיהו מסלול תלת-חלקי: RNA מעגלי (hsa_circ_0075684) שיכול "לספוג" את miR-363-3p, המולקולה miR-363-3p עצמה, וחלבון שנקרא KLF4 שעוזר להגן על תאי הכליה מפיברוזיס. יחד, השלישייה הזו נראית כמתג מולקולרי השומר על איזון ומונע היווצרות צלקות.
מתאים בכליה בתרבית ועד לעכברים במעבדה
כדי לבדוק רעיון זה, החשיפה נבדקה על תאי צינוריות כלייתיות אנושיות במבחנה בפני מנות הולכות וגדלות של קדמיום. ככל שרמות הקדמיום עלו, התאים הראו סימנים קלאסיים של פיברוזיס: חלבונים הקשורים לצלקת עלו, בעוד שחלבון המסייע לשמירה על מבנה תקין ירד. במקביל, רמות miR-363-3p עלו, ואילו הן של KLF4 ושל ה-RNA המעגלי ירדו. ניסויים גנטיים הראו כי miR-363-3p נקשר ישירות ל-KLF4 ומוריד את ייצורו, ושה-RNA המעגלי בדרך כלל קושר את miR-363-3p ומונע ממנו להשתיק את KLF4. כאשר החוקרים הגבירו את miR-363-3p, חלבוני הצלקת זינקו ו-KLF4 ירד; כאשר חסמו את miR-363-3p או הגדילו את ה-RNA המעגלי, KLF4 שב לרמות גבוהות וסימני הפיברוזיס פחתו, אף בנוכחות קדמיום.
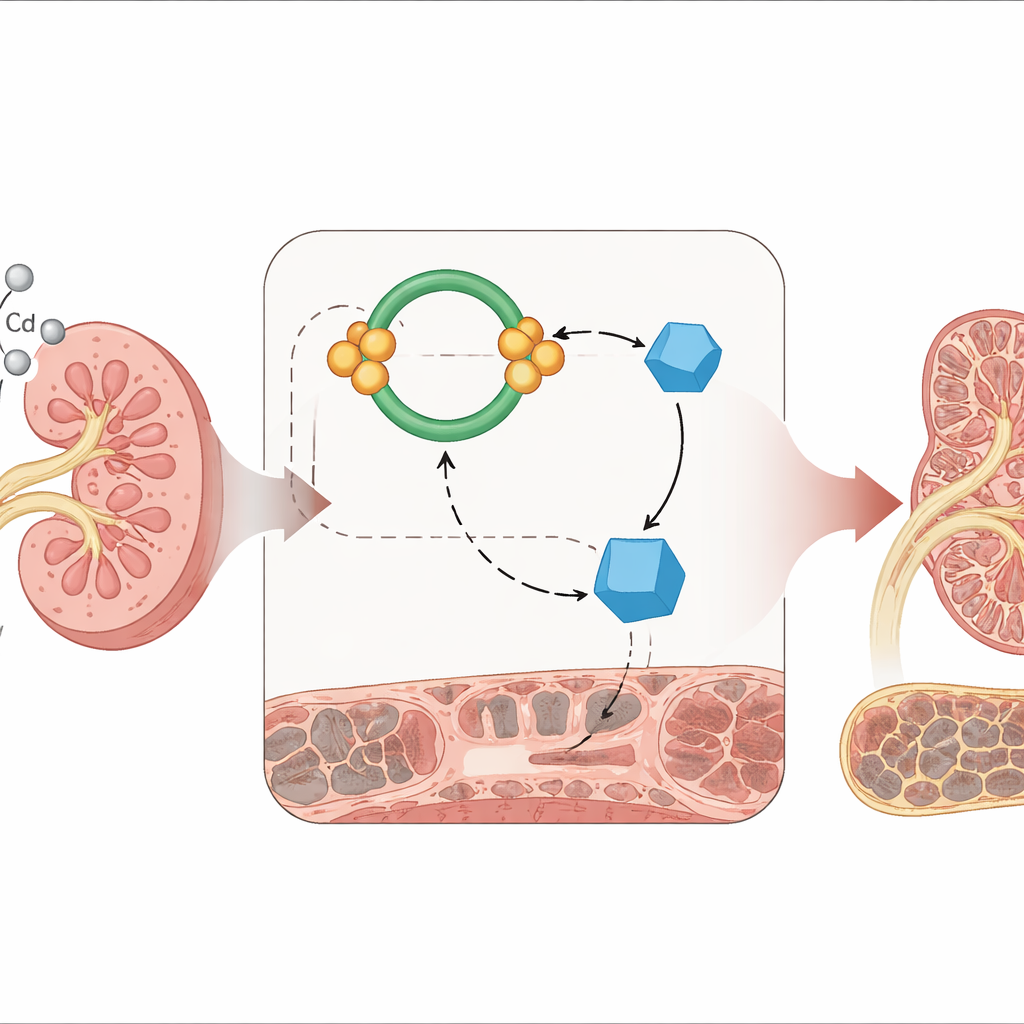
אישור הנזק בכליות החיות
החוקרים המשיכו למודל עכבר כדי לראות האם התבנית המולקולרית הזו מופיעה גם בחיות חיות. עכברים קיבלו קדמיום בפה במשך שלושה חודשים במנות שנבחרו כדי לדמות חשיפה סביבתית ארוכת טווח. במיקרוסקופ נראו בכליות של עכברים שטופלו בקדמיום שינויים פיברוטיים ברורים — סיבי קולגן צבועים בכחול ממלאים את המרווחים בין הצינוריות. הבדיקות הביוכימיות חזרו על ממצאי תרבית התאים: חלבוני הצלקת עלו, החלבון המגן KLF4 ירד, ורמות miR-363-3p בכליות עלו, תומכות ברעיון שמסלול זה פעיל במהלך נזק איטי של קדמיום בסביבה אמיתית.
מה משמעות הממצאים להגנת הכליות
במבט כולל, הממצאים מצביעים על כך שקדמיום מקדם צלקת כלייתית על ידי שיבוש איזון עדין בין RNA מעגלי, microRNA וחלבון מגן. כאשר קדמיום מוריד את ה-RNA המעגלי ואת KLF4, miR-363-3p משתחרר ונדחף את התאים לעבר פיברוזיס. עבור קהל לא מקצועי, המסר המרכזי הוא ששינויים מולקולריים מוקדמים — הרבה לפני הופעת תסמינים — עשויים בעתיד לשמש כסימני אזהרה בבדיקות דם או שתן לאנשים בסיכון לחשיפה לקדמיום. בעוד שנדרש עוד מחקר קליני, במיוחד באנשים, המסלול החדש שמיפו כאן מצביע על כלים עתידיים לאתר ואולי אף להאט את נזק הכליה הנגרם על ידי קדמיום לפני שהצלקות נעשות בלתי הפיכות.
ציטוט: Zhou, J., Huang, Y., Li, G. et al. Cadmium exposure induces renal fibrosis by inhibiting hsa_circ_0075684/miR-363-3p/KLF4 signaling pathway. Sci Rep 16, 8754 (2026). https://doi.org/10.1038/s41598-026-39715-w
מילות מפתח: חשיפה לקדמיום, צלקת כליה, microRNA, טוקסיקולוגיה סביבתית, מחלת כליות כרונית