Clear Sky Science · he
פקטור המועשר מחוסר חמצן 1α ממלא תפקידים כפולים בהתקדמות סרטן השלפוחית דרך ויסות כלי דם וחדירה בתיווך TIMP3
מדוע גידולים חסרי חמצן חשובים
תאי סרטן לעתים מתרבים במהירות כה גבוהה עד שהם מאיצים את אספקת הדם שלהם, ומשאירים חלקים מהגידול רעבים לחמצן. סביבה דלה בחמצן, או היפוקסיה, מאלצת תאים להפעיל תוכניות הישרדות שעשויות להקשות על הטיפול בסרטן. בסרטן השלפוחית — גידול נפוץ במערכת השתן — מדענים חשבו זמן רב שאחת מהתוכניות החושבות חמצן, הנשלטת על ידי חלבון בשם HIF-1α, בעיקר מסייעת לגידול ולפיזור הגידול. המחקר הזה בוחן זאת מקרוב ומגלה טוויסט מפתיע: בתנאים מסוימים, הפחתת HIF-1α עלולה בעצם להפוך את תאי סרטן השלפוחית לאגרסיביים יותר, וחלבון שני, TIMP3, עומד במרכז הפרדוקס הזה.
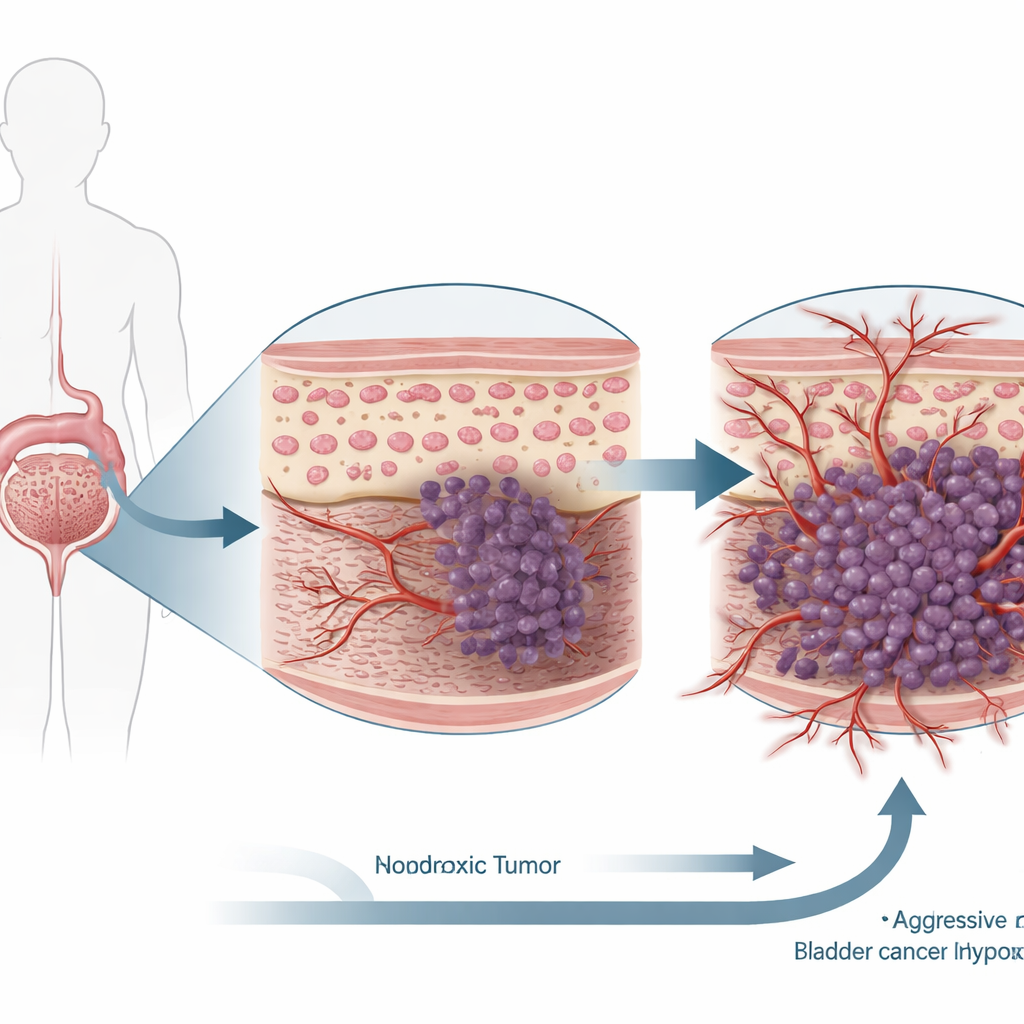
מבט קרוב על תאי סרטן השלפוחית
החוקרים עבדו עם שתי שורות תאים של סרטן שלפוחית אנושי מבוססות וחשפו אותן לרמות חמצן רגילות או להיפוקסיה, המדמה את כיסי חמצן הנמוכים שבתוך גידולים אמיתיים. לאחר מכן השתמשו בכלים גנטיים כדי להוריד את ביטוי HIF-1α בתאים אלה ומדדו כיצד שינוי זה השפיע על התנהגויות סרטניות בסיסיות: מהירות התפשטות התאים, מידת התמותה התאית, וכמה הם יכולים לנוע, לחדור מחסום ולעודד יצירת כלי דם חדשים. במקביל בדקו דגימות גידול שלפוחית ממטופלים כדי להשוות רמות של HIF-1α ו-TIMP3 ברקמה הסרטנית לעומת רקמת שלפוחית סמוכה ונורמלית.
היפוך תפקידים מפתיע בתנאי חמצן נמוך
דגימות המטופלים איששו כי HIF-1α אכן גבוה יותר בגידולי שלפוחית מאשר ברקמה נורמלית, בהתאם למוניטין שלו כגורם מקדם גידול. עם זאת, בניסויים התאית תחת היפוקסיה, הורדת HIF-1α נתנה את ההשפעה ההפוכה ממה שרבים ציפו. כאשר HIF-1α דוכא ורמות החמצן היו נמוכות, התאים הסרטניים התחלקו מהר יותר עם הזמן, היו פחות נוטים לעבור מוות תאי מתוכנת, והפכו ליותר יעילים בנדידה וחדירה דרך מחסות מדגם. הם גם שחררו אותות שעודדו תאי כלי דם ליצור רשתות צינוריות צפופות ונרחבות יותר, סימן להגדלת אספקת הדם לגידול. בקיצור, עם פחות HIF-1α בהקשר של היפוקסיה, תאי סרטן השלפוחית התנהגו באופנים אגרסיביים יותר.
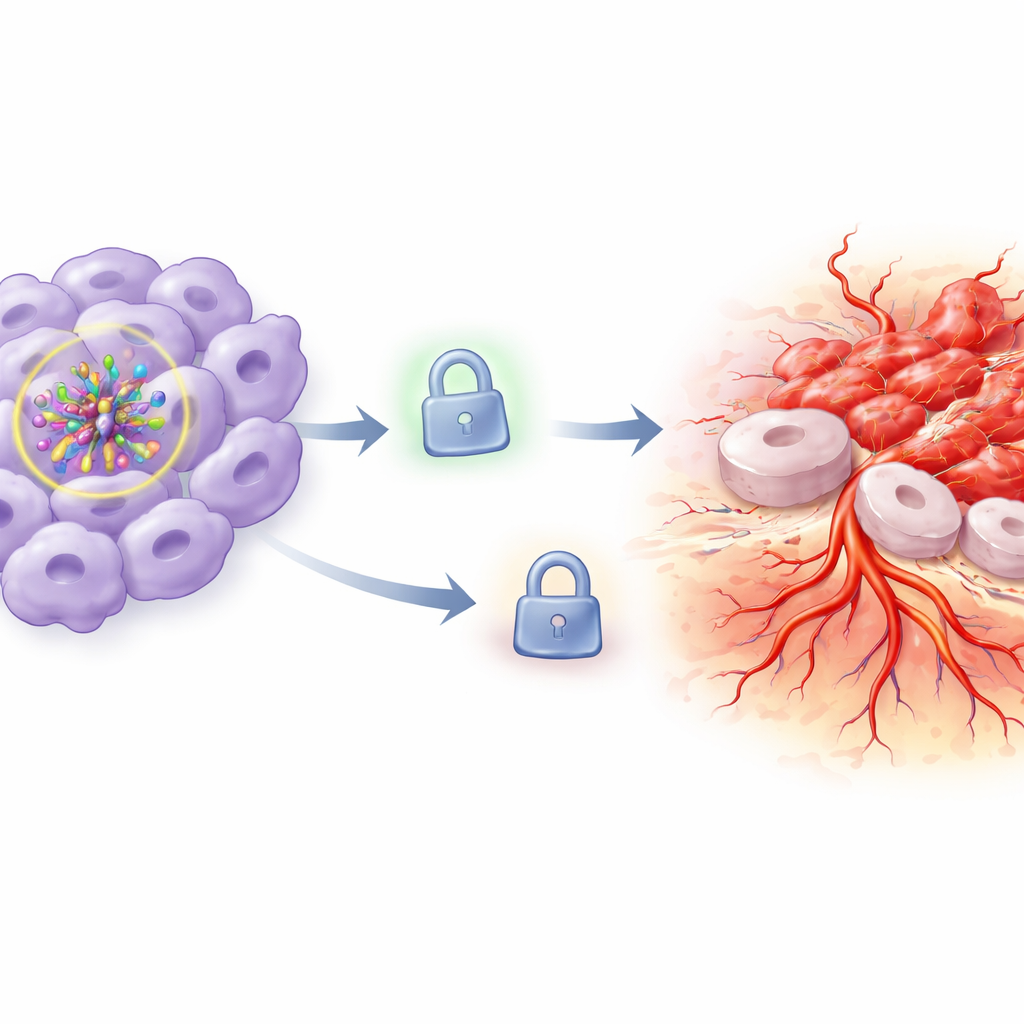
הבלם החסר על התפשטות הגידול
כדי להבין מדוע זה קרה, הצוות התרכז ב-TIMP3, חלבון שבדרך כלל פועל כבלם על פירוק הרקמות ויצירת כלי דם חדשים על ידי חסימת אנזימים שמפוררים את המטריקס המקיף. בתאים שבהם HIF-1α הוקטן והתאחסנו בחמצן רגיל, רמות TIMP3 נשארו יחסית גבוהות. אך כאשר רמות החמצן ירדו, חלבון TIMP3 צנח באופן חד. אובדן זה של TIMP3 תאם היטב את העלייה הנצפית בחדירה וביצירת כלי דם: כשהבלם נחלש, תאי הסרטן יכלו לשנות את סביבתם ולהתרחב ביתר קלות. החוקרים לאחר מכן הפכו את המצב על ידי אילוץ תאים לייצר עודפי TIMP3 בעוד HIF-1α נשאר מדוכא תחת היפוקסיה. שיחזור TIMP3 הפך חלקית או כמעט לחלוטין את ההתנהגות האגרסיבית: התאים גדלו פחות, מתו ביתר קלות, נדדו וחדרו פחות, וגרמו לפחות צינורות דמויי כלי דם ובהם קוטר וקוטר קצרים יותר.
מה משמעות הדבר עבור טיפולים עתידיים
ממצאים אלה מציעים של-HIF-1α יש אישיות כפולה בסרטן השלפוחית. מצד אחד, רמותיו הכלליות גבוהות יותר בגידולים והוא מסייע להניע תכניות ידועות התומכות בסרטן. מצד שני, תחת חוסר חמצן חמור נראה כי הוא מסייע לשמור על נוכחות מגנת של TIMP3. הסרת HIF-1α בהקשר זה עלולה שלא בכוונה להפחית את TIMP3 ולשחרר התנהגויות פולשניות ומקדמות יצירת כלי דם. מבחינה טיפולית, משמעות הדבר היא כי חסימה פשוטה של HIF-1α עלולה לחזור על פעמיה אלא אם כן הרופאים גם ימצאו דרכים לשמר את TIMP3, או את הבלמים הדומים לו. העבודה מדגישה את חשיבות ההבנה לא רק של מטרות בודדות, אלא של רשת רחבה של איזונים ובדיקות שמעצבת כיצד גידול מגיב לסביבה הקשה שלו, הדלה בחמצן.
ציטוט: Wang, X., Guo, J., Zhang, R. et al. Hypoxia-inducible factor 1α exerts dual roles in bladder cancer progression through TIMP3-mediated regulation of angiogenesis and invasion. Sci Rep 16, 8425 (2026). https://doi.org/10.1038/s41598-026-39635-9
מילות מפתח: סרטן השלפוחית, היפוקסיה גרורתית, HIF-1α, TIMP3, יצירת כלי דם