Clear Sky Science · he
פתרון הסתירה בין סימולציה ותוצאות ניסיוניות של שימוש בננו־חלקיקי זהב בטיפול פרוטונים
למה חלקיקי זהב זעירים חשובים לטיפול בסרטן
טיפול בפרוטונים הוא צורת קרינה מתקדמת היכולה למקד גידולים בדיוק ובו בזמן לשמר רקמות בריאות מסביב. בשנים האחרונות ניסו מדענים לשלב טיפול פרוטונים עם חלקיקי זהב זעירים, קרויים ננו־חלקיקי זהב, במטרה להפוך את הטיפול לאכזרי יותר כלפי תאי הסרטן. ניסויים מראים שלעתים השילוב הזה הורג יותר תאי גידול מאשר פרוטונים לבדם — אך סימולציות ממוחשבות התקשו להסביר מדוע. המאמר הזה מתמודד עם התעלומה התקופתית ומצביע על שחקן מרכזי שונה ממה שרבים מהחוקרים ציפו.
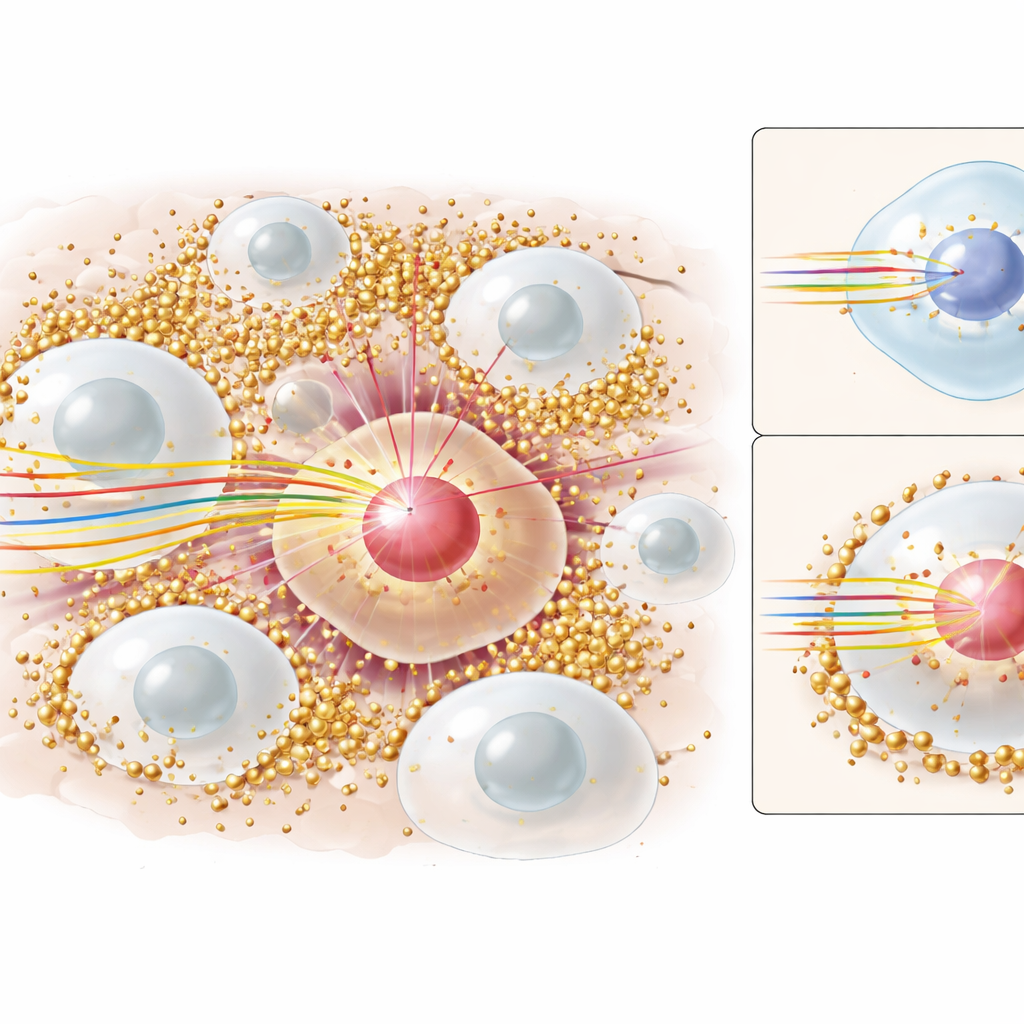
הסיפור הישן: האשמה באלקטרונים מהירים
ננו־חלקיקי זהב כבר מפורסמים בטיפולי רנטגן וקרינות גמא, שבהם הם מגבירים נזק בעיקר על ידי פליטה של שיירי אלקטרונים בעלי אנרגיה. אלקטרונים אלה נעים למרחקים קצרים ושוברים DNA בתאים סמוכים. במשך שנים רבים הניחו שהסיפור הבסיסי דומה גם בטיפול בפרוטונים: פרוטונים פוגעים בזהב, אלקטרונים נוספים נקרעים החוצה והתאים הסרטניים סובלים. אבל היתה בעיה. מודלים ממוחשבים מפורטים העוקבים אחרי כל חלקיק ואנרגייתו — כמו אלה ששומשו בעבודה זו — המשיכו לחזות תוספת מינימלית של מינון בגרעין התא כתוצאה מאותם אלקטרונים, במיוחד מכיוון שרוב הננו־חלקיקים נמצאים באזור החיצוני של התא ולא בתוך הגרעין שבו נמצא ה‑DNA. במקביל, ניסויים מעבדתיים עם תאים הראו עלייה ברורה במוות התאי ובאפקטיביות הטיפול כשיש זהב. המספרים פשוט לא תאמו.
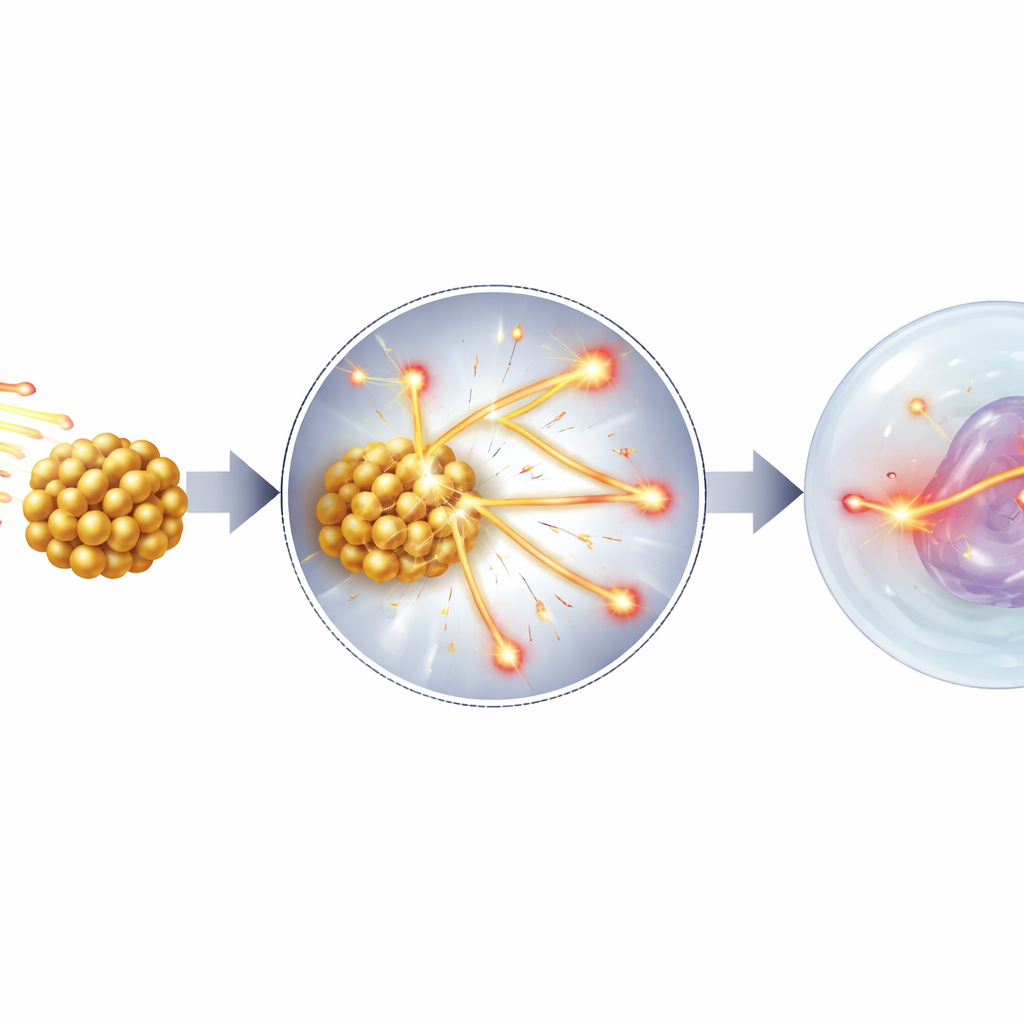
הדימוי החדש: האטת הפרוטונים עצמם
עבודה זו מציעה ובוחנת מנגנון ראשי שונה: במקום לפעול בעיקר כמפיצי אלקטרונים, ננו־חלקיקי זהב מתנהגים כשוברי מהירות זעירים לפרוטונים. כאשר פרוטון עובר דרך אזור המכיל מתכות צפופות ובעלות מספר אטומי גבוה כמו זהב או ברזל, הוא חווה מספר רב של התנגשויות קטנות עם אטומים כבדים אלה. כל התנגשות מוציאה מעט יותר אנרגיה ממה שהיתה נצרכת ברקמה רגילה, כך שהפרוטון מאט מהר יותר וקצב איבוד האנרגיה שלו ליחידת מרחק — מה שמוכר בפיזיקה כהעברה אנרגיה ליניארית (LET) — עולה. מסלולי LET גבוהים מזיקים במיוחד ל‑DNA משום שהם יוצרים אשכולות דחוסים של שברים שהחייזר מתקשה לתקן. על ידי הרצת סימולציות מונטה קרלו מפורטות עם סביבת הפיתוח Geant4, המחבר מראה שזהב וחלקיקים כבדים אחרים מגדילים משמעותית את מספר הפרוטונים האיטיים ובעלי LET גבוה שמגיעים לגרעין התא, אף על־פי שאורך המסלול הכולל הוא בסדר גודל של מיקרומטרים — הרחק מטווח האלקטרונים בעלי האנרגיה הנמוכה שבמסורת הוטלה עליהם האשמה.
התאמת סימולציות לניסויי תאים אמיתיים
כדי לבדוק האם התמונה החדשה מחזיקה מים, המחקר משחזר כמה ניסויי תאים שפורסמו שבהם גידולים טופלו בקרני פרוטונים יחד עם ננו־חלקיקים שונים (זהב, ברזל ופלדיום) בגדלים וריכוזים שונים. עבור כל מקרה, הסימולציות מחשבות כמה מינון נוסף מקבל הגרעין — מסוכם כמכפיל שיפור המינון — ואז מכניסות זאת לנוסחה רדיוביולוגית סטנדרטית שמקשרת בין מינון הניתן לשרידות תאים. גישה זו משנה את העקומה הרגילה שמתארת כמה תאים שורדים או מתים לאחר מינון נתון. עבור רוב הניסויים שנבדקו, עקומות השרידות החזויות עם ננו־חלקיקים התאימו קרוב לנתונים הנמדדים, לעתים בתוך שגיאה של כבדה אחוז אחד. במקביל, הסימולציות מראות שמינון האלקטרונים בגרעין משתנה במעט כאשר מוסיפים ננו־חלקיקים, בעוד שהפלואנס של פרוטונים איטיים ונזקניים יותר עולה בבירור. נשארו כמה אי־התאמות, שהמחבר מייחס לאי־וודאויות באופן שבהן הוקמו או דווחו חלק מהניסויים, אך המגמה הכוללת תומכת בחוזקה בהסבר ההאטת פרוטונים.
מגבלות, יוצאים מן הכלל ומתי הזהב עוזר ביותר
המאמר חוקר גם מצבים שבהם ננו־חלקיקים אינם נראים מועילים במיוחד. בקרני פרוטונים בעלות אנרגיה נמוכה מאוד שעוצרות בתוך רק שכבות של תאים, פשוט אין מרחק מספק כדי שהפרוטונים ייפגשו בהרבה ננו־חלקיקים ויאטו בצורה משמעותית, ולכן לא נצפה שיפור חזק באפקטיביות. באותו אופן, צורות מורכבות של ננו־חלקיקים או גיאומטריות ניסוי שתאורן לקוי מקשות על שיחזור בסימולציות, מה שעשוי להסביר כמה מקרים חריגים שבהם המודלים והמדידות סוטים. המחבר מציין שאם חלקיקים זעירים במיוחד מצליחים להיכנס לגרעין עצמו, פליטת אלקטרונים ותגובות כימיות עם מולקולות התא עשויות להוסיף להשפעה. עם זאת, בתנאי טיפול מציאותיים רבים, התבנית השלטת עקבית: האטה מוגברת של פרוטונים באזורים עשירים בזהב מובילה לנזק מרוכז יותר בגרעין.
מה משמעות הדבר לטיפול בסרטן בעתיד
לקהל שאינו מומחה, המסר המרכזי הוא שננו־חלקיקי זהב בטיפול פרוטונים פועלים פחות כמו תותחי אלקטרונים זעירים ויותר כמו בלמים בלתי נראים שעושים מפרוטונים מהירים ויחסית עדינים לתוקפים איטיים וחזקים יותר בדיוק במקום שבו זה חשוב — ה‑DNA של תא הגידול. בהבהרת המנגנון ובהדגמה שהוא יכול לשחזר במדויק נתוני שרידות תאים אמיתיים, המחקר מסייע לפתור סתירה ממושכת בין תאוריה לניסוי. תובנה זו עשויה להנחות תכנון חכם יותר של טיפולים מבוססי ננו־חלקיקים, כגון בחירת חומרים, גדלים וריכוזים שממקסמים את האטת הפרוטונים בקרבת גרעיני הגידול תוך הפחתת תופעות לוואי. בטווח הארוך זה עשוי להפוך את הטיפול בפרוטונים למדויק וחזק יותר, ולהציע תוצאות טובות יותר למטופלים עם סוגי סרטן שקשה לטפל בהם.
ציטוט: Tabbakh, F. Resolving the contradiction between simulation and experimental results of using gold nanoparticles in proton therapy. Sci Rep 16, 8012 (2026). https://doi.org/10.1038/s41598-026-39621-1
מילות מפתח: טיפול בפרוטונים, ננו־חלקיקי זהב, הגברת רגישות לקרינה, רדיותרפיה לסרטן, ננו־רפואה