Clear Sky Science · he
אופטימיזציה של מונוציטים THP-1-CAR המשתמשים באיתות CD32a לפאגוציטוזה להפעלת תאי T ספציפיים לאנטיגן
ללמד את מערכת החיסון טריקים חדשים
טיפולי תאים מודרניים כבר מתכנתים מחדש תאי חיסון כדי לצוד סרטן, אך רובם נשענים על תאי T, שלפעמים מתקשים בסביבה העוינת של גידולים מוצקים. המחקר הזה פונה במקום זאת למגן אחר עוצמתי — מאקרופאגים, ה״אוכלים״ המקצועיים של הגוף — ושואל איך לתכנת אותם כך שהם לא רק יבלעו תאים או וירוסים מזיקים ביעילות רבה יותר, אלא גם יקראו לתאי T למתקפה ממושכת וממוקדת יותר. העבודה חושפת חוקים עיצוביים לבניית מאקרופאגים מצוידי CAR טובים יותר, שניתן ליישם הן בזיהומים כמו COVID-19 והן בגידולים מוצקים קשים לטיפול.
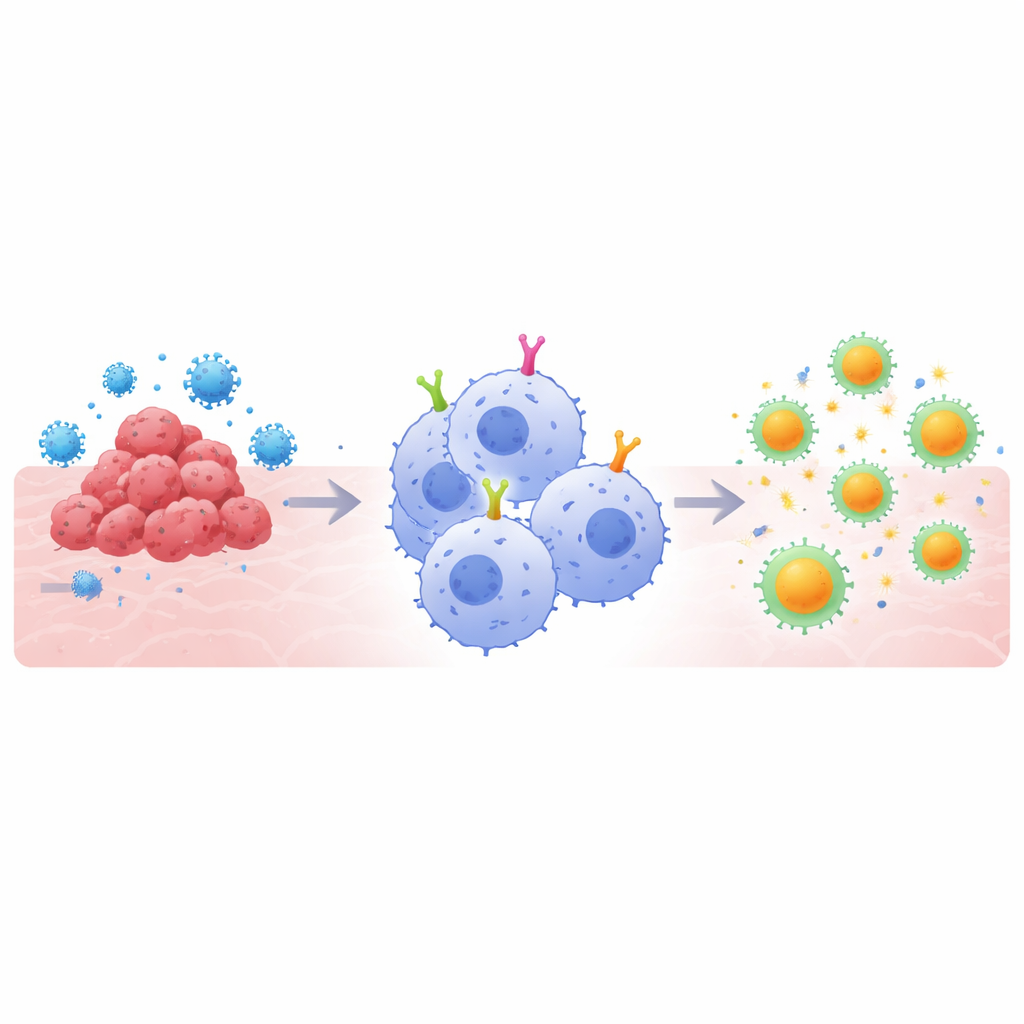
למה תאי סופר־אוכל חשובים
טיפולים מבוססי CAR פועלים על ידי הצמדת קולטנים מותאמים למשטח תאים החיסוניים שמזהים מטרה נבחרת, כגון חלבון גידול או חלבון הקוץ של וירוס. הגרסאות בתאי T שינו את הטיפול בסוגי סרטן דם מסוימים, אך נתקלות במכשולים מול גידולים מוצקים ובכמה זיהומים. מאקרופאגים מציעים זווית שונה: באופן טבעי הם בולעים איומים ומפרקים אותם לחלקים שניתן להציג לתאי T, וכך מקשרים בין זרועות החיסון הא־מולדת והנרכשת. עם זאת, רוב העיצובים של CAR נבנו במקור עבור תאי T ולא עבור מאקרופאגים. המחברים הסיקו שכדי לנצל באופן מלא את חוזקות המאקרופאגים, החלקים הפנימיים האיתותיים של ה‑CAR — הקטעים שאומרים לתא מה לעשות לאחר שביעד נקשר — צריכים להיות מותאמים במיוחד לתאי ה״אוכלים״ הללו.
איתור החיווט הפנימי הטוב ביותר
הצוות השווה באופן שיטתי כמה תחומי איתות פנימיים בתוך CAR שהוכנסו לקו תאי מונוציטים אנושי (THP‑1) שניתן להפוך מהם למאקרופאגים. הם התמקדו בתחומים שמקורם בקולטנים שמניעים בדרך כלל פאגוציטוזה ודלקת: CD3ζ (המודול הקלאסי של תאי T), CD32a (קולטן שקושר מטרות מצופות בנוגדנים), מרכיבי CR3 CD11b ו‑CD18 (קולטני משלים מרכזיים), ו‑TLR4 (חיישן סכנת מיקרוביאלי). באמצעות חרוזים ופסאודו‑וירוסים מצופים בחלבון הספייק של SARS‑CoV‑2, מדדו כמה כל עיצוב CAR אפשר לתאים לבלוע מטרות, לייצר מולקולות דלקתיות, ואז להפעיל תאי CD8 של בני אדם שהכירו בעבר את הווירוס. לאחר מכן העבירו את העיצובים המבטיחים ביותר ל‑CARים המכוונים למזותלין, חלבון שמיוצר ביתר ברבים מהגידולים המוצקים, כדי לבדוק האם אותם כללים יחולו גם בהקשר של סרטן.
בניית ״אוכלים״ וטועי אותות טובים יותר
התברר דפוס ברור: CARים המבוססים על CD32a הניעו באופן עקבי פאגוציטוזה חזקה ומהירה יותר מאלו שהשתמשו בתחום המסורתי CD3ζ, למרות של‑CD3ζ היו יותר המוטיבים הקלאסיים להפעלה. במילים אחרות, ההתאמה בין האות למכאניזם של המאקרופאג חשובה יותר מעוצמת האות הגולמית. הוספת קטעי CR3 (CD11b או CD18) על גבי CD32a בדרך כלל לא הגדילה עוד את יכולת הבליעה, אך העלתה את רמות הציטוקינים הדלקתיים המרכזיים כגון TNF‑α ו‑IL‑1β. קומבינציות שכללו TLR4 הגביהו עוד יותר את האותות הדלקתיים ואת סממן המשטח CD86, המקושר ליכולת לעורר תאי T, אם כי זה בא במחיר: רמות CAR נמוכות יותר על פני התא ופאגוציטוזה מעט מופחתת.
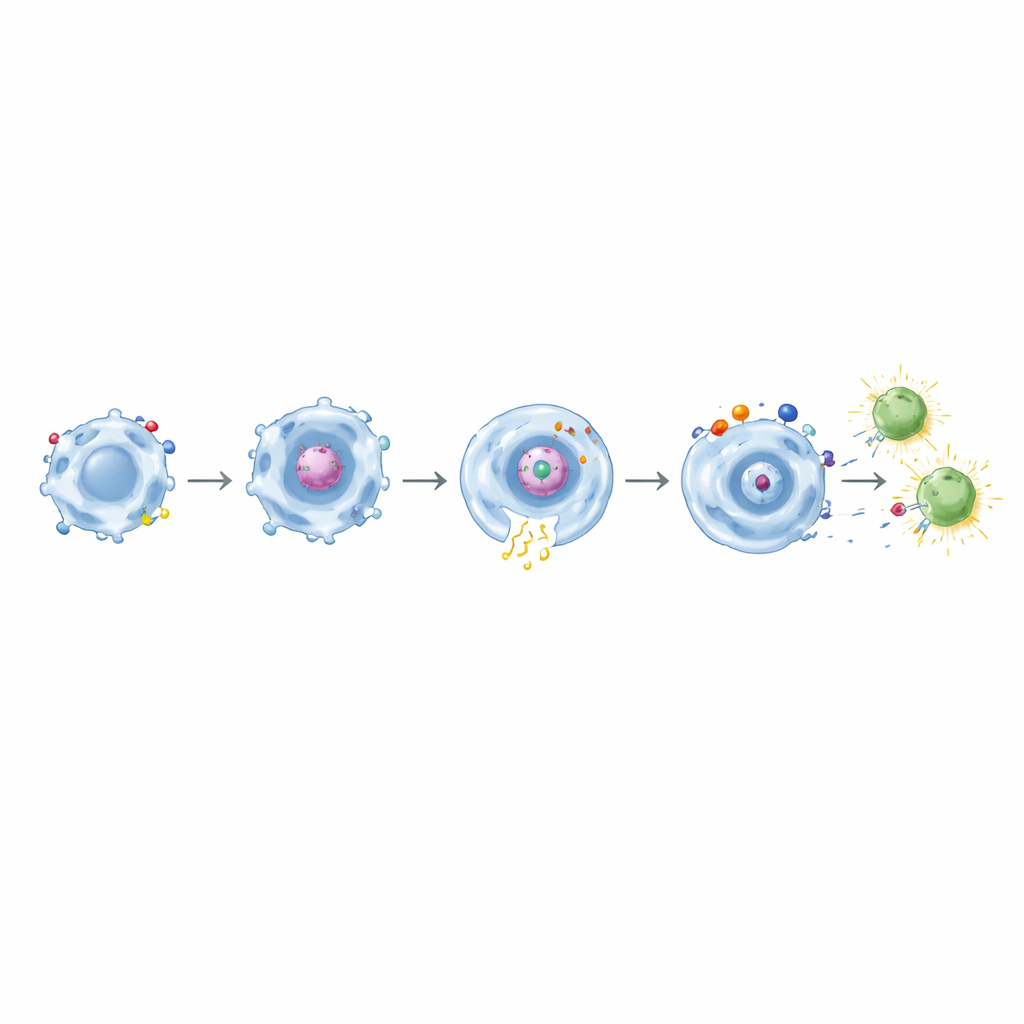
מבליעה ללימוד תאי T
חשוב לציין שאחרי שמאקרופאגים שנקשרו ל‑CD32a בלעו את חלבון הספייק, הם הצליחו להפעיל תאי CD8 זיכרון מאנשים שחוסנו בעבר נגד COVID‑19. תאים אלה הפעילו סממני הפעלה מוקדמים וייצרו מולקולות אפקטור כגון אינטרפרון‑γ ו‑TNF‑α. האפקט התחזק עוד יותר עם CARים דו‑תחומיים ששילבו CD32a עם CD11b, CD18 או TLR4. כאשר עיצובים דומים המכוונים למזותלין נבדקו נגד תאי גידול מהונדסים, הם שוב הראו פאגוציטוזה מדויקת התלויה במטרה יחד עם אותות דלקתיים מחוזקים. מתוך אלה, צירוף CD32a+TLR4 בלט כ״אזעקת רקמה״ חזקה, שהגביר באופן היעיל ביותר הפרשת ציטוקינים ו‑CD86 תוך שמירה על בליעה ממוקדת של הגידול.
מה זה עשוי להציע לטיפולים עתידיים
לעין שאינה מומחית, המחקר הזה מראה שעיצוב מאקרופאגים אינו בעיית ״גודל אחד מתאים לכולם״. על‑ידי החלפה ושילוב של מודולים פנימיים לאיתות, מדענים יכולים לעצב תאים שמתמקדים או בנקיון יעיל של תאים חולים או בהתנהגות כמגברים חיסוניים שמעצבים מחדש את הסביבה הדוחקת של הגידול וגייסים תאי T. CARים המבוססים על CD32a צמחו כיסוד חזק לעיצובים כאלה, כשהם מתעלים על המודולים המסורתיים של תאי T במאקרופאגים ופועלים גם מול מטרות ויראליות וגם מול מטרות גידול. אמנם התוצאות הללו מקורן במודלים מעבדתיים ויש לאמתן בתאים אנושיים ראשוניים ובחיות, אך הן מספקות תוכנית לעיצוב הדור הבא של טיפולי CAR‑מאקרופאגים שעשויים להתמודד טוב יותר עם גידולים מוצקים וזיהומים עמידים על ידי איחוד בליעה מהירה עם הפעלה מדויקת של תאי T.
ציטוט: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
מילות מפתח: תאי מאקרופאגים עם CAR, איתות CD32a, פאגוציטוזה, אימונותרפיה של גידולים מוצקים, הפעלת תאי T