Clear Sky Science · he
FAM120A - חלבון המוטמע ברשת המחלות של ALS
מדוע זה חשוב לאנשים ולמשפחות
לטרופיה עצבית צידית ממארת (ALS) היא מחלה הרסנית שמובילה לשיתוק הדרגתי על ידי השמדת תאי העצב שמווסתים תנועה. עד היום איננו מבינים במלואו מדוע תאים מוטוריים אלה מתים, וטיפולים יעילים עדיין נדירים. מחקר זה מאיר זרקור על חלבון מוכר מעט בשם FAM120A, ומרמז שהוא עשוי לעזור לתאי העצב להתמודד עם מתח ולמנוע הצטברות של גושים חלבוניים מזיקים — סימן היכר של ALS. על ידי גילוי האופן שבו החלבון מתנהג במהלך המחלה, הממצא פותח מסלול חדש להבנה, ואולי בסופו של דבר לטיפול, ב‑ALS.
גילוי שחקן נסתר ברשת גנים צפופה
החוקרים לא התחילו במכון המעבדה אלא במחשב. הם השתמשו בגישה של "ניתוח מתכנס" כדי לשלב מערכי נתונים רבים קיימים על גנים המקושרים ל‑ALS ועל האינטראקציות שלהם. התצוגה הרשתית אפשרה להם לראות אשכולות של חלבונים שעובדים יחד בתהליכים תאיים מרכזיים, במיוחד אלה הכרוכים בטיפול ב‑RNA ובבקרת איכות חלבונים — שניהם אזורים בעייתיים ידועים ב‑ALS. בתוך אחד האשכולות הללו, FAM120A בלט כחלבון שהיה מזוהה פחות אך בעל חיבורים רבים והוא מתקשר עם כמה חלבונים מוכרים שקושרו ל‑ALS. התפקידים המוכרים שלו בסיוע לתאים לעמוד בלחץ חמצוני ובניהול RNA עשו אותו למועמד חזק למחקר נוסף.
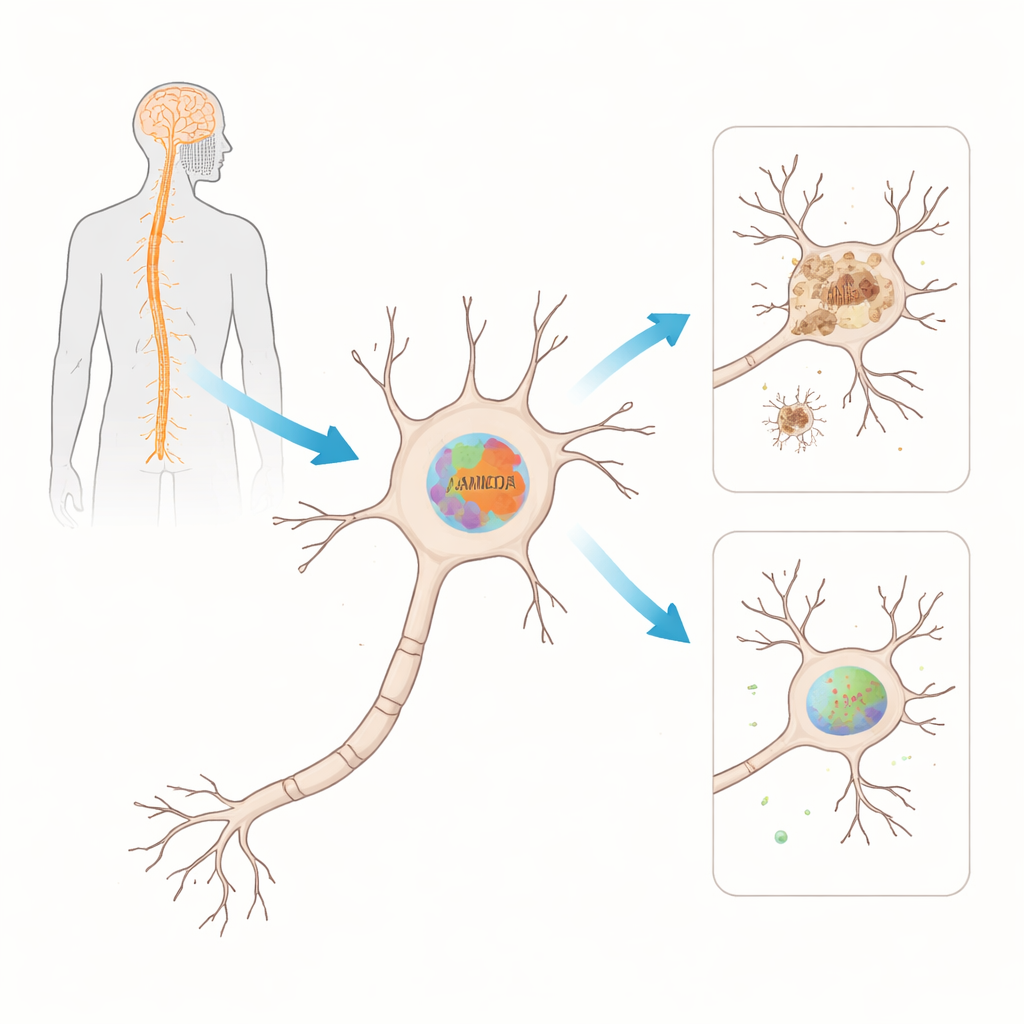
מעקב אחרי חלבון פגיע במהלך התקדמות המחלה
כדי לבדוק האם FAM120A באמת חשוב ב‑ALS, הצוות פנה לדגם עכבר נפוץ הנושא גרסה מוטנטית של הגן SOD1, אחד הגורמים הגנטיים הראשונים שזוהו ב‑ALS. הם מדדו הן את מסרי ה‑RNA והן את רמות החלבון של הנגזרת העכברית, Fam120A, בחוט השדרה לאורך זמן, מלפני הופעת התסמינים ועד שלבי מחלה מאוחרים. בשלבים המוקדמים ירדו רמות ה‑RNA של Fam120A בחוט השדרה לפני שהחיות הראו סימנים ברורים למחלה. מאוחר יותר, כאשר הופיע השיתוק, רמת חלבון Fam120A ירדה במידה ניכרת. חוסר ההתאמה הזה — שינוי ב‑RNA תחילה, וחלבון מאוחר יותר — מצביע על כך שכמה שכבות של ויסות מתמוטטות ככל שהמחלה מתקדמת.
היכן בחוט השדרה החלבון נמצא
בהמשך שאלו המדענים היכן בדיוק נמצא Fam120A בחוט השדרה. באמצעות מיקרוסקופיה פלואורסצנטית על פרוסות רקמה ראו כי Fam120A קיים בעיקר בתאים עצביים בקרן הוונטרלית — האזור העשיר בתאי עצב מוטוריים שמתנוונים ב‑ALS. בשלב מאוחר של המחלה הם ראו אות מסוים בתאי תמיכה הנקראים אסטרוציטים, אך הדפוס הדומיננטי נשאר נוירונלי. התצפיות הללו קושרות את Fam120A ישירות לתאים שנכשלו ב‑ALS ותומכות ברעיון שאובדנו עלולות להחליש את היכולת שלהם להתמודד עם מתח תאי, מה שעשוי לתרום לירידה בתפקוד המוטורי.
השמת כמות נוספת של FAM120A בעיצובים דמויי עצב
הצוות עבר אחרי כן לתאים בגידול דמויי עצב כדי לחקור מה FAM120A עושה בפועל. הם מהנדסים תאים אלה כדי להפיק או SOD1 תקין או מוטנטי, האחרון נוטה ליצור אגגרגטים רעילים, ואז אילצו את התאים לייצר עודף של FAM120A אנושי. בנוכחות SOD1 מוטנטי, הגדלת רמות FAM120A הורידה במידה ניכרת הן את כמות ה‑SOD1 הלא‑מסיסה שנמדדה בבדיקות ביוכימיות והן את מספר האגגרגטים הנראים במיקרוסקופ. באופן משמעותי, ל‑FAM120A היה מעט השפעה על צורתו התקינה של SOD1, מה שמרמז שהוא עשוי לסייע ספציפית בתמודד עם חלבונים שנטויים לקיפול שגוי או להצטברות — בעיה מרכזית ב‑ALS ובמחלות ניווניות עצביות אחרות.
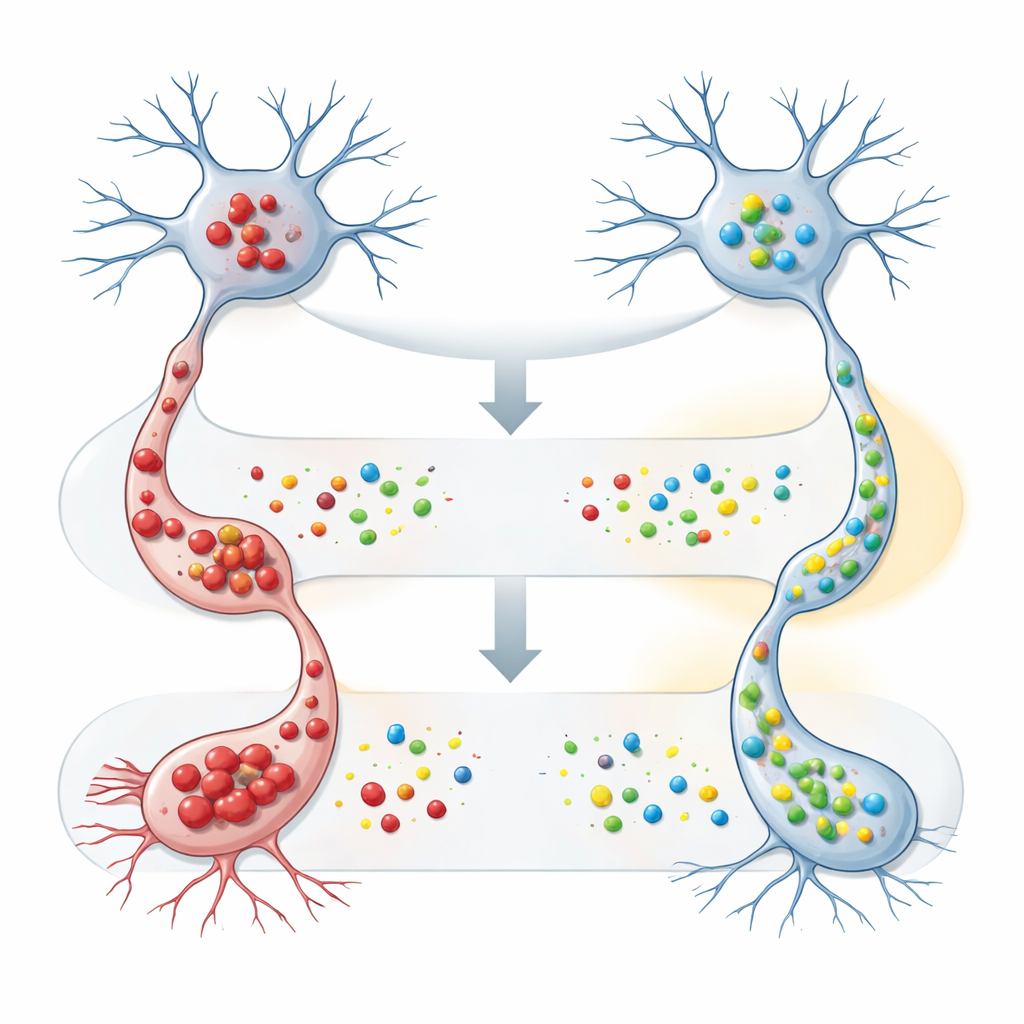
בניית מפה רחבה יותר של בעלי ברית ואויבים מולקולריים
מעבר לניסויים אלה, החוקרים חקרו את רשת האינטראקציות הרחבה של FAM120A. הם אישרו שהוא מקושר פיזית ל‑PURA, חלבון קושר RNA שכבר נקשר להתפתחות המוח ולניוון עצבי, ומצאו שגם רמות PURA יורדות בחוט השדרה של עכברי ה‑ALS, אם כי בשלבים מאוחרים יותר של המחלה. הם מדגישים קשרים נוספים בין FAM120A, גן האנטיסנס המקביל FAM120Aos, וחלבון קשירת RNA נוסף, ELAVL1, שמווסת גנים של דלקת ותגובה למתח במוח. רשת הקשרים המתהווה מציבה את FAM120A בצומת של ויסות RNA, תגובות למתח ובקרת איכות חלבונים — בדיוק המערכות שמתפקדות לקוי ב‑ALS.
מה זה יכול להצביע ליעדי טיפול עתידיים ב‑ALS
בהחלטת הממצאים יחד, הם מצביעים על כך ש‑FAM120A הוא לא רק צופה מהצד אלא חלק משמעותי מרשת מחלת ה‑ALS. הירידה המוקדמת שלו בתאי עצב מוטוריים פגיעים, הקישורים הפיזיים שלו לחלבוני ויסות RNA אחרים, ויכולתו לצמצם גושי SOD1 רעילים בתאים — כולם מצביעים על תפקיד מגן בשימור מאזן החלבונים. למרות שעבודת המשך רבה נותרה — במיוחד כדי לבחון האם שינויים דומים מתרחשים בבני אדם עם ALS ובדגמים אחרים של המחלה — FAM120A בולט כעת כמטרה מבטיחה למחקרים עתידיים ואולי, בסופו של דבר, לטיפולים שנועדו לשמר את בריאותם של תאי העצב המוטוריים.
ציטוט: Vicencio, E., Gomez, L., Beltran, S. et al. FAM120A - a protein inserted in the ALS disease network. Sci Rep 16, 8200 (2026). https://doi.org/10.1038/s41598-026-39329-2
מילות מפתח: לטרופיה עצבית צידית ממארת, תאי עצב מוטוריים, הצטברות חלבונים, חלבוני קשירה ל‑RNA, ניוון עצבי