Clear Sky Science · he
מודל פיזיקת פולימרים של גרעין התא בפאזה הבין-שלבית לסימולציות רדיוביולוגיות
מדוע צורת "הבית" של ה-DNA שלנו חשובה
הקרינה היא סם פיפיות ברפואה: היא יכולה להרוג תאי סרטן, אך גם לפגוע ברקמה בריאה. בלב שני הסיכונים והיתרונות ניצב ה-DNA שלנו, דחוס בתוך גרעין התא. מאמר זה מראה כיצד מודל תלת־ממדי מפורט בהשראת פיזיקה של הגרעין ה"עירוני" יכול לסייע לחוקרים לחזות כיצד קרינה שוברת וכיצד מתרחשות טעויות בהרכבת הכרומוזומים, מה שעשוי לשפר טיפולי סרטן והערכת סיכוני קרינה בחלל.
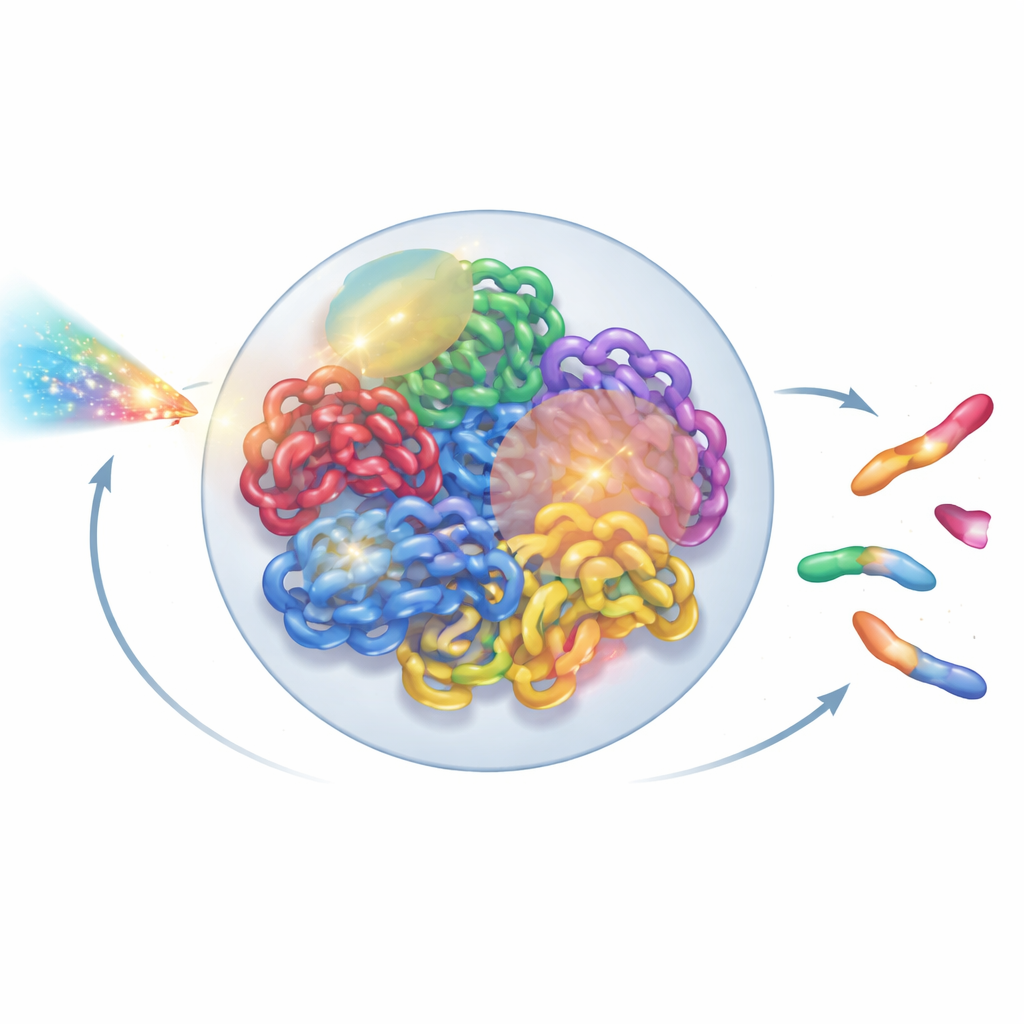
להביט בגנום כמבנה חי
בתוך כל תא אנושי, שני מטרים של DNA מקופלים לגרעין זעיר ברוחב של כמה מיקרומטרים בלבד. הקיפול הזה אינו אקראי: כל כרומוזום נוטה לתפוס טריטוריה משלו, המחולקת לשכונות ולמקבצי לולאות. כלים ניסיוניים חדשים, כמו מיקרוסקופיה ברזולוציה-יתר ומפות מגע Hi-C, חשפו סידור תלת־ממדי מפורט מאוד. עם זאת, רוב דגמי הקרינה עדיין מתייחסים ל-DNA כאל סבך מפושט של קווים או לולאות אידיאליות, ומתעלמים מהארגון המורכב הזה. המחברים ביקשו לבנות מודל של גרעין מלא שמשמר את מה שביולוגים למדו על הארכיטקטורה של הכרומטין, ועדיין מספיק מהיר להרצה במחשבי מעבדה רגילים.
בניית גרעין וירטואלי באמצעות פיזיקת פולימרים
הצוות דגם את הכרומוזומים כרצפים גמישים, שאבו רעיונות מפיזיקת הפולימרים — אותו תחום שמשמש להבנת פלסטיקים וחומרים רכים. הם פירקו את הבעיה לשלושה שלבי הרפיה כדי לרסן את העלות החישובית העצומה. ראשית, פרסו יחידות גדולות הנקראות דומיינים של כרומטין ברחבי הגרעין, אפשרו להן להדוף זו את זו, להימתח לאורך אורכן ולהתכנס לתת־מחסנים רחבים יותר. שנית, התמקדות פנימית בכל דומיין לפריסת סיבי הכרומטין הדקים יותר, כולל אזורים לולאתיים שמוחזקים יחד על ידי חלבוני קשירה. שלישית, איפשרו לכל הסיבים לשתף פעולה שוב בתוך גבול הגרעין כדי להגיע לתצורה סופית ריאליסטית. על ידי פיצול התהליך והוספת חיפוש היררכי וטריקים של חישוב מקבילי, הם הקטינו את זמן הריצה מארבעה חודשים בלתי פרקטיים לכדי כשלוש שעות לגרעין וירטואלי על תחנת עבודה עם 64 ליבות.
ממסלולי קרינה לשברים ותיקוני DNA
לאחר בניית הגרעין הווירטואלי, המחברים שמו מעליו מסלולי קרינה מפורטים שנוצרו בסימולציות Geant4-DNA. הם השתמשו בחיפוש היררכי כדי למצוא, לכל אירוע יינון, איזה דומיין כרומטין, מקטע סיב שנמצא ובאילו נוקלאוטיד היה הקרוב ביותר, מבלי לאחסן כלל את עשרת מיליארדי מיקומי הנוקלאוטידים בזיכרון. במקום זאת שמרו על תבנית כרומטין שניתנת לשימוש חוזר וביצעו טרנספורמציות קואורדינטיות חכמות בזמן ריצה. יינונים בגב ה-DNA טופלו כשברי גדיל, ושברים קרובים בגדילים מנוגדים הפכו לשברי דו־גדיל. כדי לחקות את מכונת התיקון של התא, המחברים הציגו כלל החיבור מחדש מבוסס-מרחק: קצוות DNA חופשיים שקרובים זו לזו נוטים יותר להתחבר שוב. החלטות ההחזרה התבצעו שלב אחרי שלב עד שכל הקצוות או שוויצו או נותרו בלתי מתוקנים, ושוחזרו הן תיקונים נכונים והן חיבורים שגויים של מקטעים.
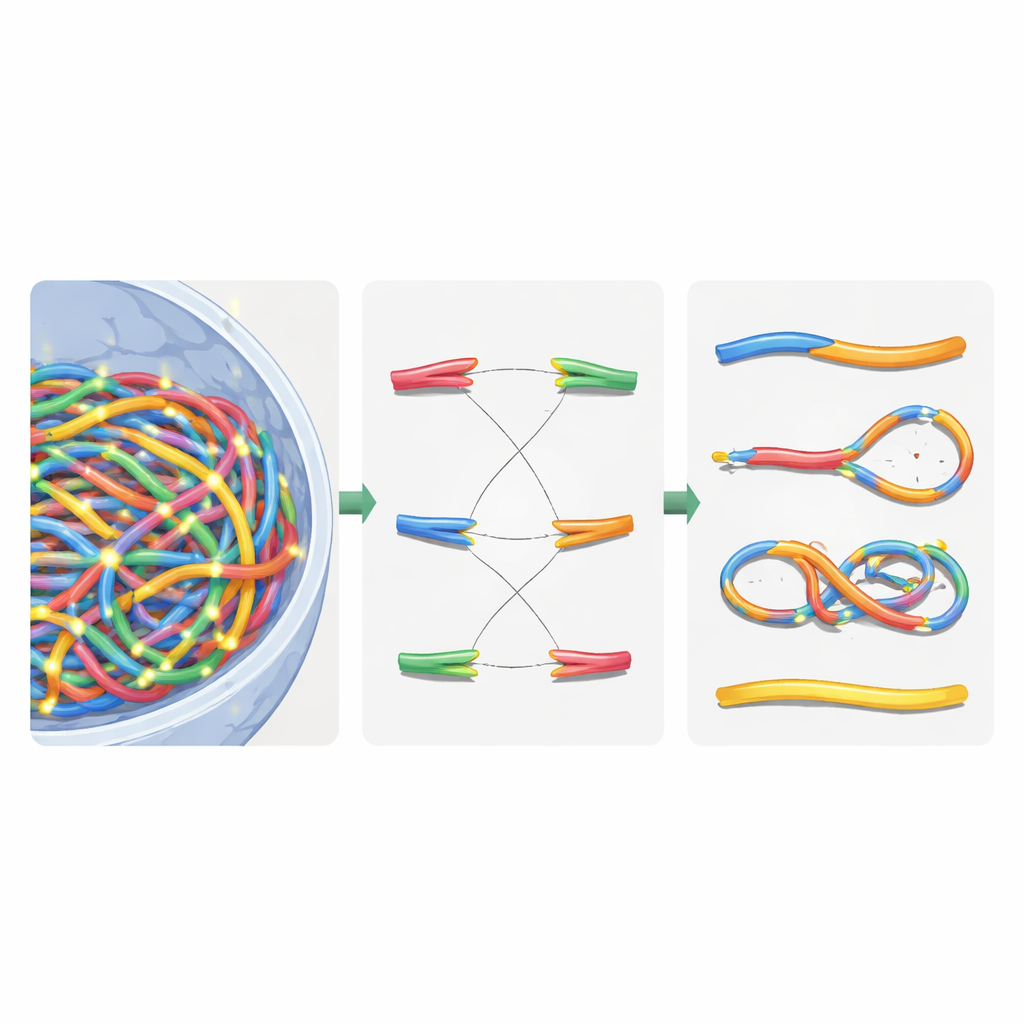
מיון כרומוזומים שבורים באמצעות לוגיקת רשת
לאחר תיקון וירטואלי זה, הגרעין הכיל תערובת של כרומוזומים מורכבים מחדש וחלקים שנותרו. כדי לסווג את מה שקרה, המחברים תרגמו את הגנום המתוקן לגרף בלתי ממויין: מקטעי כרומוזום הפכו לקשתות, וקצותיהם ונקודות השבר הפכו לקודקודים. באמצעות אלגוריתם רכיבים מחוברים סטנדרטי, הם יכלו לשחזר אוטומטית כל אובייקט דמוי-כרומוזום ולספור תכונות מפתח כגון מספר הצנטרומרות (נקודות ההיקשרות לחלוקת התא) והטלומרים (הקצוות הטבעיים). מתוך זה זיהו דיצנטרים (כרומוזומים עם שתי צנטרומרות), טבעות ומחיקות. לאחר מכן השוו את הסימולציות שלהם לניסויים קלאסיים בתאי עור אנושיים שנחשפו לקרני גמא וחלקיקי אלפא, ומצאו כי סך החריגות הכרומוזומליות שוחזר בערך בתוך כ-20% מהערכים הנמדדים — שיפור מהותי לעומת מודלים קודמים.
מה זה אומר למטופלים ולאסטרונאוטים
במילים פשוטות, עבודה זו מראה ש"היכן" ה-DNA יושב בגרעין ו"איך" הוא מקופל משפיעים בעוצמה על האופן שבו נזקי קרינה מצטברים לשינויים כרומוזומליים מסוכנים. על ידי שילוב ארכיטקטורת גנום תלת־ממדית מציאותית, סימולציה יעילה מבוססת פיזיקה וקריאת תוצאות באמצעות גרפים של כרומוזומים שבורים, המחברים מספקים גשר חזק בין ביולוגיה מבנית לרדיוביולוגיה. הם טוענים ששיפורים עתידיים — כגון הוספת תזמון תיקון מפורט ושימוש בנתוני רצף גנום מלא — עשויים להפוך את הגישה הזו לטובה עוד יותר בחיזוי ההשפעה הביולוגית של חלקיקי אנרגיה גבוהה בהם משתמשים בטיפולי סרטן או שנחשפים להם בחלל העמוק. בסופו של דבר, דגמים טובים יותר של "בית" ה-DNA בתוך תאי הגוף שלנו עשויים לסייע בהתאמת טיפולי קרינה בטוחים ויעילים יותר ולהעמיק את הבנתנו לגבי סיכוני קרינה בטווח הארוך.
ציטוט: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
מילות מפתח: נזק ל-DNA הנגרם מקרינה, ארכיטקטורת הכרומטין בתלת־ממד, חריגות כרומוזומליות, דוגמנות פיזיקת פולימרים, תרפיית חלקיקים