Clear Sky Science · he
הפעלה תעתיקית של PPP1R14C על ידי KLF7 משחררת פעילות CDK1 ומקדמת קרצינומה קשקשית של הריאה
מדוע הממצא הזה בסרטן הריאה חשוב
סרטן הריאה נשאר הגורם המוביל למקרי מוות ממחלה זו ברחבי העולם, וצורה עיקרית אחת — קרצינומה קשקשית של הריאה — נותרה מאחור בעידן התרופות הממוקדות. בשונה מסוגי גידולים ריאתיים אחרים שניתן לטפל בהם בעזרת תרופות שמכוונות למוטציות ספציפיות, תת‑הסוג הזה לעתים קרובות מאלץ רופאים להסתמך על כימותרפיה ואימונותרפיה, שאינן עובדות עבור כולם. המחקר חושף מעגל בקרה שהיה מוסתר עד כה בתוך תאי קרצינומה קשקשית של הריאה, שפועל כמו שיחרור הבלמים על חלוקת התאים, ומצביע על נקודת תורפה קונקרטית שתרופות עתידיות עשויות לנצל.
קישור חסר בסוג סרטן שקשה לטפל בו
החוקרים התחילו בחיפוש במאגרי סרטן ציבוריים גדולים כדי לבדוק האם ישנם גנים שבולטים בקרצינומה קשקשית של הריאה. אחד מהם, בשם PPP1R14C, הופיע בעקביות ברמות גבוהות בדגימות הגידול בהשוואה לרקמת ריאה תקינה. שכיחותו עלתה ככל שהסרטנים התקדמו לשלב מתקדם יותר, וחולים שלגידוליהם הייתה רמת מולקולה זו גבוהה חיו תקופות קצרות יותר. דפוסים אלה הופיעו הן ברמת ה‑RNA — ההודעות שהתא משתמש בהן לבניית חלבונים — והן ברמת החלבון עצמו, מה שמציין כי PPP1R14C לא רק נמצא אלא מעורב באופן פעיל בקידום המחלה. 
כיצד הגידולים משחררים את הבלמים
כדי להבין מדוע PPP1R14C שופע בגידולים אלה, הצוות פנה למתג ההדלקה/כיבוי של הגן — הפרומוטר שלו. באמצעות שילוב של מספר מאגרים שעוקבים אחרי נקודות קשירה של חלבוני בקרה שונים ל‑DNA, הם זיהו גורם בשם KLF7 כחשוד ראשי. בתאי קרצינומה קשקשית של הריאה שנגידו במעבדה, הגדלת רמות KLF7 גרמה לעלייה ב‑PPP1R14C, בעוד שהפחתת KLF7 הורידה אותה באופן חזק. ניסויים שבהם חיברו את פרומוטר PPP1R14C לדוחף פליטה אורות אישרו כי KLF7 יכול להפוך את המתג ישירות; שינוי רצף DNA קצר שבו KLF7 נקשר השמיד את ההשפעה. טכניקה של משיכת DNA הקשור ל‑KLF7 מתאים מהתאים הראתה כי הגורם יושב פיזית על פרומוטר PPP1R14C, ובכך חותמת את המקרה ש‑KLF7 מדליק את הגן ישירות.
ממתג גנטי להתנהגות אגרסיבית
לאחר שגילו מה דוחף את PPP1R14C, המדענים שאלו מה המולקולה עושה בפועל. בשורות תאי קרצינומה קשקשית של הריאה הם הורידו את PPP1R14C בעזרת כלים גנטיים וצפו בהתנהגות התאים. תאים חסרי PPP1R14C גדלו בקצב איטי יותר, יצרו פחות מושבות, חדרו דרך מעבר ג'ל פחות בקלות והיו בעלי סבירות גבוהה יותר לעבור מוות תכנותי של התא. התמונה ההפוכה גם היא נכונה: תאים שהונדסו לייצר עודף של PPP1R14C התחלקו מהר יותר, יצרו יותר מושבות וחדרו באופן אגרסיבי יותר. כאשר שתלו את התאים המותאמים בעכברים, גידולים עם PPP1R14C מופחת גדלו פחות ושקלו פחות. יחד, ממצאים אלה מראים כי PPP1R14C אינו צופה מהצד אלא מניע פעילויות סרטניות.
מבט שלב‑אחר‑שלב בתוך מנוע מחזור התא
בעומק רב יותר, הצוות חקר אילו תוכניות תאיות תלויות ב‑PPP1R14C. סקרים רחבים של פעילות גנים חשפו כי הסרת PPP1R14C פרעה במיוחד לגנים השולטים בנקודת הבדיקה הקריטית G2/M — הנקודה שבה התא מתחייב להתחלק לשניים. במרכז נקודה זו עומד CDK1, מתג מאסטר לכניסה למיטוזה. בתאים סרטניים בהם PPP1R14C גבוה, CDK1 נשא תג זרחון מפעיל והמטרות שמתחתיו נדלקו, מה שמעיד על אור ירוק לחלוקה. כאשר הפחיתו את PPP1R14C, ההפעלה הזו דעכה. ניסויים ביוכימיים הראו מדוע: PPP1R14C נקשר לאנזים "מוחק" תאי בשם PP1, שאחראי בדרך כלל להסרת תג הזרחון המפעיל מ‑CDK1. על ידי הידוק על PP1, PPP1R14C מונע ממנו להגיע ל‑CDK1, כך שאות ההפעלה נמשך והתאים ממשיכים להסתובב במחזור. 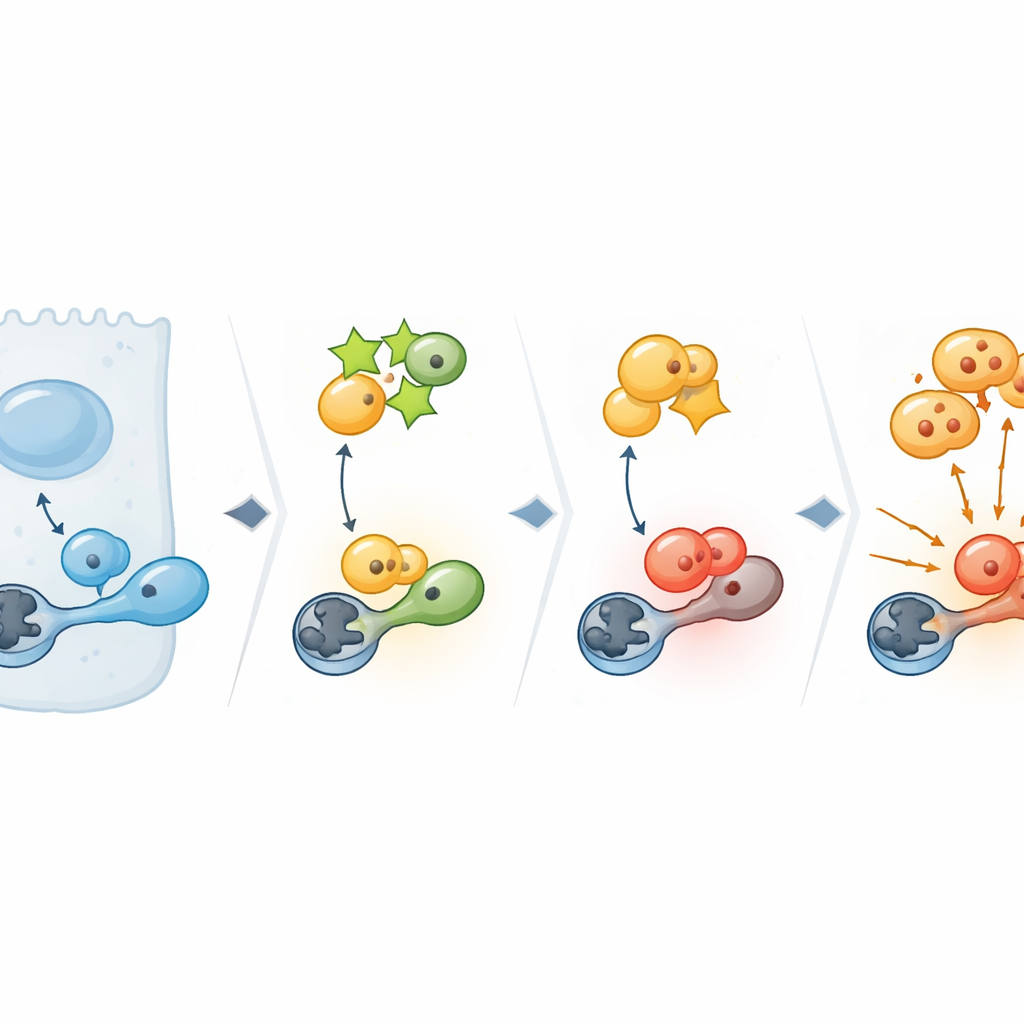
מהפיכה מולקולרית לרעיון טיפולי
החלק המעודד ביותר בעבודה הגיע כאשר החוקרים בחנו תרופה שחוסמת ישירות את CDK1. בתאים העמוסים ב‑PPP1R14C, המעכבת של CDK1 ביטלה את יתרון הצמיחה, הפחיתה יצירת מושבות וצמצמה את החדירה, ובאופן אפקטיבי החזירה את הבלמים ש‑PPP1R14C שחרר. הסקה של כל החלקים מציגה שרשרת אירועים ברורה: KLF7 מפעיל את PPP1R14C; PPP1R14C מנטרל את PP1; CDK1 נשאר היפראקטיבי; ותאי קרצינומה קשקשית של הריאה מתחלקים ללא מעצורים. עבור קוראים שאינם מומחים, משמעות הדבר היא שהמדענים זיהו גם דגל אזהרה — רמות גבוהות של PPP1R14C שמסמנות גידולים מסוכנים יותר — וגם מנוף מבטיח לטיפול: תרופות שמכבות את CDK1, ובמיוחד אצל מטופלים שהגידולים שלהם תלויים במעגל זה יוצא השליטה.
ציטוט: Xing, L., Yuan, C., Shen, X. et al. Transcriptional activation of PPP1R14C by KLF7 unleashes CDK1 activity to promote lung squamous cell carcinoma. Sci Rep 16, 9244 (2026). https://doi.org/10.1038/s41598-026-39174-3
מילות מפתח: קרצינומה קשקשית של הריאה, מחזור התא, CDK1, PPP1R14C, טיפול ממוקד