Clear Sky Science · he
חסר Dlgap2 מופר את הומיאוסטזיס הסינפטי על‑ידי קידום פירוק Itsn1 בתיווך ubiquitin במודל הדמוי אוטיזם המושרה על‑ידי חומצה ואלפרואית
מדוע תרופה נפוצה וחיווט המוח חשובים
חומצה ואלפרואית היא תרופה בשימוש ממושך לטיפול באפילפסיה ובהפרעות מצב רוח, אך כאשר נלקחת במהלך ההריון היא נקשרה לסיכון מוגבר לאוטיזם בילדים. המחקר הזה שואל שאלה חשובה עבור משפחות ורופאים: מה בדיוק עושה תרופה זו לחיווט המתפתח של המוח? על‑ידי מעקב אחר שינויים עד מולקולות ספציפיות בסינפסות — נקודות התקשורת בין תאי עצב — החוקרים חושפים שרשרת אירועים חדשה שיכולה להסביר התנהגויות דמויי‑אוטיזם ולהצביע על אסטרטגיות טיפול עתידיות. 
מסתכלים על מינים שונים כדי למצוא נקודות פגיעה משותפות
כדי למצוא רמזים מהימנים, הצוות לא הסתמך על מודל חיה יחיד. השוו מוחים או רקמות דמויות‑מוח מארגניונים קורטיקליים אנושיים, קופים, חולדות ועכברים שנחשפו לחומצה ואלפרואית לפני הלידה. באמצעות סקרים נרחבים של גנים וחלבונים זוהה סט קטן של גנים ששינו את ביטויים בכל המערכות הללו ושקשורים לסינפסות ולבידוד הסיבים העצביים. מתוכם בלט אחד: Dlgap2, חלבון שלד שמסייע בארגון הצדו́תנו‑פסי של סינפסות מעוררות. בעכברים שניתנה להם חומצה ואלפרואית פרה‑נטלית, רמות Dlgap2 ירדו בקורטקס ובאופן ספציפי בתוך תתי‑המחיצות הסינפטיות הזעירות, מה שמרמז שמולקולת שמירה על מבנה זו היא נפגעת מרכזית מחשיפה לתרופה.
משינויים מולקולריים לשינויים בהתנהגות
המחברים שאלו האם אובדן Dlgap2 בלבד מספיק להפר את תפקוד המוח. הם השתמשו בוירוסים נשאים של RNA קצר שיער (shRNA) כדי להפחית Dlgap2 בתאי עצב מותאיים של עכבר ובעכברים ניו‑בורן. בתרבית, נוירונים עם Dlgap2 נמוך פיתחו ענפים קצרים יותר והציגו פחות נקודות פוסט‑סינפטיות, סימנים לחיבורים מוחלשים. בחיות חיות, דיכוי ממוקד של Dlgap2 במוח ייצר התנהגויות דמויי‑אוטיזם: זכרים צעירים התקשו ללמוד את מיקום פלטפורמה מוסתרת במבוך מים והראו עניין מופחת בבן/בת זוג חברתיים ובחידוש חברתי במבחן שלוש‑תאים. השינויים הללו מחקים את הגירויים בלמידה ובחברה הנצפים בחיות שנחשפו לחומצה ואלפרואית, ומחזקים את הטענה שאובדן Dlgap2 אינו רק תופעת לוואי אלא גורם משני לשינויים בהתנהגות.
מוצאים שותף פגיע בסינפסה
כדי להבין כיצד אובדן Dlgap2 מהדהד בסינפסה, החוקרים הביטו מקרוב בחלבונים המעוגנים בצפיפות הפוסט‑סינפטית, משטח מולקולרי צפוף המקבל מסרים כימיים. באמצעות פרוטאומיקה נמצא כי הפחתת Dlgap2 שינתה את השפע של מאות חלבונים סינפטיים, במיוחד אלה המעורבים בארגון הסינפסות ובמיחזור וזיקולות על‑ידי אנדוציטוזה. חלבון אחד, Intersectin‑1 (Itsn1), ירד באופן בולט במיוחד. עבודות ביוכימיה נוספות הראו כי Dlgap2 ו‑Itsn1 יושבים פיזית באותם קומפלקסים חלבוניים בחלקים מועי‑סינפסות וכי שניהם מופיעים בין גנים המקושרים לאוטיזם. הדבר מצביע על שותפות רגולטורית ממוקדת בין שתי המולקולות בנוף סינפטי צפוף. 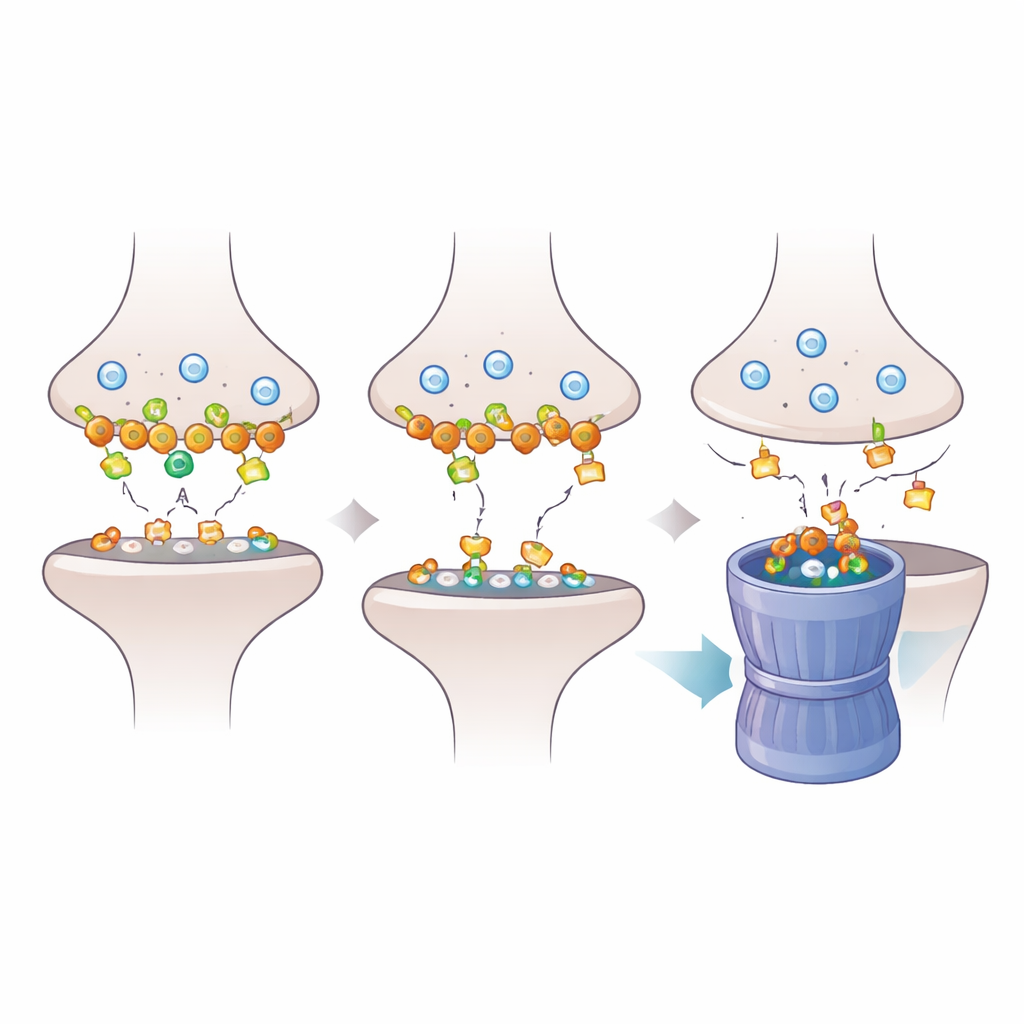
מסלול היפטרות חבוי מתגלה
הצוות שאל מדוע רמות Itsn1 יורדות כאשר Dlgap2 חסר. הם צפו שבתתי‑המחיצות הסינפטיות, דיכוי Dlgap2 עורר צורת תג‑חלבון הידועה כ‑K48‑קושרת ubiquitination, שמסמנת חלבונים לפירוק על‑ידי הפרוטאזום התאי — ה"מפצח" התאי. חסימת מערכת ההיפטרות הזו בעזרת התרופה MG132 מונעת את אובדן Itsn1, מה שמעיד כי Dlgap2 בדרך כלל מגן על Itsn1 מסימון והשמדה. ללא Dlgap2, Itsn1 מסומן יותר, מוזן לפרוטאזום ומתדלדל מהסינפסות, מה שפוגע במיחזור אנדוציטוטי ובאיזון הפעילות הסינפטית. המחקר מציע כי שינויים עדינים בקצב ההחלפה של חלבונים מרכזיים יכולים לייצב סינפסות בצורה לקויה במהלך התפתחות המוח.
מה זה אומר לגבי אוטיזם וטיפולים עתידיים
בהיקף, המחקר מציע רעיון פשוט אך חזק לקהל הרחב: חשיפה פרה‑נטלית לחומצה ואלפרואית יכולה להחליש חלבון "תומך" מבני (Dlgap2) בסינפסות. כאשר התומך הזה נאבד, חלבון שותפו (Itsn1) הופך יעד מוגבר להיפטרות התאית, מה שמוביל למיחזור לקוי של מרכיבי הסינפסה ולבסוף לחיבורים שגויים ולהתנהגויות דמויי‑אוטיזם בעכברים. אמנם גנים רבים וגורמים סביבתיים תורמים לאוטיזם, אך ציר Dlgap2–Itsn1 מספק שרשרת מולקולרית מוחשית מחשיפה פרה‑נטלית לשינוי בתפקוד המוח. בטווח הארוך, אסטרטגיות שישמרו שותפות זו או יתאימו את מכונת הפינוי החלבונית בסינפסות עלולות לעזור להגן על מוחות מתפתחים מפגיעות דומות.
ציטוט: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
מילות מפתח: חומצה ואלפרואית וההריון, חלבוני שלד סינפטיים, מנגנונים של ספקטרום האוטיזם, מסלול ה‑ubiquitin‑proteasome, מודלים של אוטיזם בעכברים