Clear Sky Science · he
זיהוי במחשב של אנטגוניסטים קטני‑מולקולה נשאפים ל‑IL‑33/ST2 עבור אנדוטיפים של אסתמה חמורה מסוג‑2‑גבוה
מדוע זה חשוב לנשימה
עבור מיליונים הסובלים מאסתמה חמורה, אפילו משאפים מודרניים והזרקות מתקדמות עלולים להשאיר אותם קצורי נשימה בסיכון להתקפים מסוכנים. המחקר בוחן האם תרופות מוכרות בסגנון טבליה ניתן לשכתב כך שיעבדו כטיפולים נשאפים החוסמים אחד מאותות ה"אזעקה" המוקדמים בריאות. באמצעות סימולציות מחשב בלבד חיפשו החוקרים מולקולות קטנות שעשויות להתאים על קולטן מרכזי המעורב באסתמה אלרגית חמורה, ומספקים בסיס לניסויים מעבדתיים עתידיים במקום להציע תרופה מוכנה לשימוש.
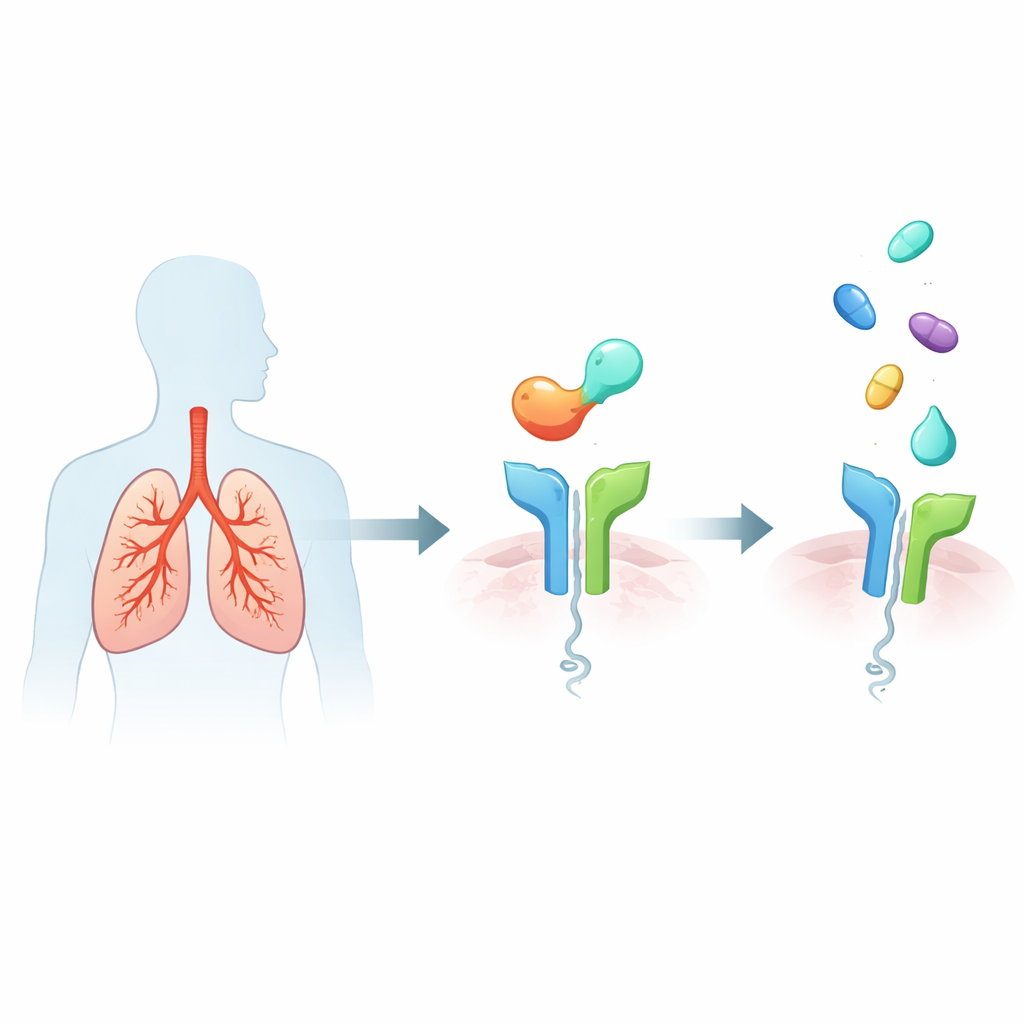
מערכת האזעקה בתוך ריאות של חולי אסתמה
אסתמה חמורה מסוג‑2‑גבוה מתאפיינת בתגובה חיסונית פעילה מאוד הממלאת את דרכי האוויר בריר ותאים דלקתיים, מצמצמת את צינורות הנשימה ופוגעת במבנה הריאה לאורך זמן. טריגר מרכזי הוא חלבון בשם IL‑33, שמשתחרר מתאי רירית המועלים. IL‑33 קושר את עצמו לקולטן בשם ST2 על תאים חיסוניים שונים, שגורמים לשחרור מולקולות מסר עוצמתיות המניעות תכונות אופייניות של אסתמה כגון צפצופים, החמרות ושינויי מבנה בדרכי האוויר. מאחר שרמות פעילות גבוהות של IL‑33/ST2 מקושרות לתסמינים חמורים ולהתקפים תכופים יותר, ST2 בלט כיעד אטרקטיבי מוקדם: חסימת ST2 עשויה להרגעת הרבה מהאותות הדלקתיים בהמשך הדרך בבת אחת.
מנוגדנים חיסוניים אל מול תרופות בסגנון יומיומי
כמה מטיפולים הקיימים לאסתמה חמורה משתמשים בנוגדנים מוזרקים הסופגים חלבונים דלקתיים בדם או יחסמו את קולטןם. למרות היעילות אצל חלק מהמטופלים, תרופות ביולוגיות אלה יקרות, ניתנות בהזרקה ומתמקדות בעיקר באותות בשלב מאוחר יותר של המסלול. בניגוד לכך, תרופות קטני‑מולקולה—במובן של פלס או משאפים מסורתיים—ניתנות לייצור בקנה מידה גדול, לאחסון בקלות, ועלולות להינתן ישירות לריאות. האתגר הוא ש‑ST2 נקשר ל‑IL‑33 דרך ממשק חלבון‑חלבון רחב, שקשה יותר למולקולות קטנות לשבש מאשר כיס עמוק ומוגדר באנזים. לכן פנו המחברים לנתוני מבנה ברזולוציה גבוהה של קומפלקס ST2–IL‑33 ולכלי in silico מודרניים כדי לבדוק האם תרופות אנטי‑דלקתיות ידועות עשויות, באופן בלתי צפוי, להתחבר לחלק מהממשק הזה.
חיפוש פני השטח של הקולטן בעזרת מחשב
באמצעות מבנה גבישי של ST2 אנושי קשור ל‑IL‑33, הצוות הסיר תחילה את IL‑33 לחשוף את משטח הקישור של הקולטן והשתמש בתוכנה לאיתור כיסים כדי לזהות את האזור המבטיח ביותר למולקולה קטנה להתמקם בו. לאחר מכן בחרו עשר מולקולות קליניות רלוונטיות שכבר משמשות באסתמה או במחלות חיסוניות קשורות—כגון חוסמי לוקוטריאנים מונטלוקסט וזאפרלוקסט, קרובי תרכובת של תיאלידומיד המשפיעים על המערכת החיסונית, ומעכבי JAK—בנוסף למולקולה ידועה ממוקדת ST2 כהשוואה. באמצעות תוכנת דוקינג וירטואלית מקמו כל תרכובת אלפי פעמים על פני שטח ST2, והתנוחות הטובות ביותר מדורגות לפי חוזק הקישור החזוי. זאפרלוקסט עלתה כשלד המדורג הגבוה ביותר, עם ביצועים מעט גבוהים יותר ממונטלוקסט ומהמשווה המכוון‑ST2 הידוע.
כוונון מולקולת עופרת על המסך
מכיוון ש‑Zafirlukast הראתה את האיזון המבטיח ביותר בין קישור צפוי להתנהגות דמויית‑תרופה כללית, השתמשו המחברים בכלי עיצוב מונחה‑בינה מלאכותית כדי ליצור גרסה משופרת של מולקולה זו. המטרה הייתה לשמור על אחיזתה ב‑ST2 תוך שיפור פרופיל הבטיחות החזוי. האנלוג שעוצב מחדש הציג ציון דוקינג דומה מאוד וניבוי של רעילות מופחתת במחשב. מיפויי מגע מפורטים הראו כי גם התרכובת המקורית וגם השונה נוגעות בכמה מאמינו‑חומצות של ST2 שמתקשרות בדרך‑כלל עם IL‑33, רומזות שהן מתמקמות בחלקים פונקציונליים חשובים של הממשק. הסימולציות המורחבות של דינמיקת מולקולות—חצי מיקרושנייה של תנועה וירטואלית במים ומלח—הראו שהקולטן והליגנד שניהם נשארים גמישים, כאשר המולקולה הקטנה מדגמנת מיקומים שונים לאורך המשטח במקום להיקשר במקום קשיח. חישובי אנרגיות אינטראקציה לאורך זמן הצביעו על התאחדות משמעותית אך דינמית, בהתאמה למולקולה הבוחנת משטח חלבון‑חלבון יחסית שטוח.
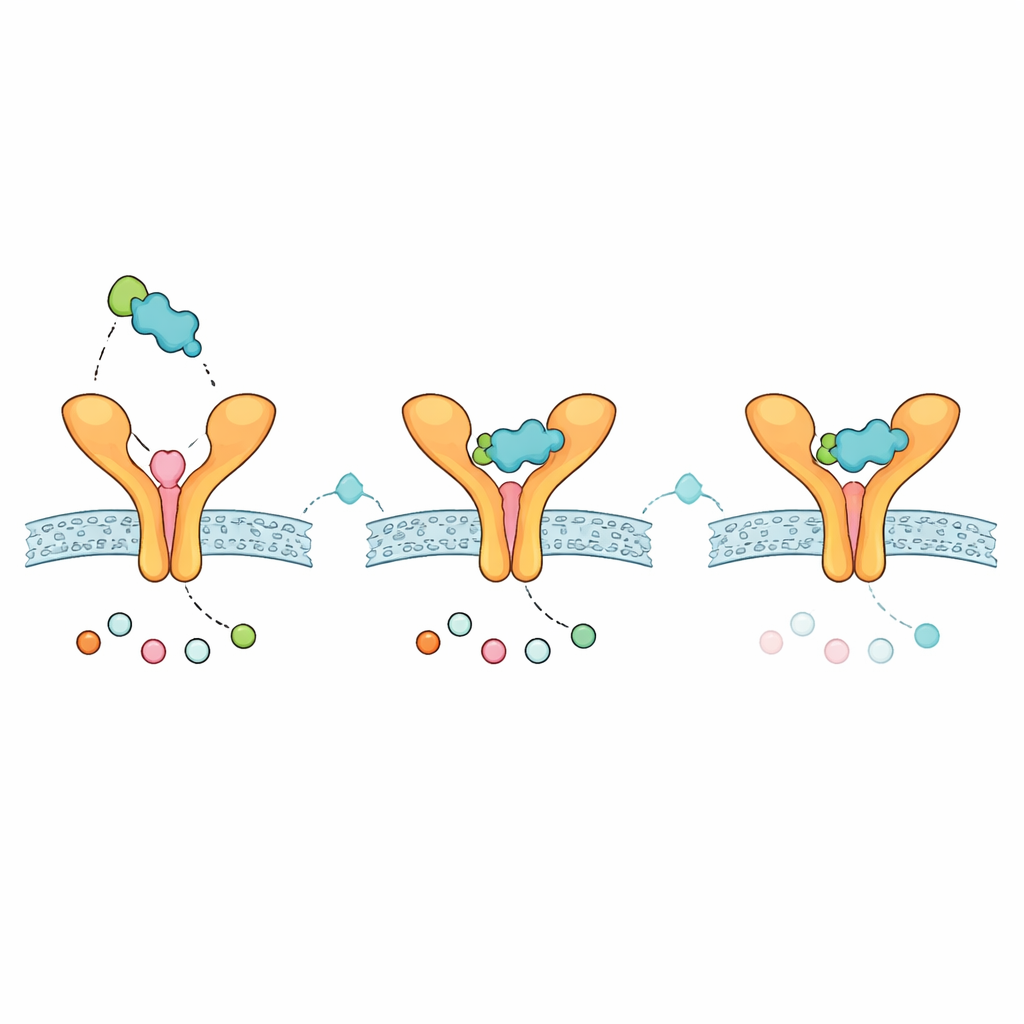
רמזים לגבי כיצד משאף עתידי עלול להתנהג
כדי לבדוק האם ה‑Zafirlukast המשופר יכול להתנהג באופן סביר כתרופה, ערכו הצוות בדיקות חישוביות סטנדרטיות של ספיגה, חלוקה, מטבוליזם, הפרשה ורעילות. האנלוג עמד בכללי דמויות‑תרופה אוראליים מקובלים, הציג גודל ושומניות מתונים, וניבא שיישאר מחוץ למוח—תכונות שעשויות להיות עדיפות לטיפול ממוקד‑ריאה עם תופעות לוואי מערכתיות מוגבלות. הערכות המסיסות השתנו לפי המודל, מה שאומר שיהיה צורך בניסוח זהיר, במיוחד לדרכי מתן שאינן אוראליות כגון שאיפה. בנוסף, החומר צפוי אינטראקציה עם אנזימי כבד מסוימים, דבר המצביע על כך שיש לתת תשומת לב לאינטראקציות תרופה‑תרופה אפשריות אם ישמש לצד תרופות אחרות.
מה שהעבודה הזו באמת מראה
במקום לספק תרופת אסתמה חדשה, מחקר זה מציג אסטרטגיה חישובית של צעד‑אחר‑צעד למציאת ולהשבחת מולקולות קטנות שעשויות להפריע למערכת האזעקה IL‑33/ST2 על משטח תאי דרכי האוויר. הוא מדגיש את Zafirlukast ובעל־הנבט שאופטימז על ידי בינה מלאכותית כנקודות התחלה סבירות לניסויים מעבדתיים, ומראה שהן יכולות לתפוס חלקים מרכזיים בממשק ST2 ולהציג תכונות בטיחות ודמויות‑תרופה צפויות המקובלות בכלליות. עם זאת, כל הראיות הן וירטואליות: העבודה אינה מוכיחה שמולקולות אלה חוסמות את קישור IL‑33 ל‑ST2, מדכאות איתות דלקתי או משפרות נשימה של מטופלים. תשובות אלו ידרשו בדיקות ביוכימיות, ניסויים בתאים, מודלים של בעלי חיים ולבסוף ניסויים קליניים. לעת עתה, המחקר מציע מפת דרכים חישובית ורשימת מועמדים קצרה של שלדים למדענים השואפים להפוך את מתג האזעקה של האסתמה ליעד תרופתי מעשי ונשאף.
ציטוט: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
מילות מפתח: אסתמה חמורה, מסלול IL‑33 ST2, אנטגוניסטים קטני‑מולקולה, עיצוב תרופתי במחשב (in silico), תרופות לנשימה בנשיפה