Clear Sky Science · he
שינוי בביטוי של ציר CD26/ADA בדלקת חיסונית של מונונוקלאוזיס זיהומי
למה הווירוס הילדותי הזה חשוב
הורים רבים מכירים את המונונוקלאוזיס הזיהומי, שנקרא לעתים ‘‘מונו’’, כהחלמה רעה אך בדרך כלל חולפת שמתאפיינת בחום, כאב גרון ובלוטות נפוחות. עם זאת, במיעוט מקרי ילדים ההדבקה יכולה להחמיר ולפגוע באיברים כמו הכבד. המחקר הזה בוחן במיקרוסקופ כיצד מערכות החיסון של ילדים מגיבות לוירוס אפשטיין–באר, הגורם העיקרי למונו, ומתמקד בזוג שותפים זעירים על פני התא — CD26 ופעיל אנזימטי בשם ADA — שעשויים להסביר מדוע תגובות חיסוניות מסוימות הופכות לעזות ומסוכנות.
מגינים בגוף שנמצאים בהגברה
כאשר וירוס אפשטיין–באר נכנס לגוף, הוא מדביק בעיקר תאי דם לבנים מסוימים ומעורר תגובת חיסון חזקה. במחקר זה השוו הרופאים דם מ־30 ילדים עם מונו אקוטי ל־30 ילדים בריאים. הם מצאו שלילדים החולים היו יותר תאי דם לבנים בסך הכל, בעיקר תת־קבוצה שנקראת תאי CD8 שמומחים להריגת תאים נגועים. במקביל, קבוצה חשובה מסייעת אחרת, תאי CD4, הייתה יחסית מופחתת, כך שהאיזון הרגיל בין תאי ‘‘התקפה’’ ל‘‘תמיכה’’ התהפך. גם רמות החלבונים הלוחמים בזיהום בדם, כולל מספר מולקולות איתות שמגבירות או מדכאות דלקת, היו גבוהות יותר, דבר שמראה שמערכת החיסון הופעלה במלואה.
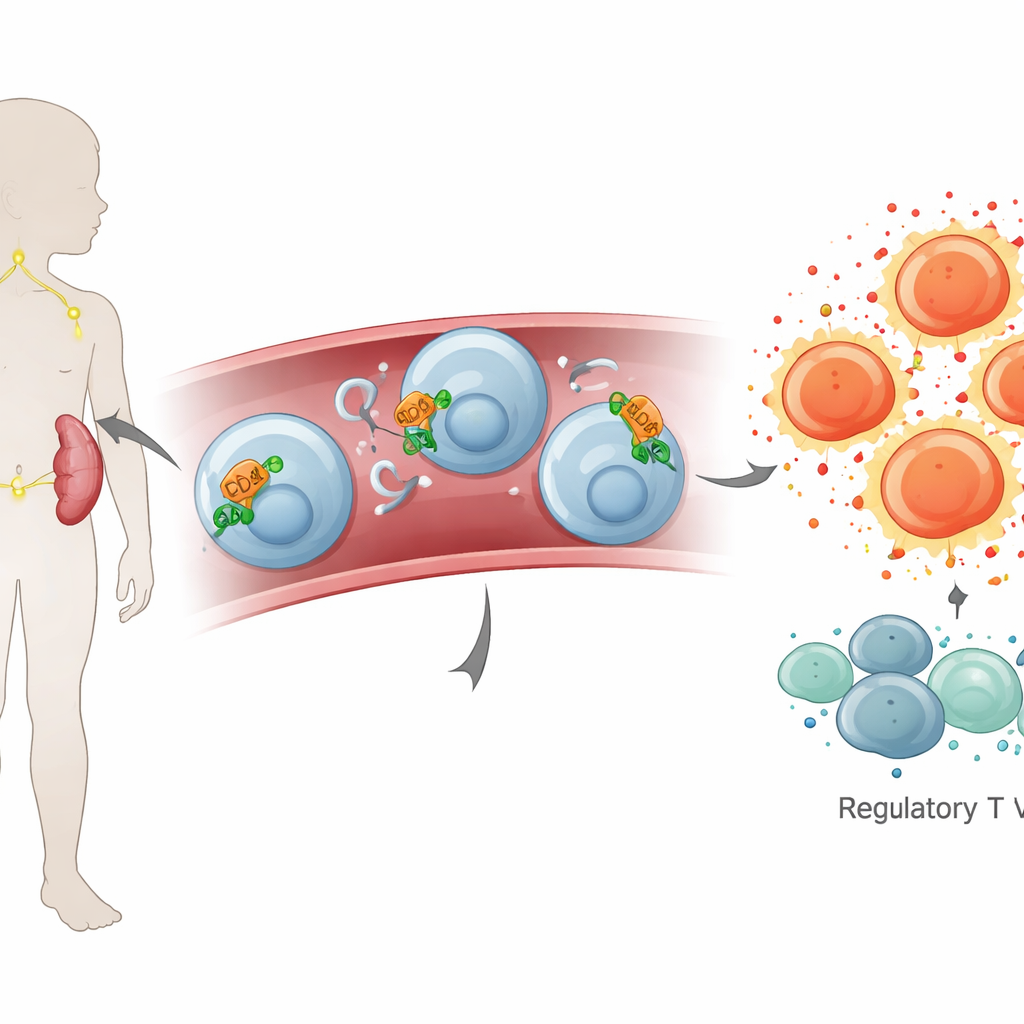
מבט צמוד על מתג שליטה זעיר
החוקרים כיוונו אז את העין אל CD26 ו־ADA, שתי מולקולות שיושבות בצומת שבין הפעלת תאים לאיתות כימי מחוץ לתאים. בעזרת בדיקות גנטיות על תאי דם הם מצאו שלילדים עם מונו היו רמות גבוהות יותר של הוראות ליצירת CD26 ו־ADA (mRNA), מה שמרמז שתאי החיסון התכוננו לייצר יותר מהחלבונים האלה. בדיקות דם איששו שפעילות ADA עצמה הייתה גבוהה יותר. באופן מעניין, כמות CD26 המסתובבת בפלזמה לא נבדלה במידה רבה בין החולים לבריאים, מה שמרמז שבמונו מולקולה זו עשויה להישאר בעיקר קשורה למשטחי התאים במקום לצוף בחופשיות.
הזזת האיזון בין התקפה להגבלה
כדי להבין כיצד מתג הבקרה הזה מתנהג על תאי חיסון שונים, הצוות השתמש בציטומטריית זרימה, שיטה שסופרת ומאפיינת תאים אחד־אחד. על תאי CD8, אלו שמתרחבים באופן דרמטי במהלך מונו, CD26 היה נפוץ יותר, בין אם או לא נשא התאים סימן נוסף שנקרא CD39 הקשור למערכת ברקס כימית עוצמתית. תבנית זו מרמזת שבתאים ‘‘הרוצחים’’ האלה CD26 עשוי לעזור להתגבר על אותות כימיים מקומיים שבדרך כלל היו מרגיעים את פעילותם, ובכך לתמוך בפעולת התקפה חזקה נגד תאים נגועים בנגיף. במקביל, בקרב תאי CD4 שבעבר מסייעים בתיאום תגובות חיסוניות, התמונה הייתה מעורבת יותר. תאים שנושאים גם CD4 וגם CD39 — שלעיתים קשורים לתפקידים רגולטוריים ומרגיעים — היו יחסית תכופים יותר, מה שעשוי להסביר רמות גבוהות של אותות מרגיעים כמו הציטוקין IL-10.
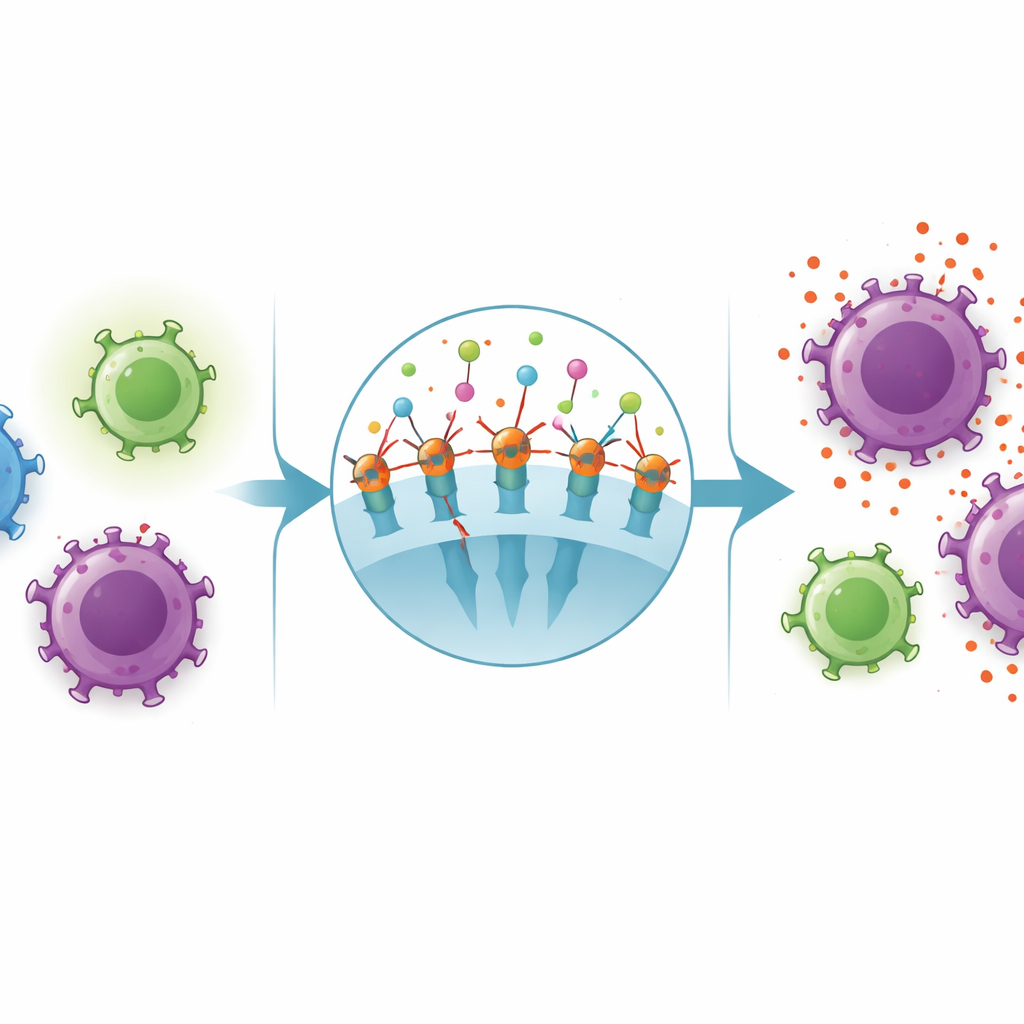
כשהוויסות נחלש
אולם, בתוך אוכלוסיית תאי CD4 שחסרה CD39 ובאופן טיפוסי מורכבת מתאי עזר פעילים, השבר של תאים שהציגו CD26 היה למעשה נמוך יותר בילדים עם מונו לעומת בני גילם הבריאים. אובדן זה של CD26 על תאי עזר עשוי להחליש את יכולתם להתרבות ולתאם תגובות מאוזנות, אפילו כאשר תאי CD8 נדחפים לפעילות מוגברת. המחקר גם הראה שכמות CD26 בפלזמה התואמה לרמות ADA ול־אינטרפרון־גמא, אות דלקתי עוצמתי, והייתה מקושרת ביחס הפוך לשיעור תאי CD4 וליחס CD4 ל־CD8. יחד, דפוסים אלה מצביעים על ציר CD26/ADA כקשור בקשר הדוק לעוצמת התגובה החיסונית במהלך ההדבקה.
מה זה אומר לגבי הילדים החולים
עבור משפחות והרופאים, הממצאים האלה מציעים תמונה ברורה יותר של מדוע וירוס שכיח יכול לעיתים להוביל למחלה מדאיגה. במונו האקוטי מערכת החיסון של הילדים נראית נשענת במידה רבה על תאי CD8 המצוידים בפעילות CD26–ADA מוגברת, דוחפת דחיפה אנטי־ויראלית חזקה שעלולה להחריג ולפגוע ברקמות. במקביל, תאי עזר ורגולטוריים מסוימים מאבדים או משנים את דפוסי CD26 שלהם, מה שעלול להחליש את הברקסים שמאחורי שליטת הדלקת. בעוד שדרוש מחקר נוסף — במיוחד במקרים קשים מאוד — המחקר הזה מציע שמדידה ובהמשך ויסות של ציר CD26/ADA עשויים יום אחד לסייע לרופאים להעריך חומרת המחלה או לעצב טיפולים שמרגיעים דלקת מזיקה בלי לכבות לחלוטין את הגנות הגוף.
ציטוט: Shi, T., Shi, W., Tian, J. et al. Altered expression of the CD26/ADA axis in immune-mediated inflammation of infectious mononucleosis. Sci Rep 16, 9316 (2026). https://doi.org/10.1038/s41598-026-38891-z
מילות מפתח: מונונוקלאוזיס זיהומי, ווירוס אפשטיין–באר, תאי T, וויסות חיסוני, נתיב האדנוזין