Clear Sky Science · he
הערכת הקשר האבולוציוני של חלבון הקשירה ל-TATA (TBP) עם תבניות קיפול שונות של דומיינים חלבוניים באמצעות מכונת וקטור תומכת (SVM)
כיצד חלבון "מפתח" של ה‑DNA מקשר אותו לאחרים רבים
חלבון קשירת ה‑TATA, או TBP, הוא סוס עבודה בתאינו: הוא מסייע בהדלקת גנים על‑ידי אחיזת ה‑DNA ברצפי פרומוטור רבים. המחקר הזה שואל שאלה שמסתמנת פשוטה אך בעלת משמעויות רחבות: האם קיימים חלבונים אחרים, בעלי תפקידים שמבחינה פונקציונלית שונים מאוד, שמשתפים בשקט את הצורה הבסיסית של ה‑TBP? באמצעות שילוב של השוואת מבנה תלת‑ממדי, ניתוח רצפים וכלי למידת מכונה מודרניים, המחברים מציירים קווי משפחה נסתרים בין ה‑TBP וחלבונים המעורבים במטבוליזם, בכימיה של נוירוטרנסמיטורים ואף במסלולים הקשורים לסרטן.
חלבון מפתח במרכז שליטת הגנים
TBP יושב בפתח הביטוי הגנטי ביצורים שמטווחם מנבגים ועד בני אדם. הוא מזהה רצף קצר של DNA שנקרא תיבת TATA ומעוות את ה‑DNA כדי לסייע בהרכבת המכונה הגדולה של השעתוק שמעתיקה גנים ל‑RNA. מאחר שהשלב הזה קריטי כל כך, הקיפול — הסידור התלת‑ממדי — של הליבה של TBP נשמר בחוזקה לאורך האבולוציה. המחברים מתמקדים במבנה TBP שנחקר היטב הידוע כ‑1tba ומשתמשים בו כגלאי לחיפוש חלבונים אחרים שעשויים לשתף את התכנון האדריכלי שלו, גם אם רצפי החומצות האמיניות שלהם ותפקידיהם היומיומיים נראים שונים במבט ראשון.
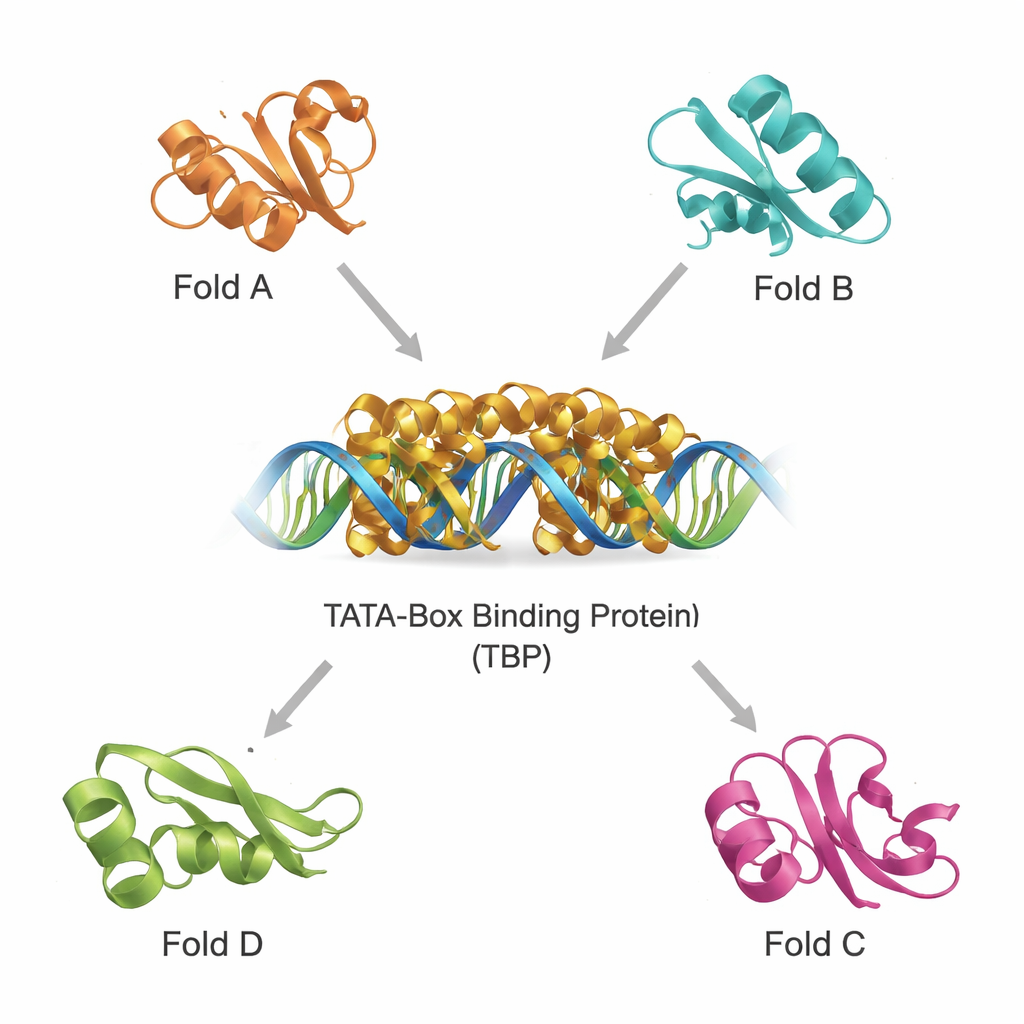
מחפש קרובים מבניים ביקום חלבוני צפוף
מסדי נתונים מודרניים מכילים מאות אלפי מבני חלבונים, מה שמאפשר לסרוק אחר קרובים מרוחקים לפי צורה תלת‑ממדית ולא רק לפי רצף. באמצעות שני כלים רבי‑עוצמה, DALI ו‑TOP‑search, הצוות משך תחילה חלבונים שקיפולם נראה דומה לזה של TBP. לאחר מכן הם סיווגו את המועמדים עם קטלוג דומיינים אבולוציוני והצרו אותם לקבוצה קטנה של דוגמאות בעלות דמיון מבני אך מגוון פונקציונלי. אלה כוללים אנזים היוצר גלוטמין החשוב במטבוליזם, דומיין המצוי בכמה אנזימים המטפלים ב‑tRNA, אנזים בעל קיפול אופייני בצורת "הוט‑דוג" המעורב בכימיה של חומצות שומן, וחלבונים שסייעים ביצירת טטרהידרו‑ביופטרין, מולקולה חשובה לתפקוד המוח. החפפה של המבנים שלהם עם TBP הראתה כי למרות תפקידים שונים, הם חולקים מוטיבים ליבתיים ניתנים לזיהוי.
לימוד מכונות לזהות משפחות חלבון נסתרות
כדי להתקדם מעבר לבדיקה מקרה‑מקרה, המחברים בנו מודלים של למידת מכונה שיכולים לסמן אוטומטית קיפולים דמויי‑TBP. הם הרכיבו קבוצות גדולות של רצפי חלבונים הידועים כשייכים ל‑TBP או לכל אחד מהקיפולים הקשורים, יחד עם קבוצת "רקע" רחבה של חלבונים לא קשורים. כל חלבון הומר לסכמות מספריות פשוטות: תדירות הופעת כל חומצת אמינו וכמה פעמים מופיעה כל צמד חומצות אמינו ברצף. פרופילים אלה הוזנו למכונות וקטור תומכת (SVM) ולמודלים של יער אקראי (random forest), שלמדו להבחין בין סוג קיפול אחד לכל האחרים. בעזרת אימות־חוצי מוקפד, המודלים הגיעו לדיוק מאוד גבוה — לעתים מעל 95 אחוז — אפילו כאשר אומנו רק על חלקים מהרצפים המתאימים לאיזורים שמורים.
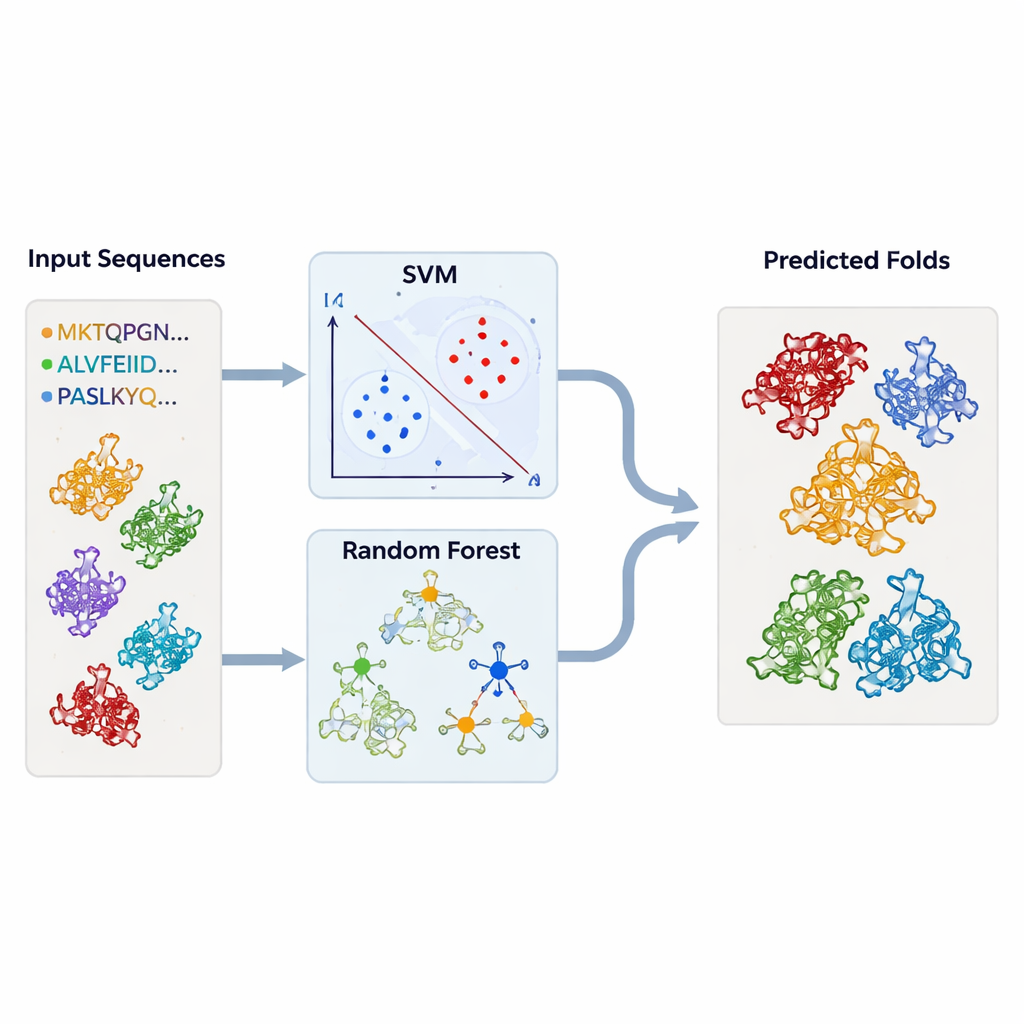
מבחן המודלים על אלפי מבנים לא ידועים
מצוידים בממיינים מאומנים אלה, הצוות חזר למסדי המבנה. הם הריצו אלפי שרשראות חלבון — שהושגו מ‑DALI ו‑TOP‑search — דרך המודלים שלהם כדי לראות אילו נושאים את החתימות הסטטיסטיות של קיפולי TBP או קיפולים קשורים. גישת ה‑SVM והיער האקראי התאחדו ברובן ובחרו מועמדים רבים שמכשירי המבנה גם סימנו כדומים. במקרים מסוימים, אנזימים בעלי פעילויות לכאורה לא קשורות צברו בכל זאת יחד באופן חזק עם TBP או זה עם זה, מה שמחזק את הרעיון שאבולוציה יכולה למשתמש באותו מסגרת בסיסית למשימות ביוכימיות שונות רבות.
מדוע הקשרים הנסתרים הללו חשובים
המחקר מסכם כי ל‑TBP יש שורש מבני עמוק משותף עם כמה משפחות אנזימים, כולל חלבונים דמויי גלוטמין סינתטאז ודומייני עריכה של אנזימי עיבוד tRNA. גם כאשר הרצפים דהו והתפקידים התפצלו, חלבונים אלה שומרים מוטיבים אדריכליים משותפים, מה שמרמז על ירידה ממקור משותף. עבור הקורא הלא‑מומחה, המסר המרכזי הוא שהטבע נוטה למחזר עיצובים מצליחים: קיפול אחד יכול להיות מותאם פעמים רבות כדי לפתור בעיות שונות מאוד, מהפעלת גנים ועד לכיול מטבוליזם וכימיה מוחית. באמצעות שילוב של השוואת מבנים תלת‑ממדית ולמידת מכונה, המחברים מספקים ארגז כלים מעשי לחשיפת קשרים כאלה, המסייע לביולוגים לחזות מה חלבונים לא מאופיינים עשויים לעשות ומכוון מפתחים של תרופות לעבר מטרות חדשות, מונחות אבולוציה, במסלולים הרלוונטיים למחלה.
ציטוט: Selvaraj, M.K., Kaur, J. Evaluating the evolutionary relationship of TATA binding protein (TBP) with various folding patterns of protein domains using support vector machine (SVM). Sci Rep 16, 7696 (2026). https://doi.org/10.1038/s41598-026-38883-z
מילות מפתח: חלבון קשירת TATA-box, אבולוציה של חלבונים, למידת מכונה, מבנה חלבון, מכונת וקטור תומכת