Clear Sky Science · he
פרופיל פארמקוגנומי של ABCB1 ו-CES1 בחולי פרפור פרוזדורים המקבלים דביגטרן מקוהורט מולטי-אתני מלזי
מדוע הגנים שלכם עשויים להשפיע על מדללי הדם
רבים מהאנשים עם קצב לב בלתי סדיר הנקרא פרפור פרוזדורים נוטלים כדורים המדללים את הדם כדי למנוע שבץ. תרופות אלה, כולל אחת הנקראת דביגטרן, בדרך כלל ניתנות במינון זהה לרוב המבוגרים. עם זאת, אצל חלק מהאנשים רמות התרופה בגוף יהיו גבוהות מדי או נמוכות מדי, מה שעלול להגדיל את הסיכון לדימום חמור או לקרישת דם. המחקר הזה שואל שאלה פשוטה אך חשובה: האם הגנים של אדם יכולים להסביר מדוע דביגטרן פועל אחרת ממטופל למטופל במרפאה במציאות היומיומית במלזיה?
בעיה נפוצה בקצב הלב וכדור בשימוש נרחב
פרפור פרוזדורים הוא אחד מההפרעות בתדירות הלב השכיחות בעולם ומעלה את הסיכון לשבץ במספר רב. כדי להפחית סיכון זה, לרוב נרשמים למטופלים מדללי דם. במלזיה, רופאים משתמשים יותר ויותר בתרופות חדשות הידועות כנוגדי קרישה אורליים ישירים במקום התרופה הישנה וורפרין. דביגטרן היא אחת מהאפשרויות החדשות האלה ופופולרית כי לרוב אינה דורשת בדיקות דם תכופות לכיול המינון. עם זאת, רופאים עדיין מבחינים בהבדלים משמעותיים בכמות הדביגטרן בדם של מטופלים ובחוזק ההשפעה המדללת, אף כשהם מקבלים את אותו המינון.
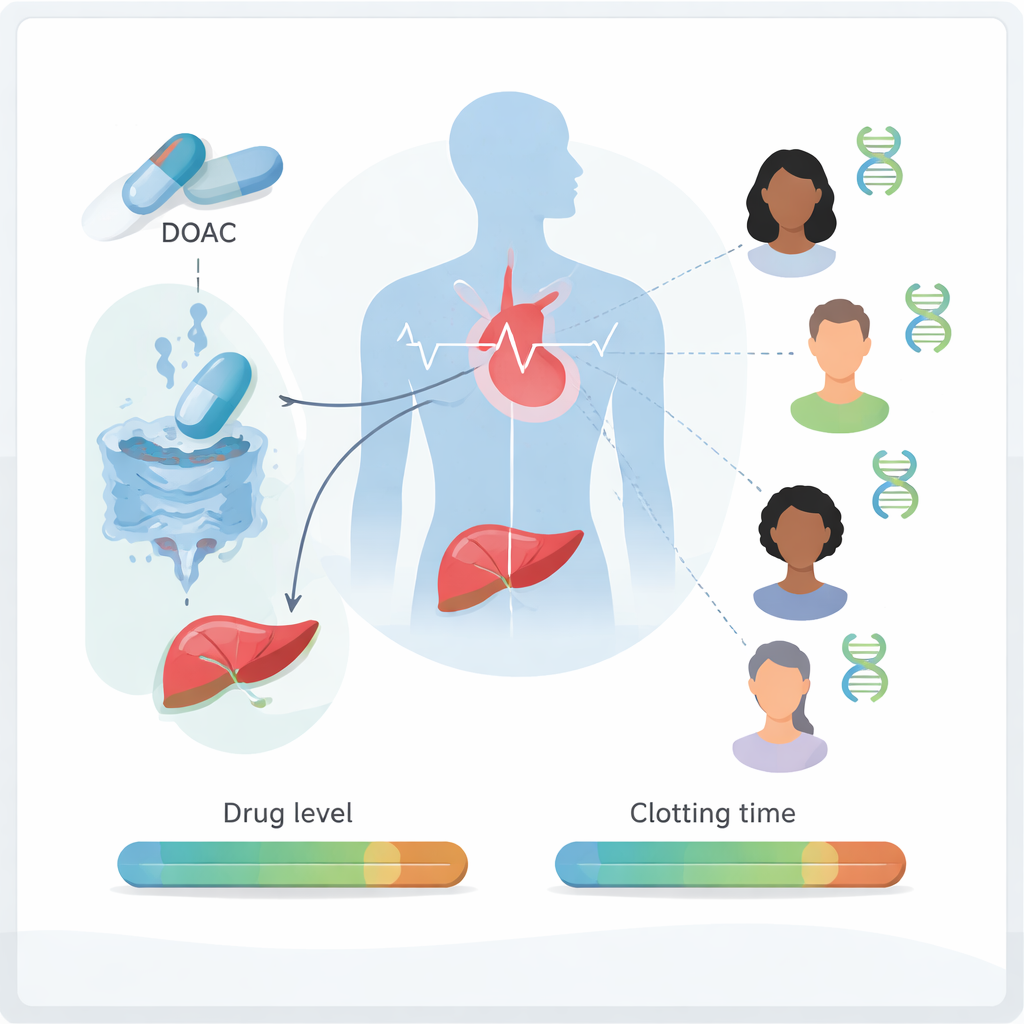
התבוננות בדם וב-DNA
כדי לחקור הבדלים אלה, החוקרים גייסו 180 מטופלים מלזים עם פרפור פרוזדורים שקיבלו דביגטרן. הקבוצה שיקפה את התמהיל הרב-אתני של המדינה, כולל סינים, מלאים וקהילות ילידיות. במהלך ביקור במרפאה נלקח דם ישר לפני המנה הבאה, כאשר רמות הדביגטרן נמוכות ביותר — הרמה הקרויה trough. חלק מהדגימה שימש למדידה מדויקת של כמות התרופה בדם, וחלק אחר למדידת משך זמן הקרישה, מדד מעשי לחוזק ההשפעה המדללת. במקביל חילצו את ה-DNA והשתמשו בטכנולוגיות ריצוף מודרניות לסריקה של האורך המלא של שני הגנים, ABCB1 ו-CES1, המסייעים לשלוט בהובלה ובפירוק של דביגטרן בגוף.
הבדלים גדולים ברמות, רמזים מתונים מהגנים
המטופלים הראו שונות בולטת ברמות דביגטרן: אצל חלק כמעט לא זוהתה תרופה, בעוד אצל אחרים היו כמעט 300 יחידות בדם. זמני הקרישה השתנו גם הם במידה נרחבת, וכצפוי רמות תרופה גבוהות יותר לוות עם זמני קרישה ארוכים יותר. גיל מבוגר, תפקוד כלייתי ירוד והיות אישה נטו להיות קשורים לרמות תרופה גבוהות יותר ולזמני קרישה ממושכים יותר. באופן מפתיע, המינון שנרשם — האם המטופלים קיבלו את המינון הסטנדרטי 150 מ"ג פעמיים ביום או את המינון הנמוך 110 מ"ג פעמיים ביום — לא הבחין בצורה ברורה בין קבוצות של רמות גבוהות ונמוכות בהקשר המציאותי הזה.
מה הסריקה הגנטית הראתה ומה לא
כאשר הבודקים בחנו מאות הבדלים עדינים באיות בגן ABCB1 ובגן CES1, הם מצאו עשרות אתרים שנראו, במבט ראשון, קשורים לרמות דביגטרן או לזמן הקרישה. רוב השינויים הללו היו באזורים לא מקודדים של ה-DNA שמסייעים לשלוט בהדלקה וכיבוי של גנים, ולא בחלקים המקודדים לחלבון עצמם. שבעה-עשר אתרים חפפו, מרמזים על מתגים משותפים שעשויים להשפיע גם על כמות הדביגטרן שנכנסת למחזור הדם וגם על השפעתה על הקרישה. עם זאת, ברגע שהצוות יישם בדיקות סטטיסטיות מחמירות כדי למנוע תוצאות חיוביות שגויות, אף אחד מהאותות הגנטיים הללו לא נשאר חזק מספיק כדי להיחשב כמובהק. תוצאי קליניים כגון שבץ, בעיות לב או דימום היו מלבד המזל נדירים במהלך שנה, מה שחדשות טובות למטופלים, אך הקשה על קישור חד משמעי בין כל וריאנט גנטי לאירועים במציאות היומית.
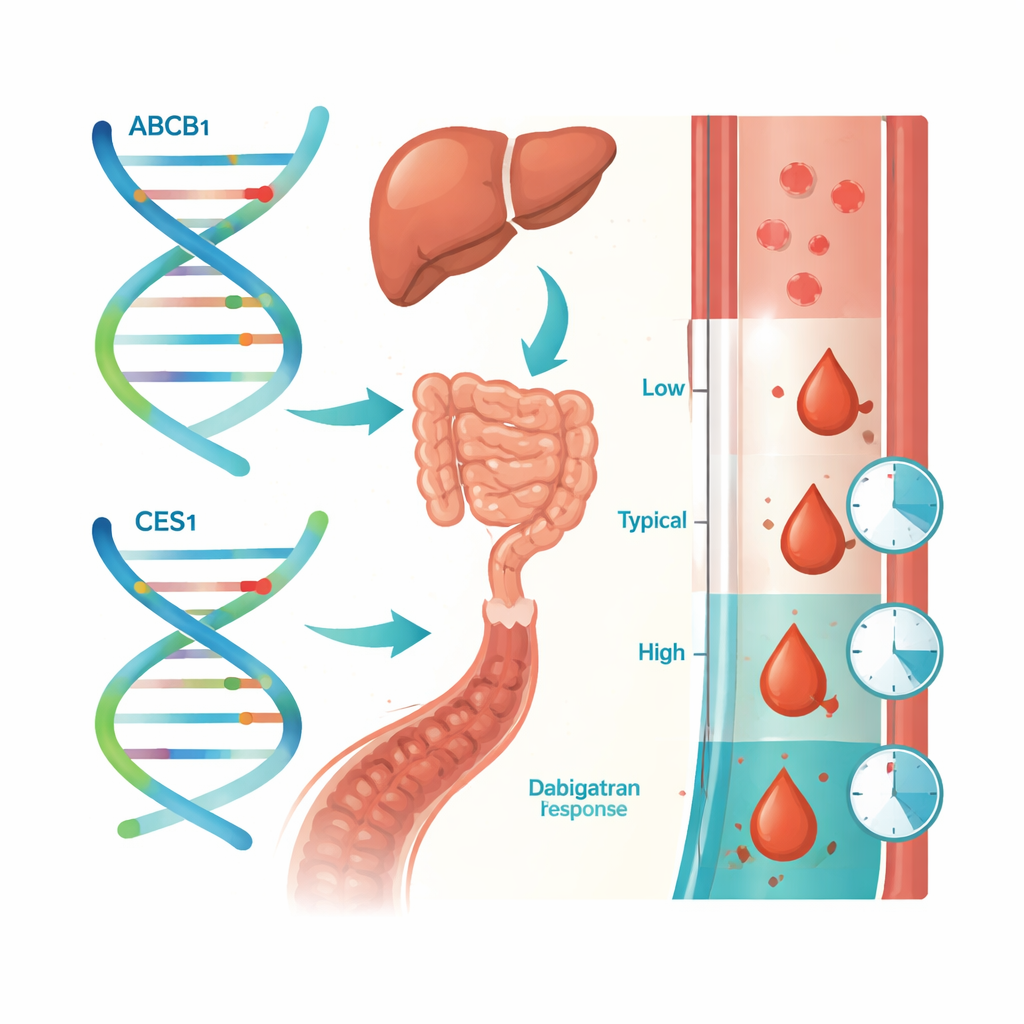
מה משמעות הדבר עבור מטופלים וטיפול עתידי
כרגע המחקר מצביע על כך שכשיש שינויים גנטיים בגן האחראי על טיפול בתרופות הם כנראה תורמים למידה מסוימת לאופן בו יחידים מגיבים לדביגטרן, אך אין לנו עדיין סימנים גנטיים ברורים ומבוססים קלינית שהרופאים יכולים להשתמש בהם כדי לכוונן מינון, לפחות באוכלוסייה המלזית הזו. המחקר מדגיש עד כמה תגובות למדללי דם יכולות להיות מורכבות, נשלטות על ידי גיל, תפקוד כליות, מין וסביר להניח הרבה השפעות גנטיות קטנות הפועלות יחד. העבודה גם מדגישה מדוע חשוב לחקור אוכלוסיות מגוונות במקום להסתמך רק על נתונים מאירופה או מצפון אמריקה. יידרשו מחקרים רחבים יותר, רב-מרכזיים שמשלבים גנטיקה, מדידות מדויקות של תרופות ומעקב מפורט לפני שתאימת מינון מבוססת גנים של דביגטרן תיכלל בשגרה היומיומית.
ציטוט: Tan, S.S.N., Sim, E.UH., Jinam, T.A. et al. Pharmacogenomic profiling of ABCB1 and CES1 in atrial fibrillation patients on dabigatran from a multiethnic Malaysian cohort. Sci Rep 16, 7539 (2026). https://doi.org/10.1038/s41598-026-38856-2
מילות מפתח: פרפור פרוזדורים, דביגטרן, מדללי דם, פארמקוגנומיקה, בדיקה גנטית