Clear Sky Science · he
קובעי רמת-חומצה אמינית של יציבות תרמית של האנדוליזין האקסטרמופילי Ts2631
מדוע וירוסים החובבים חום חשובים עבור אנטיביוטיקות עתידיות
ככל שעמידות לאנטיביוטיקה עולה, המדענים ממהרים למצוא דרכים חדשות להרוג חיידקים מסוכנים. גישה מבטיחה אחת שואבת כלי נשק מוירוסים שמדביקים חיידקים, הנקראים בקטריופאז'. וירוסים אלה מייצרים אנזימים, הנקראים אנדוליזינים, שחוררים את דופן התא החיידקי. המחקר המוצג כאן מתמקד באנדוליזין עמיד בחום באופן יוצא דופן, Ts2631, שמקורו בווירוס שחי במעיינות חמים באיסלנד. על ידי גילוי אילו אבני בניין בודדות של חלבון זה עושות אותו יציב כל‑כך בטמפרטורות הקרובות לרתיחה, החוקרים מקווים לעצב אנזימים אנטיבקטריאליים חזקים ועמידים יותר לשימושים רפואיים וביוטכנולוגיים. 
כלי ויראלי שנוצר במעיינות שרותות
Ts2631 מגיע מבקטריופאז' שמדביק את החיידק החובב‑חום Thermus scotoductus, שמצטיין במים שמגיעים הרבה מעל 60 °C. האנזים Ts2631 חותך קשר מסוים בפפטידוגליקאן, הרשת החזקה שמקיפה תאי חיידק. מה שמבחין את Ts2631 הוא יציבותו התרמית הקיצונית: הוא נשאר מקופל עד בערך 100–105 °C, תלוי בממס. זה הרבה מעל הטמפרטורות שבהן רוב החלבונים מתפרקים. המחברים השוו את Ts2631 לקרובו הנחקר היטב מוירוס בטמפרטורה מתונה, איימן ה‑T7 lysozyme, כדי להבין אילו טריקים מבניים הטבע השתמש כדי לשמור על Ts2631 בשלמותו בתנאים כה קשוחים.
לולאות קצרות ותערובת שונה של אבני בניין
חלבונים הם שרשרות של 20 סוגי חומצות אמינו, המקופלות לצורות מורכבות. כאשר החוקרים חפפו את המבנים התלת‑ממדיים של Ts2631 ושל T7 lysozyme, הם מצאו שהארכיטקטורה הכללית דומה מאוד: לשניהם ליבת קומפקטית של לולאות אלפא‑הליקס וסטרנדס. ההבדל המרכזי הוא באזורי הלולאה הגמישים שמחברים את האלמנטים הללו. ב‑Ts2631 הלולאות קצרות יותר ומראות גמישות נמוכה יותר, בעוד של־T7 lysozyme יש לולאות ארוכות ורופפות יותר. ל‑Ts2631 גם יש יותר ממספר חומצות אמינו שנקשרות לעתים קרובות לעמידות בחום: פרולין הקשיח; שיירים ארומטיים כגון טירוזין וטריפטופן; וארגינין בעלי מטען חיובי. באותו הזמן יש בו פחות שרונים של סרין, חומצת אספרטית וגלוטמית, שעלולות להפוך חלבונים לפגיעים בטמפרטורות גבוהות. דפוס זה מתקיים לא רק בהשוואה ל‑T7 lysozyme אלא גם כאשר משווים את Ts2631 למאות אלפי חלבונים ויראליים ולעשרות מיליוני חלבונים חיידקיים.
החלפת חומצות אמינו בודדות כדי לבדוק את חשיבותן
כדי לעבור מקורלציות להסבר סיבתי, הצוות החליף באופן שיטתי 55 חומצות אמינו בודדות ב‑Ts2631 ומדד כיצד כל מוטציה השפיעה על טמפרטורת ההיתוך (Tm) ועל יכולת האנזים לפרק דפנות חיידק. כמה שינויים סביב האתר הפעיל המכיל אבץ היו מזיקים במיוחד. כאשר הם שינו שלושה שרידים המקושרים לאבץ (H30, H131 ו‑C139), ה‑Tm של החלבון ירד בעד כ‑20 °C, והפעילות אבד. שני טירוזינים שמורים (Y60 ו‑Y69) גם הם תרמו ליציבות. באופן מפתיע, הסרת קשר די‑סולפיד — סוג של קישור קוולנטי בין ציסטאינים C80 ו‑C90 — דווקא העלתה את טמפרטורת ההיתוך, אף על פי שהשמידה את הפעילות. זה מדגים שעצם היותו יציב מאד בצינור מבחן לא תמיד אומר שהחלבון יתפקד טוב יותר בתנאים ממשיים. 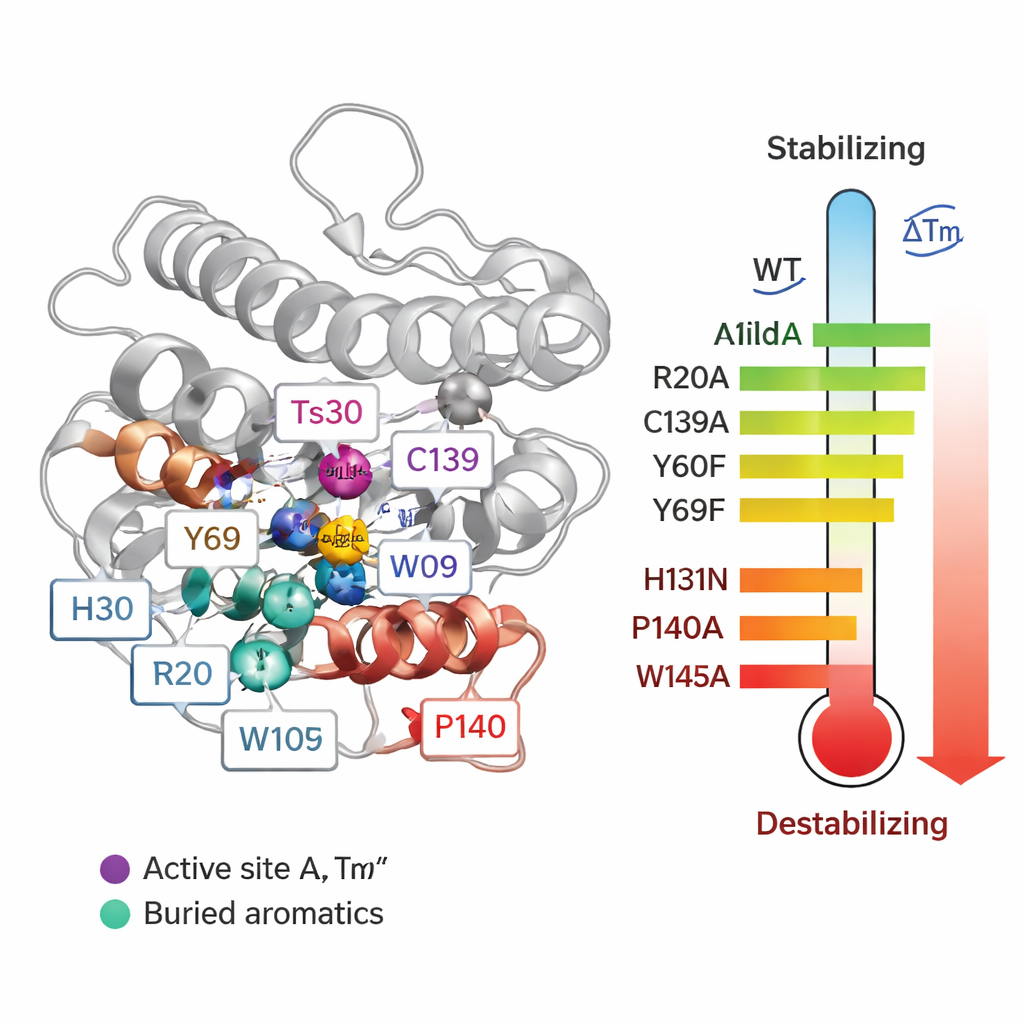
"עוגנים" ארומטיים חבויים ואחיזה מרכזית בדופן החיידק
התוצאות הבולטות ביותר הגיעו ממוטציות בפרולין ובטריפטופן. החלפת פרולין בודד (P140), הממוקם סמוך מאוד לציסטאין הקושר אבץ C139, הפחיתה את ה‑Tm ביותר מ‑21 °C וחלשה את הפעילות אחרי חימום, משום שהמוטציה הפרה גאומטריית קישור מתכת מיוחדת שנחוצה לקשירה נכונה של היונר. כמה טריפטופנים שקועים עמוק (W102, W109 ובמיוחד W145) גם הם היו קריטיים: החלפתם לאלאנין גרמה לירידות ב‑Tm של 14–24 °C והפכה את האנזים לרגיש הרבה יותר לחום במבחני פעילות. שיירים ארומטיים אלה פועלים כעוגנים פנימיים הנועלים את ליבת החלבון במקומה. בין הארגינינים, לרוב היה מעט השפעה על היציבות, אבל R20 התברר כחיוני לאחיזת הפפטידוגליקן. כאשר R20 הוחלף, האנזים התקשה לקשור את דופן התא החיידקי ואיבד פעילות בחימום, מה שמראה שחלק מהשרידים תורמים יותר לתפקוד מאשר לעמידות תרמית טהורה.
מאנזימים של מעיינות חמות לאנטיבקטריאלים חזקים יותר
בסך הכל, המחקר מראה שהעמידות התרמית החריגה של Ts2631 מתבססת על חבילת חומצות אמינו ממוקמות היטב במקום על חיזוק אחיד של כל החלבון. שרידי קשירת האבץ, פרולין שמור ליד האתר הפעיל ושיירים ארומטיים שקועים מהווים ליבה מייצבת, בעוד שתכונות מייצבות קלאסיות כמו קשרי די‑סולפיד או גשרים מלחים פחות חשובות כאן ממה שציפו. לשדה הרחב יותר, העבודה מרמזת שניתן להפוך אנדוליזינים מזניים מזופילים (טמפרטורה מתונה) לעמידים יותר על‑ידי החלפה מדודה של עמדות נבחרות לטריפטופן או לפרולין מבלי לוותר על פעילות אנטיבקטריאלית. במילים אחרות, על‑ידי לימוד האופן שבו הטבע בונה אנזימים שמתעלמים מטמפרטורות קרובות לרתיחה, המדענים מקבלים מתווה מעשי להנדסה של антибиотיקה מבוססת חלבון אמינה ועמידה יותר לאורך זמן.
ציטוט: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
מילות מפתח: אנדוליזין עמיד בחום, אנזימי בקטריופאז', יציבות תרמית של חלבונים, עמידות אנטיביוטית, הנדסת חלבונים